Материал: ВОЗ Алгоритм лаборатоной диагностики ТБ 2017
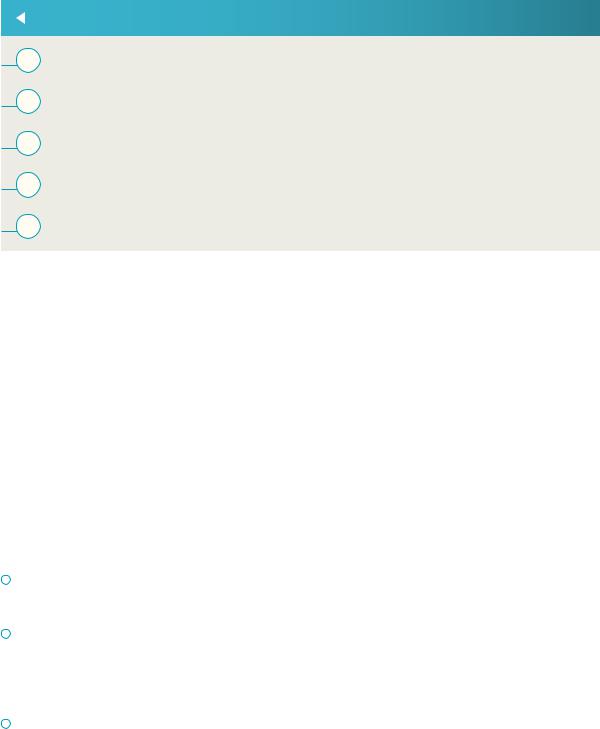
Алгоритмы для лабораторной диагностики и мониторинга состояния больных ТБ и МЛУ-ТБ в процессе лечени
Сноски к Рис. 2
1
2
3
4
5
Проведение быстрого молекулярного теста на первичных образцах мокроты для выявления лекарственной устойчивости (например, Xpert или LPA) сокращает задержку с получением соответствующих результатов фенотипического теста на лекарственную чувствительность
LPA к препаратам второго ряда подходят для проведения в референс-лабораториях центрального или национального уровня, или регионального уровня при наличии необходимой инфраструктуры.
Если исследование микроскопии мазка и/или посева дают положительный результат для образца, полученного через два месяца после начала лечения, для подтверждения наличия/отсутствия МБТ и для определения модели лекарственной устойчивости предлагается провести молекулярный тест, рекомендованный ВОЗ, и ТЛЧ.
До начала проведения молекулярного теста, рекомендованного ВОЗ, необходимо проверить результаты молекулярных тестов для предыдущих изолятов того же пациента для гарантии того, что выбранный молекулярный тест сможет выявить дополнительную устойчивость.
Согласно критериям соответствия
В данном случае цель диагностического тестирования состоит в определении успешности лечения. Проведения повторного ТЛЧ обычно не требуется, за исключением случаев сохранения положительных результатов микроскопии и посева у больного или наличия данных о сопутствующем контакте с больным МЛУ-ТБ (т.е. потенциальная суперинфекция), или ухудшения клинического состояния больного. Лаборатория должна быть информирована о том, что полученный образец прислан для исследования лишь с целью оценки успешности лечения.
Алгоритм мониторинга состояния больных туберкулезом легких с множественной лекарственной устойчивостью и устойчивостью к рифампицину в процессе лечения
Этот алгоритм представлен на рисунке 3.
Культуральные и микроскопические исследования 1–2 образцов мокроты следует проводить ежемесячно (начиная с третьего месяца) на протяжении всей интенсивной фазы лечения (28-30).
После абациллирования по посеву (т.е. после получения двух последовательных отрицательных результатов посева, проведенных с промежутком не менее 30 дней), культуральные исследования можно проводить каждые три месяца, а микроскопию мазка мокроты – ежемесячно (28) или согласно временным рамкам протокола лечения, принятого в стране.
Если результат микроскопии мазка становится положительным, и когда получен положительный результат посева, следует провести LPA-анализ для препаратов второго ряда и фТЛЧ для дополнительных противотуберкулезных препаратов (нет необходимости повторять исходные тесты на чувствительность к рифампицину, поскольку устойчивость к этому препарату сохранится).
13
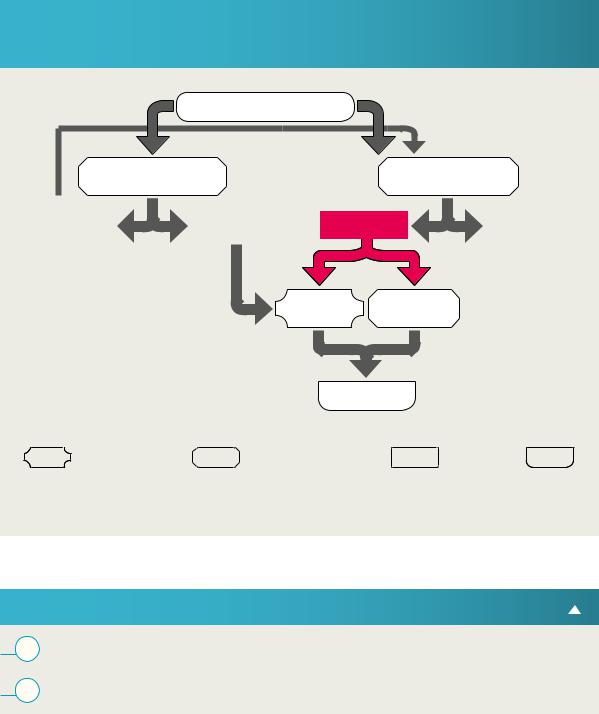
Aлгоритм лабораторной диагностики и мониторинга лечения туберкулеза легких и туберкулеза с лекарственной устойчивостью на основе применения современных быстрых молекулярных методов
Рис. 3. Алгоритм мониторинга состояния больных с МЛУ-ТБ и устойчивостью к рифампицину в процессе лечения
Два образца мокроты
Микроскопия (бактериальная нагрузка, Посев
инфекционность)
КУМ-отрицательный |
|
КУМ-положительный |
|
МБТ выявлены |
|
МБТ не выявлены |
||
|
|
|
|
|
|
|
|
|
фТЛЧк
LPAкпрепаратам дополнительным второгоряда1 противотуберкулезным
препаратам2
Индивидуально
подобранная лекарственная схема
Методы быстрой молекулярной |
Традиционные диагностические |
Результаты |
Лечение |
диагностики туберкулеза, |
методы (микроскопия или |
диагностических |
|
одобренные ВОЗ |
фенотипические методы, основанные |
исследований |
|
|
на посеве) |
|
|
Сноски к Рис. 3
1
2
Проводить, только если ранее не было выявлено устойчивости к препаратам второго ряда (FLQ и инъекционным препаратам второго ряда)
Нет необходимости повторять исходные тесты на чувствительность к рифампицину, поскольку устойчивость к препарату сохранится.
14

Практические вопросы, касающиеся диагностического алгоритма
Практические вопросы, касающиеся
диагностического алгоритма
Лаборатории разных уровней в лабораторной сети проводят разные исследования. В некоторых странах лаборатории, занимающиеся диагностикой разных инфекций (не туберкулезной) с применением ПЦР, могут располагать инфраструктурой и обученным персоналом для выполнения LPA-анализов, тем более что во многих странах диагностика туберкулеза объединена с
клиническими микробиологическими исследованиями по другим заболеваниям
Результаты всех исследований, проводимых на более низких уровнях лабораторной сети, следует направлять в национальную референс-лабораторию (НРЛ) вместе с образцами и/или изолятами культур. Это позволит предотвратить нерациональное дублирование исследований (за исключением некоторой доли образцов, используемых в целях контроля качества). Европейская сеть референс-лабораторий Европейского центра по контролю и профилактике заболеваний опубликовала руководство с подробным описанием методологий тестирования
(31).
ВОЗ рекомендует заменять традиционное исследование микроскопии мазка быстрыми молекулярными тестами (такими как GeneXpert MTB/RIF) для проведения первичной диагностики туберкулеза (3, 17, 24, 25, 32). Если ресурсы позволяют, необходимо исследовать два образца для повышения чувствительности теста. Таким образом, микроскопические исследования будут ограничены тестированием образцов, положительных на туберкулез, выявленный с применением быстрых молекулярных методов, для оценки степени инфекционной опасности пациента в целях инфекционного контроля, а также для мониторинга лечения. Продолжение практики практики проведения микроскопических исследований также позволяет сохранить наработанные навыки в этой сфере на случай, если молекулярные исследования окажутся недоступными.
15

Aлгоритм лабораторной диагностики и мониторинга лечения туберкулеза легких и туберкулеза с лекарственной устойчивостью на основе применения современных быстрых молекулярных методов
Предпочтительные диагностические методы
Несмотря на использование средств молекулярной диагностики необходимо сохранять потенциал выполнения таких исследований, как микроскопия мазка, посев и ТЛЧ. Исследования микроскопии и посевов особенно важны для мониторинга лечения. Наличие молекулярных диагностических тестов не исключает необходимости проведения традиционных исследований-микроскопии мазка, посева и ТЛЧ; микроскопические и культуральные исследования и культуральные исследования остаются необходимыми для контроля за лечением. В настоящее время посевы обеспечивают максимальную диагностическую чувствительность, в то время как традиционные ТЛЧ нужны в помощь диагностике ШЛУ-ТБ и позволяют подобрать соответствующую схему лечения больных М/ШЛУ-ТБ. В будущем, в зависимости от эпидемиологической ситуации, потребности в традиционных методах могут измениться.
Светодиодная люминесцентная микроскопия является рекомендованным методом микроскопии для всех уровней лабораторий (33). Светодиодная и традиционная люминесцентная микроскопия как минимум на 10% более чувствительны, чем микроскопия по методу Циль-Нильсена. Однако при сравнении с традиционной люминесцентной микроскопий светодиодная микроскопия оказывается менее дорогостоящей (33).
Посевы рекомендуется проводить как на плотных, так и на жидких средах. Посевы на жидких средах более чувствительные и быстрые, чем посевы на плотных средах
(результативность повышается на 10%) (34).Результаты посевов на жидких средах можно получить в течение нескольких дней, но они более подвержены контаминации, имеют более высокую стоимость и ассоциированы с повышенным риском биобезопасности. При положительных результатх посева, необходимо провести видовую идентификацию изолята для определения принадлежности к комплексу МБТ или к нетуберкулезным микобактериям. Подтверждение принадлежности к комплексу МБТ проводится посредством биохимических тестов, методов молекулярной амплификации или иммунохроматографических анализов. Последние два рекомендованы для видовой идентификации изолятов культур, поскольку они обеспечивают быструю и точную идентификацию микобактерий комплекса МБТ.
Лекарственную устойчивость можно выявить генотипическими и фенотипическими методами. Автоматизированные системы на жидких средах являются золотым стандартом для ТЛЧ к препаратам первого и второго ряда (34). Проведение ТЛЧ требует соблюдения рекомендаций ВОЗ и применения обязательных методов обеспечения качества (29, 34, 35). При проведении ТЛЧ к препаратам второго ряда следует стремиться к включению тестирования чувствительности к аминогликозидам, полипептидам и фторхинолонам,
применяемым в стране. Результаты ТЛЧ к этим препаратам имеют хорошую достоверность и воспроизводимость, позволяют проводить диагностику ШЛУ-ТБ гарантированного качества. С внедрением LPA-анализа для препаратов второго ряда с целью выявления устойчивости к фторхинолонам и инъекционным препаратам второго ряда появилась возможность получать результаты устойчивости к этим препаратам в более короткие сроки.
16
Практические вопросы, касающиеся диагностического алгоритма
При прямом тестировании LPA-анализ для препаратов второго ряда выявляет 86% больных с устойчивостью к фторхинолону, 87% – с устойчивостью к инъекционным препаратам второго ряда и 69% – ШЛУ-ТБ; во всех случаях тест редко выдает ложноположительный результат (26). Интерпретируя результаты, следует помнить, что LPA-анализ для препаратов второго ряда не может определить устойчивость к отдельным фторхинолонам. Ведущие к устойчивости мутации, выявленные при помощи LPA-анализа для препаратов второго ряда, в высокой степени коррелируются с фенотипической устойчивостью к офлоксацину и левофлоксацину. Однако остается неясной корреляция этих мутаций с фенотипической устойчивостью
к моксифлоксацину и гатифлоксацину, |
|
|
и для включения моксифлоксацина или |
При прямом тестировании |
|
гатифлоксацина в схему лечения МЛУ-ТБ |
||
лучше всего руководствоваться результатами |
LPA-анализ для препаратов |
|
|
||
фТЛЧ (26). Мутации в некоторых регионах |
второго ряда выявляет 86% |
|
генома комплекса МБТ (таких как промоторная |
||
область eis) могут быть ответственны за |
больных с устойчивостью |
|
появление устойчивости к одному препарату |
||
класса (группы) больше, чем к другим |
к фторхинолону, 87% |
|
|
||
препаратам внутри того же класса (группы). |
– с устойчивостью к |
|
Например, мутация eis C14T ассоциирована |
||
с устойчивостью к канамицину в штаммах из |
инъекционным препаратам |
|
Восточной Европы (26). |
||
Некоммерческие методы для посевов и ТЛЧ, |
второго ряда и 69% – ШЛУ-ТБ; |
|
во всех случаях тест редко |
||
включая метод микроскопического наблюдения |
||
за лекарственной чувствительностью (MODS), |
выдает ложноположительный |
|
методы с использованием колориметрического |
||
результат |
||
окислительно-восстановительного |
||
индикатора и нитратредуктазная реакция |
|
|
(NRA), также рекомендованы Всемирной |
|
организацией здравоохранения (36). В настоящее время эти тесты рассматривают в качестве промежуточного решения в процессе подготовки к расширению масштабов генотипического тестирования. По сравнению с коммерческими, эти системы дешевле, однако они могут быть более подвержены ошибкам вследствие отсутствия стандартизации; они в большей степени зависимы от квалификации оператора и подходят для использования только на уровне референс-лабораторий.
В настоящее время рекомендованные ВОЗ молекулярные диагностические тесты включают LPA-анализ и Xpert MTB/RIF (а также петлевую изотермическую амплификацию (LAMP) только для диагностики туберкулеза). Данные систематических обзоров и мета-анализов указывают на то, что при сравнении с традиционным ТЛЧ, LPA -анализы демонстрируют высокую чувствительность (≥97%) и специфичность (≥99%) для выявления устойчивости к рифампицину или к комбинации рифампицина и изониазида (чувствительность ≥90%; специфичность ≥99%) на изолятах МБТ и образцах с положительным результатом микроскопии мазка мокроты
(23, 37, 38).
17