Материал: Совершенствование технологии получения адсорбентов из местных полиминеральных глин
В исследованном образце бентонита (Рис.1.1.),
как показывают рентгенографические данные наблюдается большое количество
максимумов, что отражает сложную кристаллическую слоистую структуру глины.
Преобладает SiO2 с
характерными рефлексами 2q = 210, 270, 36,60 и 39,50. (наиболее
интенсивные рефлексы). Для AI2O3
наиболее характерные рефлексы при 2q = 29,60, в
интервале 42-440 и 47-500.
Рис. 1.1. Электронно-микроскопические данные
образцов исходного бентонита
При РЭМ - исследованиях видно, что сами частицы исходного бентонита имеют зернистую структуру и при больших увеличениях имеют геометрическую форму, что соответствует кристаллической природе бентонита.
Производство масел из восточных нефтей сильно отличается от производства масел из старых промышленно освоенных нефтей. Открытие новых перспективных месторождений высокопарафинистых сернистых, смолистых нефтей вызывает необходимость разработки новых способов и подходов их переработки для получения качественных масел.
Для улучшения качеств нефтяных масел в работе рассматривается вопрос подбора селективных адсорбентов на основе местного Навбахорского бентонита для удаления нежелательных компонентов масляных фракций, ухудшающих эксплуатационные свойства.
Поскольку исходный бентонит и продукт его
кислотно-термической активации обладают определенными значениями удельной
поверхности, следует полагать, что они будут обладать поглотительными
способностями.
1.4 Адсорбционная
активность бентонита Навбахорского месторождения по нефтяным компонентам
Для определения емкости бентонита в статических и динамических условиях из жидкой фазы по различным нефтяным компонентам и приготовления их модельных растворов выбран циклогексан, как наиболее инертный растворитель, адсорбционный индекс которого довольно низок 3,30 и который должен быть высокой степени чистоты.
Циклогексан, полученный любым из существующих методов, требует тщательной очистки от сопутствующих примесей. Разделить смесь циклогексана от примесей обычной перегонкой затруднительно. О чистоте циклогексана судить по коэффициенту преломления также трудно: различное сочетание циклогексана, бензола, метилциклопентана, а также наличие влаги может дать значение показателя преломления, близкое к значениям показателя преломления для чистого циклогексана, в то время как в нем может быть значительное количество этих примесей. Наиболее правильным критерием чистоты продукта является температура его кристаллизации, которая для циклогексана (100-ной степени чистоты) равна 6,520С.
Данные Маскарелли [103] о температурах кристаллизации системы бензол-циклогексан показывают, что кривая температуры выпадения циклогексана из раствора при вымораживании падает круто и эвтектическая точка приходится на температуру - 43,70С, что соответствует содержанию 24,2% бензола в смеси.
Было показано, что в области высоких концентраций циклогексана (97 мол. % и выше) коэффициент преломления не является достоверным критерием чистоты циклогексана, и здесь необходимо определить температуру кристаллизации. Для этого предложен адсорбционный способ очистки циклогексана до температуры кристаллизации 6,400С и выше с использованием силикагелей, активированных углей и цеолитов: наиболее оптимальным адсорбентом являются активированные угли, в частности угли СКТ и БАУ. Наиболее полную информацию об углях можно подшепнуть из [93].
В данной работе для очистки циклогексана - до 99,00% степени чистоты использовался уголь БАУ - березовый активированный уголь.
Очистка циклогексана до требуемых норм осуществлялась следующим способом: уголь БАУ фр 0,25-0,5мм предварительно просушенный в сушильном шкафу при температуре 160-1800С в течение 6 часов, загружался в стеклянную колонку (обыкновенную бюретку с краником), можно в делительную воронку, и через адсорбент непрерывно пропускался циклогексан с заранее определенной температурой кристаллизации и собирался в отдельные приемники. Для каждого фильтрата определялась температура кристаллизации. Скорость фильтрации циклогексана через адсорбент - 1 капля в 1 сек. По окончании очистки пробы с одинаковыми температурами кристаллизации сливались в единую колбу. Составлялся баланс выхода чистого циклогексана.
В работе все растворы готовились на циклогексане с температурой кристаллизации 6,400С.
Адсорбция в статических условиях. Так как в состав моторного масла входят углеводороды, сняты изотермы адсорбции н-гексана и самого моторного масла селективной очистки (продукция Ферганского НПЗ), из неполярного растворителя циклогексана из жидкой фазы на исходном и кислотноактивированном образцах бентонита (фр. 0,25-0,5мм). Образцы сорбентов высушены при температуре 160-1800С в течении 6 часов. При этом условно допускали, что вся адсорбированная вода удаляется с поверхности сорбента, а гидроксильный покров бентонита оставался нетронутым.
Растворы готовились 1, 2, 3, 4, 5 %-ной концентрации. Измерения производились на рефрактометре ИРФ - 22. Предварительно построен калибровочный график и изучена кинетика адсорбции исследуемых сорбатов на бентоните. Установлено, что адсорбционное равновесие наступает через 20 часов. Поэтому равновесная концентрация растворов определялась по истечении этого времени.
Изотермы адсорбции снимали следующим образом: 1г измельченного адсорбента, предварительно дегидратированного в вышеуказанных условиях, заливали 10мл растворов сорбатов, н-гексана и трансформаторного масла в циклогексане различной концентрации. Пробы в закрытых склянках выдерживали при комнатной температуре (20-250С) при периодическом встряхивании, после чего определяли равновесную концентрацию.
Величину Гиббсовой адсорбции вычисляли по
общеизвестной формуле:
Cu - Cp
r = ------------ ∙ V где
m
Cu - исходная концентрация раствора, моль/л
m - навеска адсорбента, г
V - объем исследуемого раствора, взятый для исследования адсорбции.
Cp- равновесная концентрация, моль/л
Из построенных изотерм адсорбции было видно (рис. 1.2.) , что адсорбция изученных сорбатов в области низкой концентрации резко возрастает, а затем идет почти параллельно оси абсцисс и имеется у всех кривых один изгиб.
Причем все они адсорбируются положительно во
всем интервале концентрации, и изотермы адсорбции выражаются простыми
изотермами адсорбции типа изотерм Ленгмюра или Фрейндлиха.
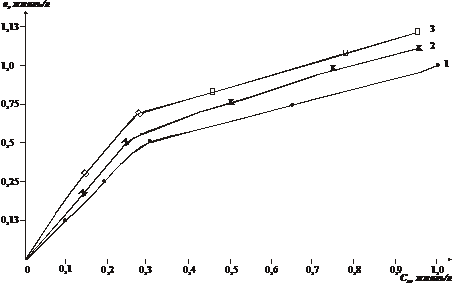
Рис.1.2. Изотермы адсорбции на Навбахорском бентоните.
- н-гексана на термоактивированном бентоните
- н-гексана на кислотнотермоактивированном бентоните
- трансформатоного масла на термоактивированном
бентоните
Причем, наибольшую активность имеет бентонит по трансформаторному маслу, чем по н-гексану. Это можно объяснить многокомпонентностью трансформаторного масла.
Если сравнить изотермы адсорбции н-гексана на исходном и кислотно-активированном образце бентонита, то последний имеет наибольшую емкость. По значениям емкости монослоя (am) они располагаются в следующий ряд: исходный бентонит (amмасла 0,6 ммоль/л) > кислотно-активированный бентонит (am н-гексана 0,5 ммоль/л) > исходный бентонит (am н-гексана 0,45 ммоль). Установлено что при адсорбции из
неполярной среды (циклогексан) у природных минеральных сорбентов участвует ½ часть поверхностных гидроксильных групп. Это обусловлено наличием у природных минеральных сорбентов активных центров типа центров кислотности Бренстеда у атома алюминия. Вода, адсорбированная на таких центрах значительно легче диссонирует таким образом усиливается адсорбционное взаимодействие между гидроксилом природных минеральных сорбентов и водородом атомов молекул углеводородов с образованием водородной связи.
Наиболее полное представление о природе адсорбционных сил, механизме адсорбции и о состоянии адсорбированного вещества дают термодинамические характеристики процесса адсорбции. Мономолекулярное взаимодействие в системе сорбат-сорбент может быть оценено и газоадсорбционным вариантом хроматографии. При этом допускается, что скорость массообмена между газовой и твердой фазой намного больше, чем скорость инертной фазы (газоносителя). Газохроматографическим методом измеряется избыточное время удерживания сорбата в колонке, заполненной сорбентом (в данном случае - бентонитом). Данный метод позволяет непосредственно определять избыточную величину адсорбции. Дифференциальная теплота находится из наклона прямолинейных отрезков изотер, выраженных в координатах LgP - T-1.
Проведено сравнение энергетических характеристик адсорбции - теплот адсорбции (Q, кДж/моль) гомологического ряда н-алканов и углеводородов различной электронной структуры состава С6 - н-гексана, бензола, циклогексана на исходном и кислотнотермоактивированном образцах бентонита (фракция 0,25-0,5 мм), определенных вышеуказанным методом.
Как известно, по классификации А.В.Киселева [3], н- алканы относятся к группе А, т.е. это молекулы со сферически симметричной электронной оболочкой, как у благородных газов.
Рабочие условия: Хроматограф ЛХМ-7А Дзержинского ОКБА (РФ), колонка стальная длиной 2м, диаметром 0,4мм, газ-носитель-гелий, температура колонок - 100,110 и 1200С. В качестве адсорбентов использовались исходный бентонит и его активированный образец. Как следует из [63], из всех известных методов улучшения адсорбционных свойств природных минеральных сорбентов является кислотно-термическая активация. Активирование производили 15% серной кислотой и подвергали температурной обработке при 160-1800С в течение 6 часов.
В таблице 1.1. приведены значения удельного удерживаемого объема (Vg см3/г), который является основной физико-химической константой в храмотографии. Видно, что Vg является функцией молекулярной массы сорбата: с ее повышением значение Vg увеличивается, а с повышением температуры Vg для каждого сорбата уменьшается, в связи с тем, что связь сорбат-сорбент ухудшается и увеличивается количество молекул, переходящих в газовую фазу.
Так, например при температуре колонки 473 К
н-гексана Vg составляет
48,34; н-гептана 95,31 и н-октана - 149,73; инкремент Vg
на одну метиленовую группу в гомологическому ряду 45 см3/г. Такая же картина
наблюдается и для других температур колонки.
Таблица 1.1.
Удельные удерживаемые объёмы н-алканов на Навбахорском бентоните
|
Сорбат |
Т, К пол. |
Vg, см3/г |
|
н-Гексан н-Гептан н-Октан н-Гексан н-Гептан н-Октан н-Гексан н-Гептан н-Октан |
473 493 513 |
48,34 ±0,84 95,31 ±0,42 149,73 ±0,20 40,40 ±1,02 70,64 ±0,58 105,47 ±0,32 33,38 ±1,33 57,80 ±0,64 79,80 ±0,54 |
Причем с повышением температуры колонки Vg
для каждого сорбата, как и следовало ожидать, уменьшается ввиду того, что
процесс десорбции превалирует над адсорбцией. Так, например для н-гексана Vg
при 473 К составляет 48,34 см3/г, 493 К - 40,40 см3/г, а при 513 К - 33,38
см3/г.
Таблица 1.2.
Теплоты адсорбции н-алканов С6-С8
|
Сорбат |
Т, К |
1/1000 К |
TR, мин |
Lg tR |
tgα |
Q, кДж/моль |
|
н-Гептан н-Гексан н-Октан н-Гексан н-Гептан н-Октан н-Гексан н-Гептан н-Октан |
473 493 513 |
2,114 2,028 1,949 |
2,01 2,505 4,05 1,385 2,175 3,34 1,255 2,04 3,175 |
0,27155 -0,661 0,574 -0,6819 0,2655 0,4472 -0,57245 -0,65155 0,4252 |
н-гексан 1,30 н-гептан 1,6 н-октан 1,84 |
н-гексан 33,00 н-гептан 34,42 н-октан 35,68 |
В таблице 1.2. представлены значения температур колонки, tR мин - время удерживания компонента, мин; тангенс угла наклона линейной зависимости lg времени удерживания от обратной величины температуры колонки и рассчитанные на их основе значения теплота адсорбции исследованных сорбатов (Q, кДж/моль). Видно, что Q н-алканов в ряду С6-С8 меняется от 35,65 до 35,68 кДж/моль; инкремент на метиленовую группу в гомологическом ряду н-алканов равен 1,3 кДж/моль. Составлена графическая зависимость Vg и Q от числа углеродных атомов в молекуле и температуры кипения, которые являются номограммами. По ним можно вычислить значения Vg и Q для гомологического ряда н-алканов.
На предложенном сорбенте снята хроматограмма смесей н-алканов С6-С8. Пики хроматограмм четкие, симметричные.
Определенные теплоты адсорбции углеводородов, состава С6- различной электронной структуры: бензола, циклогексана и н-гексана даны в таблице 1.3.
Сравнивая теплоты адсорбции углеводородов
различной электронной структуры - бензола, циклогексана и н-гексана, можно
сказать, что по значениям теплот адсорбции углеводороды располагаются, как на
исходном, так и обработанном бентоните в следующий ряд: н-гексан <
циклогексан < бензол.
Таблица 1.3.
Теплоты адсорбции углеводородов состава С6
|
Сорбаты |
Теплоты адсорбции (Q, кДж/моль) |
|
|
|
Q1 исх. |
Q2 обраб. |
|
Бензол |
26,00 ±0,46 |
13,61 ±0,14 |
|
н-гексан |
20,43 ±0,59 |
10,12 ±0,14 |
|
Циклогексан |
22,08 ±0,55 |
11,16 ±0,12 |
В обоих случаях, как на исходном, так и термоактивированном бентоните теплота адсорбции бензола выше, что можно объяснить наличием наряду с дисперсионным взаимодействием в системе сорбат - сорбент специфического взаимодействия за счет π - электронов ароматических углеводородов. Причем, сравнивая теплоты адсорбции бензола и н-гексана можно сказать, что теплота адсорбции π - электронов ароматического кольца составляет 0,57 кДж/моль.
Из приведенных данных видно, что теплоты адсорбции изученных сорбатов на обработанном бентоните ниже почти в два раза, чем на исходном, что можно объяснить концентрированием кристаллической фазы и уменьшением удельной поверхности бентонита, следовательно, и десорбция углеводородов будет происходить с меньшими затратами.
Следовательно, бентонит Навбахорского месторождения можно использовать в качестве сорбента для газоадсорбционной храмотографии.
Определялась емкость исходного и кислотнотермически обработанного бентонита по широкому кругу органических веществ, которые могут встречаться в масляных фракциях: углеводородам и гетероорганическим веществам, как S-, N-, и О-содержащие соединения - для первых шести сорбатов (н-гексану, бензолу, тиофену, пиридину, фенолу, циклогексанкарбоновой кислоте) криоскопическим методом ( разработка ИОНХ АН РУз [55] ) и двух последних (асфальтенам и смолам) - по обесцвечиванию их растворов при прохождении через слой сорбента [63]. Сущность криоскопического метода определения динамической емкости сорбентов заключается в изменении температуры кристаллизации модельных 2% растворов сорбатов при хроматографировании через 10г. сорбента (фр. 0,25-0,5мм, стеклянная колонка диаметром 1см, скорость фильтрации 1 капля в 1 сек.).
Так как изменение температуры кристаллизации раствора пропорционально его концентрации, то, пользуясь экспериментально найденными значениями температуры кристаллизации, построим «выходные кривые», (рис.1.3.) откладывая по оси абсцисс количество жидкости, прошедшей через слой адсорбента, а по оси ординат - температуру кристаллизации раствора.
При этом площадь фигуры АВЕД, отнесенная к 1кг
(или 100г) адсорбента, соответствует полной динамической емкости до проскока,
на основании которой рассчитывается рабочая активность адсорбента.