Материал: Совершенствование технологии получения адсорбентов из местных полиминеральных глин
Второе вещество, входящее в состав
аллофона, - кремнезем, встречающийся иногда в виде геля. Он состоит из
тетраэдрических групп ![]() ,
соединенных между собой в гексагональную сеть состава
,
соединенных между собой в гексагональную сеть состава ![]() . Расстояние
0-0 в тетраэдрическом слое равно 2,55
. Расстояние
0-0 в тетраэдрическом слое равно 2,55 ![]() ; пространство, доступное для иона,
в тетраэдрической координации имеет размер примерно 0,55
; пространство, доступное для иона,
в тетраэдрической координации имеет размер примерно 0,55![]() ; толщина
этого структурного элемента в структурах глинистых минералов равна 4,93
; толщина
этого структурного элемента в структурах глинистых минералов равна 4,93![]() . Каждый из
них имеет расстояние от центра до центра примерно 2,1
. Каждый из
них имеет расстояние от центра до центра примерно 2,1![]() [3, 11, 22].
[3, 11, 22].
Кристаллическая фаза глинистых минералов состоит из двух выше приведенных структурных элементов. Первый состоит из двух слоев плотно упакованных атомов кислорода или ОН - групп с атомами алюминия, железа и магния между ними в октаэдрической координации, второй - из кремнезекислородных тетраэдров.
Различные совокупности этих структурных элементов образуют отдельные разновидности глинистых минералов [3, 11, 22]. Например, двухслойный тип кристаллической решетки (1:1), состоящий из пакетов, которые содержат один слой кремнекислородных тетраэдров, характерен для глинистых минералов каолинитовой группы (каолинит, накрит, галлуазит и т.д.). к трехслойному типу решетки (2:1), который образован из двух слоев кремнекислородных тетраэдров и расположенного между ними одного слоя алюмокислородных октаэдров, относятся монтмориллонитовые (монтмориллонит, сиконит, вермекулит, нонтронит и др.) и иллитовые (иллит, слюда и т.п.) группы.
Наличие аморфных веществ обычно незначительно и не Вов всех глинах. Глинистые минералы в природе встречаются всегда с примесями; мономинеральные глины редки и все равно в той или иной степени содержат различные примеси [3, 4, 11, 23].
Химичекими, спектроскопическими, изотопными и другими методами выявлено, что на поверхности природных алюмосиликатов (следовательно, и на поверхности глинистых минералов, а также глин) имеются гидроксилы, связанные с атомами кремния и алюминия в соответствующих структурных единицах - кремнекислородных тетраэдрах и алюмокислородных октаэдрах (реже тетраэдрах). Поверхностные гидроксилы природных алюмосиликатов при их взаимодействии с молекулами сорбтива в ряде случаев проявляют протонодонорную функцию. Происходящую при этом частичную протонизацию водорода можно рассматривать как проявление кислотной природы гидроксильных групп [4, 23]. Поверхностные гидроксилы природных алюмосиликатов обладают слабокислотными свойствами и играют решающую роль при адсорбции веществ, способных и донороакцепторному взаимодействию [23], а также при каталитических процессах, протекающих по карбоноионному механизму [24].
На основании результатов работ, посвященных изучению химии поверхности [25-27] адсорбционно-каталитических свойств [28,29] силикагелей, силикатов, алюмосиликатов можно заключить, что водород группы ОН, принадлежащие атому кремния в тетраэдрической координации, обладает относительно слабым кислотным свойством, чем водород гидроксильной группы принадлежавшей атому алюминия, а октаэдрических (даже в тетраэдрических) координациях.
В настоящее время различают три вида поверхности у природных алюмосиликатов [30].
Поверхность первого рода - поверхность скола, представляющая собой край кристаллической решетки или частиц. Энергия этой поверхности определяется числом атомов с некомпенсированными электровалентными связями, и поэтому эта поверхность является наиболее активной. По мнению Э. А. Арипова [4, 31], этот вид поверхности является не только активным, но и ответственным за число свободных радикалов (или число парамагнитных центров) у глинистых минералов и глин. Поверхность второго рода - базальные поверхности внутри пакета; она находится в поле влияния плоскостей. Поверхность третьего рода - тоже базальная; она представляет внешнюю поверхность частиц (или кристаллов) и поэтому является свободной от влияния соседней поверхности, следовательно, по энергетическому состоянию отличается от поверхности второго рода.
Если рассматривать поверхности второго и третьего родов без учета изоморфных замещений атомов решетки, то эти поверхности должны в силу своего кристаллохимического строения являться электронейтральными. Однако, как отмечено в [3, 11, 22], в реальных глинистых минералах всегда имеет место изоморфное замещение кремния на алюминий в тетраэдрической координации и алюминия на магний, железо и др. в октаэдрической координации, при которых освобождаются отрицательные заряды по одному от каждого освобождаются.
Таким образом, активные адсорбционные центры у алюмосиликатов самые разнообразные. Однако, приписывать предпочтению одного из этих факторов процесс адсорбции или адсорбционного отбеливания нельзя. Но увеличить долю одного из этих факторов можно путем активирования и модифицирования глин. Например, увеличение степени дисперсности образца при активации способствует повышению величин его поверхности первого рода. Благодаря этому обеспечивается максимальный эффект при контактной очистке минеральных и растительных масел.
Активная кислотность выражается
величиной рН водной вытяжки образца или его водной суспензии. При внесении
образца в воду в нее переходят присутствующие в образце водорастворимые
минеральные и органические соли, газы (особенно ![]() ). Кроме того, имеет место
диссоциация соли алюмо-кремниевых кислот (определение Вернадского В. И. [34]).
). Кроме того, имеет место
диссоциация соли алюмо-кремниевых кислот (определение Вернадского В. И. [34]).
Обменная кислотность определяется
титрованием нейтральной солевой вытажки (![]() и др.), а гидролитическая
кислотность - титрованием вытяжки, полученной обработкой образца растворами
гидролитически щелочной соли (
и др.), а гидролитическая
кислотность - титрованием вытяжки, полученной обработкой образца растворами
гидролитически щелочной соли (![]() ),
), ![]() и др.).
и др.).
При вытеснении поглощенных катионов алюмосиликатами (почва, глина), катионом нейтральных солей в раствор переходит и некоторое количество алюминия, соли которого, гидролизуясь, дополнительно обусловливают кислотность. Этот вид кислотности принято называть обменно-алюминиевой формой кислотностей находят обменно-водородную форму кислотности образца.
Протонную (бренстедовскую) кислотность алюмосиликатов, глубоко гидролитическую, определяют отравлением гидролитически щелочной солью, но только с той разницей, что в этом случае находят не все подвижные и неподвижные водородные ионы, а по К. В. Топчиевой [33] - лишь подвижные.
Апротонную (льюисовскую) кислотность по методу В. Трамбуза [35] определяют титрованием неводной (обычно бензиновой) суспензии образца этилацетатом или диоксаном в присутствии индикатора парадиметиламино-азабензола (НДА). Беря в качестве титрующего агента Н-бутиламин в этих же условиях согласно Тамеле [36], определяется сумма протонной и апротонной кислотности алюмосиликатов.
Г.А.Бенези [37], измеряя силу поверхностной кислотности синтетических и природных алюмосиликатных катализаторов крекинга, показал, что на поверхности катализаторов имеются кислотные центры, общее количество которых составляет не больше семи процентов от общей поверхности образца.
С целью приближения к оценке числа активных центров в условиях катализа К.В.Топчиевой с сотрудниками [38] разработан импульсный хроматографический метод определения кислотных центров, основанный на дозировании органического основания-пиридина во время опыта, с образованием нона пиридина.
О причинах появления кислых свойств алюмосиликатов (почв, глин и др.) высказаны различные гипотезы. Первая из них объясняет кислотность наличием поглощенных ионов водорода на поверхности коллоидных частиц (например, кислые глины) алюмосиликатов. По этой гипотезе, кроме более прочной связи с частицей алюмосиликатов, ионы водорода ничем не отличаются от других поглощенных катионов образцами [32, 39].
По второй гипотезе, кислотность алюмосиликатов обусловлена адсорбированными солями алюминия, которые обмениваются на катионы нейтрального солевого раствора; образующаяся при этом в растворе соль гидролизуется и создает кислую реакцию равновесного солевого раствора [32, 39].
Следующая гипотеза основывается на наличии гидроксилов на поверхности частиц алюмосиликатов. Допускается, что водород этих гидроксилов обладает способностью обмениваться на катион других металлов и, таким образом, водороды ОН группы обусловливают обменную кислотность [28].
Число поверхностных гидроксилов
зависит от двух факторов - от наличия изоморфного замещения и степени
дисперсности образца. При этом: 1) Чило Он в алюмосиликатах увеличивается с
ростом степени изоморфного замещения ![]() на
на ![]() в тетраэдре и
в тетраэдре и ![]() на
на ![]() в октаэдре,
т.е. число гидроксилов пропорционально росту отрицательного заряда частиц
алюмосиликата, который повышается с увеличением степени замещения катионов с
большей валентностью на катионы с меньшей валентностью [3, 11, 22, 34, 40, 2].
Число гидроксилов на поверхности частиц тем больше, чем больше степень
дисперсности частиц образца; при диспергировании увеличивается число разрывов
связи
в октаэдре,
т.е. число гидроксилов пропорционально росту отрицательного заряда частиц
алюмосиликата, который повышается с увеличением степени замещения катионов с
большей валентностью на катионы с меньшей валентностью [3, 11, 22, 34, 40, 2].
Число гидроксилов на поверхности частиц тем больше, чем больше степень
дисперсности частиц образца; при диспергировании увеличивается число разрывов
связи ![]() и
и ![]() , куда могут
присоединяться наряду с другими молекулами и молекулы воды, водород которых
обладает в этом случае сильно протонизирующей способностью. Причем, этот протон
не входит в состав минерала и обладает высокой подвижностью [41].
, куда могут
присоединяться наряду с другими молекулами и молекулы воды, водород которых
обладает в этом случае сильно протонизирующей способностью. Причем, этот протон
не входит в состав минерала и обладает высокой подвижностью [41].
Многочисленными трудами отечественных и зарубежных ученых установлено, что природные алюмосиликаты обладают каталитическими свойствами по отношению к различным органическим веществам и что у глин разного состава эти свойства проявляются различно. Рассмотрению явления катализа и роли глинистых катализаторов в крекинге нефти посвящено много работ.
Главным в этих работах, по-видимому, является решение вопросов, связанных с каталитическими свойствами алюмосиликатов, с их структурной особенностью. Предполагают, что на поверхности частиц алюмосиликатов имеются активные каталитические (адсорбционные) центры. Так, активные центры согласно И. Легмюра [42], - это энергетически неоднородные участки на поверхности; Г. С. Тейлора [43] - это взаимнонекомпенсированные атомы, выступающие в виде пиков; А. Ф. Иоффе [44] - это молекулярные трещины и ямы, вызывающие понижение прочности и где работа диссоциации будет понижена в несколько раз (Я. Х. де-Бур [45] считает, что ямы являются активными центрами при ван-дер-ваальсовой адсорбции); Баландина А. [46] - это участки кристаллической решетки, способные с молекулами реагентов образовывать мультиплетный комплекс; Н. И. Кобозова [47] - это ансамбль атомов, которые на поверхности катализатора удерживаются благодаря адсорбционной силе.
Образование активных цкентров (мест) катализаторов А. В. Писаржевский [48] связывает с явлением электронной изоляции. Это послужило основанием для разработки электронно-химической теории явления катализа, а также процесса адсорбции на неоднородной поверхности сорбента [49, 50].
В. И. кузнецов [51] поверхность кристаллических и аморфных алюмосиликатных катализаторов рассматривает как непрерывно изменяющийся бертоллоид. В основе этого понятия лежит неоднородность поверхности, которую можно разделять на структурную неоднородность, вызванную различной активностью разных граней кристаллов, атомов или группы атомов на ребрах, вершинах граней, на ступенях дислокаций, и на неоднородность, обусловленную включениями посторонних веществ и образованием новой фазы.
В реакциях превращения углеводородов
самыми наилучшими катализаторами являются кислые катализаторы [52]. В связи с
этим заслуживают внимания данные А. В. Фроста, в которых указано на глубокие
сходства каталитических действий алюмосиликатов с каталитическими действиями
таких кислых катализаторов, как ![]() и
и ![]() [53].
[53].
В настоящее время в литературе
имеется ряд работ, в которых предпологается модель активного центра
алюмосиликатного катализатора. Одна из таких моделей, как апротонный кислотный
центр тип Льюиса для алюмосиликата, согласно Л. Литтлу [54], состоит из
кремнекислородного тетраэдра и алюмокислородного октаэдра. Рост кислотности
алюмосиликатов проявляется тем сильнее, чем больше степень замещения атома
кремнияв кремнекислородной структурной единице атомом алюминия. Допускается,
что ион алюминии в этой структуре стремится присоединением пары электронов
заполнить р-подуровень. При этом в отсуствии воды образуются кислоты типа
Льюиса, а в ее присутствии - кислоты типа бренстеда по схеме:
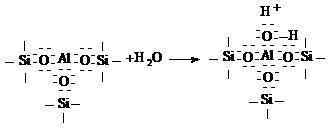
Или
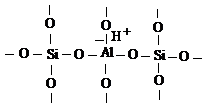
Этот протон, как указывает О. В. Крылов [41], не входит в состав ОН -группы и обладает высокой подвижностью. Наличие протона М. М. Мортленд и др. [55] объясняют высокой степенью диссоциации воды, адсорбированной на центре Льюиса. Причем, воды диссоциируясь, образует кислоту с подвижным водородом.
Согласно М. Р. Базила и др. [57], все первичные кислые места на алюмосиликатах представляют собой центры Льюиса, локализованные на поверхностных атомах алюминия. Бренстедовская кислотность образуется взаимодействием молекул углеводорода, хемосорбированных на льюисовских центрах и на соседних поверхностных гидроксильных группах.
Подвижный протон может возникать не
только в четверто координации алюминия, но и в результате электронного смещения
от поверхности силанальной группы к алюминию [58].
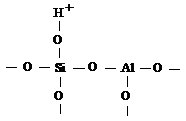
Согласно модели активного центра
алюмосиликата, предложенной А. П. Боллод и К. В. Топчиевой [59], кислотность
связана так с замещением кремния в кремнекислородных тетраэдрах на алюминий с
образованием комплекса ![]() , где
трехвалентный алюминий неспособен полностью насытить все четыре атома
кислорода, в результате чего алюмосиликат проявляет сильные кислотные свойства
по схеме:
, где
трехвалентный алюминий неспособен полностью насытить все четыре атома
кислорода, в результате чего алюмосиликат проявляет сильные кислотные свойства
по схеме:
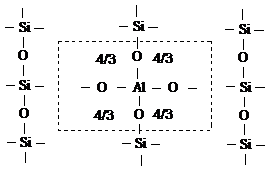
В работе [10] З.Г. Зульфугаровым
предложена модель для активированного килотой монтмориллонита с учетом активных
центров как для гидролитический, так и для обменной формы кислотности по
следующей схеме:
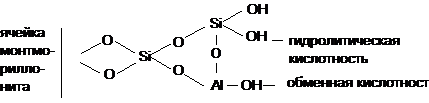
Эта модель рассматривает обменную и гидролитическую кислотности, отравление ионами щелочных металлов, а также механизм дегидратации кислого монтмориллонита. Ответственность за отбеливание и катализ приписывается атому водорода, находящемуся в обменном положении.
Согласно модели А. В. Киселева и В.
И. Лыгина [60], возбужденный протон появляется за счет возникновения парных
кислотных центров апротонного и протонного типа по схеме:
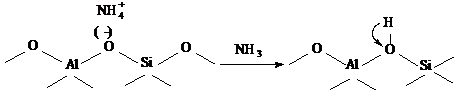
Природа активных центров
алюмосиликатов, согласно М. А. Калико [61], следующая: генерация протона может
осуществиться за счет адсорбированной воды при температурах крекинга:
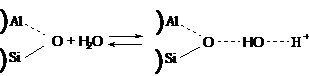
а за счет перестройки гидроксилов -
в хемосорбированную воду:

допускается, что из-за химически
ненасыщенной связи между ![]() и
и ![]() образуется
молкулярный комплекс (например, при разложении кумола), т.е. изопропилобензол
состоящий из адсорбированных молекул воды и молекулы углеводорода, по следующей
схеме:
образуется
молкулярный комплекс (например, при разложении кумола), т.е. изопропилобензол
состоящий из адсорбированных молекул воды и молекулы углеводорода, по следующей
схеме: