Материал: Практикум по общей химии
Вспомогательный раствор: аммиачно-буферный (рН = 9,5-10). Индикатор: хромоген черный.
Способ титрования: прямой.
Для установления точки эквивалентности используется индикатор хромоген черный, который в зависимости от рН раствора ионизирует по-разному:
H3V |
↔ H2V- + H+ |
↔ HV2- + 2H+ |
↔ V3- + 3H+ |
рН<6 |
pH=6 |
pH=7-11 |
pH=11,5 |
|
винно-красный |
синий |
оранжевый |
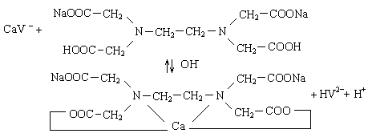
При рН = 9,5-10 комплекс Са2+ с индикатором имеет виннокрасную окраску:
Са2+ + HV2- |
→ СаV- + H+ |
синий |
винно-красный |
При титровании трилоном Б в точке эквивалентности наблюдается полный переход металла из непрочного комплекса
с индикатором |
в более |
прочный |
комплекс |
с |
трилоном |
Б |
|||
(бесцветным), и винно-красная окраска меняется на синюю: |
|
||||||||
- |
+ |
Na2H2I |
ОН |
|
Na2СаI |
+ |
2- |
+ H |
+ |
СаV |
|
HV |
|
||||||
винно-красн. |
б/цветн. |
|
|
б/цветн. |
|
синяя |
|
||
или:
В коническую колбу с помощью пипетки отмерьте 10 мл слюны. Добавьте 5 мл буферного раствора мерной пробиркой и несколько кристалликов индикатора. Исследуемый раствор приобретает винно-красную окраску. Титруйте из бюретки трилоном Б до перехода винно-красной окраски в синюю. Показания бюретки отметьте с точностью до 0,1 мл. Титрование повторите до получения трех результатов, отличающихся не более чем на 0,1±0,2 мл. Результаты титрования занесите в табл.
18.
61
Таблица 18
|
мл |
|
№ опыта |
иссл.р-ра, |
Vтр., мл |
|
V |
|
110,0
210,0
310,0
|
|
i |
|
|
V |
|
V |
,мл |
|
n |
||||
|
|
|||
|
(V V ) |
|
|
V |
i |
, |
|
n |
|||
|
|
||
МЛ |
|
|
Относит. ошибка
V |
100% |
|
V |
||
|
Содержание Са2+, мг/100мл
По |
V тр. рассчитайте содержание ионов Са2+ в слюне, в |
мг/100 мл, сравните с нормой, сделайте вывод.
КОНТРОЛЬНЫЕ ВОПРОСЫ:
1.Почему определение ионов Са2+ необходимо проводить в щелочной среде?
2.Как рассчитывается эквивалент определяемого элемента в методе трилонометрии?
3.Рассчитайте содержание ионов Са2+ в слюне в г/л по результатам титрования.
4.Возможно ли применение данного метода для анализа магния, железа, других биогенных элементов в биологических жидкостях?
5.Возможны ли другие аспекты применения комплексонов в биологии и в медицине, кроме аналитических целей?
ЛИТЕРАТУРА:
1. С. 250-252; 2. С. 226; 4. С. 151-155; 6. С. 263-265.
62
РАБОТА 16. МЕТОД ОКСИДИМЕТРИИ. ОПРЕДЕЛЕНИЕ ОКИСЛЯЕМОСТИ ВОДЫ МЕТОДОМ ПЕРМАНГАНАТОМЕТРИИ
(для медико-профилактического факультета)
Окисляемость воды – условный показатель, характеризующий содержание в ней восстановителей. Окисляемость воды выражается числом мг перманганата калия, израсходованного на окисление восстановителей в 1 л воды. В норме окисляемость воды составляет до 25 мг/л.
ЦЕЛЬ ЗАНЯТИЯ:
1.Ознакомиться с возможностями метода перманганатометрии.
2.Научиться записывать уравнения окислительно-восстанови- тельных реакций с участием перманганата калия.
3.Ознакомиться с условиями проведения анализа.
4.Освоить методику перманганатометрического титрования.
5.Научиться на основании результатов титрования производить количественные расчеты.
ЗАДАНИЕ:
Выполните обратное титрование восстановителей методом перманганатометрии и рассчитайте окисляемость воды в мг KMnO4 на 1 л воды. Представьте отчет по работе.
МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ВЫПОЛНЕНИЮ РАБОТЫ:
Перманганат калия реагирует с восстановителями,
находящимися в воде, по реакции:
MnO4- + 8H+ + 5e → Mn2+ + 4H2O (1)
Избыток внесенного KMnO4 устраняется оксалат-ионом:
2MnO4- + 5С2О42- + 16H+ → 2Mn2+ + 10СО2 + 8H2O(2)
Не вступившие в реакцию оксалат-ионы оттитровываются перманганатом калия по уравнению (2). Определение точки эквивалентности (конца титрования) – по слабо-розовой окраске раствора в колбе от одной сверхэквивалентной капли перманганата калия.
Рабочий раствор: KMnO4, Сэ = 0,05 моль экв/л. Исследуемый раствор: водопроводная вода.
63
Вспомогательные растворы: титрованный раствор оксалата натрия Сэ = 0,05 моль экв/л и серная кислота.
Способ титрования: титрование по остатку (обратное титрование).
Порядок титрования: в коническую колбу для титрования налейте мерным цилиндром 50 мл водопроводной воды. Прилейте мерной пробиркой 5 мл разбавленной серной кислоты и из бюретки точно 5 мл раствора KMnO4. Смесь взболтайте в течение 8-10 мин. При этом часть KMnO4 расходуется на реакцию с восстановителями, находящимися в воде. К приготовленной смеси прилейте пипеткой 5 мл раствора щавелевой кислоты или оксалата натрия, перемешайте кругообразным взбалтыванием и нагрейте до 80оС. Горячий раствор титруйте при тщательном перемешивании раствором KMnO4 до появления слабо-розовой окраски. Титрование повторите 4-5 раз до получения сравнимых результатов. Результаты занесите в таблицу 19.
Таблица 19
№ опыта |
VH2O, мл |
VNa2C2O4, мл |
VH2SO4, мл |
VKMnO4, мл |
1 |
50 |
5,0 |
5,0 |
|
2 |
50 |
5,0 |
5,0 |
|
3 |
50 |
5,0 |
5,0 |
|
|
V |
|
||
V |
|
|
i |
, |
n |
|
|||
|
|
|
||
KMnO |
4 |
, мл |
||
|
|
|
|
|
|
(V V ) |
|
|
V |
i |
, |
|
n |
|||
|
|
||
МЛ |
|
|
Относи т.
ошибка
V |
100% |
|
V |
||
|
Окисляемость, мг KMnO4/л Н2О
Рассчитайте окисляемость воды, мг KMnO4/л Н2О, сделайте вывод.
КОНТРОЛЬНЫЕ ВОПРОСЫ:
1.Назовите условия титрования по методу перманганатометрии.
2.Почему для создания кислой среды используется серная кислота?
64
3.Объясните, почему для количественного определения восстановителей в воде используется метод обратного титрования?
4.Запишите состояние эквивалентности в случае обратного титрования.
5.Приведите пример анализа восстановителя по методу перманганатометрии.
6.Приведите пример анализа восстановителя по методу перманганатометрии способом прямого титрования.
ЛИТЕРАТУРА:
1. С. 227; 4. С. 135-142.
65