Материал: Практикум по общей химии
РАБОТА 19. МЕТОД ЙОДОМЕТРИИ. ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ СВОБОДНОГО ХЛОРА В ВОДЕ (для медико-профилактического факультета)
Метод йодометрии дает возможность определять как окислители, так и восстановители благодаря промежуточному
значению нормального потенциала (
E |
o |
|
|
|
I |
2 |
/ 2I |
|
|
|
|
|||
0,54 В). В санитарии
используют метод йодометрии для определения чистоты питьевой воды (бром, остаточный хлор), анализе хлорной извести, используемой для дезинфекции, анализе сельскохозяйственных ядов (определение Cu2+ в хлорокиси меди).
ЦЕЛЬ ЗАНЯТИЯ:
1.Ознакомиться с возможностями метода йодометрии, научиться писать уравнения реакций.
2.Научиться выбирать метод и условия титрования, рабочий раствор при определении окислителей и восстановителей.
3.Научиться решать задачи на определение содержания веществ в растворе.
ЗАДАНИЕ:
Выполните йодометрическое определение содержания свободного хлора в воде. Напишите отчет по лабораторной работе.
МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ВЫПОЛНЕНИЮ РАБОТЫ:
Определение свободного хлора в воде основано на вытеснении йода из йодидов по реакции:
Cl2 + 2KI = I2 + 2KCl
Выделившийся йод может быть оттитрован раствором Na2S2O3: 2 Na2S2O3 + I2 = 2NaI + Na2S4O6
Исследуемый раствор: водопроводная вода.
Рабочий раствор: тиосульфат натрия Na2S2O3, Сэ = 0,05 моль экв/л.
Вспомогательный раствор: 10 % раствор KI. Индикатор: раствор крахмала.
Способ титрования: по замещению.
71
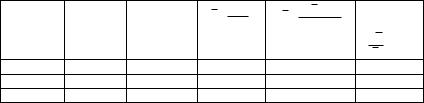
В коническую колбу пипеткой отмерьте 20 мл анализируемой водопроводной воды, добавьте 10-15 мл 10 % раствора KI, и титруйте выделившийся йод рабочим раствором тиосульфата натрия до соломенно-желтой окраски. Добавьте несколько капель крахмала и синий раствор дотитруйте до обесцвечивания. Титрование проводите 3 раза. Результаты должны отличаться между собой не более чем на 0,1-0,2 мл. Занесите их в табл. 22.
Таблица 22
№V воды,
опыта мл
120,0
220,0
320,0
V |
S |
O |
, |
Na |
3 |
||
2 |
2 |
|
|
мл |
|
|
|
|
V |
|
|
V |
i |
, |
|
n |
|||
|
|
||
мл |
|
|
|
(V V ) |
|
|
V |
i |
, |
|
n |
|||
|
|
||
МЛ |
|
|
Относит. ошибка
V |
100% |
|
V |
||
|
По
V |
S |
O |
|
Na |
3 |
||
2 |
2 |
|
определите содержание С12 в воде в г/л.
КОНТРОЛЬНЫЕ ВОПРОСЫ:
1.Объясните, почему невозможно прямое определение С12 йодометрическим методом, если ЕоС12/2С1- = 1,36 В, ЕоI2/2I- =
0,54 В.
2.Почему при определении окислителей йодида калия берут в несколько раз больше, чем требуется по уравнению?
3.Запишите закон эквивалентов в случае титрования по замещению.
4.Назовите условия титрования при определении окислителей (температура, рН, количество вспомогательного раствора), дайте объяснения.
5.Когда добавляют индикатор при йодометрическом определении окислителей и почему?
ЛИТЕРАТУРА:
1. С. 138-139.
72
РАБОТА 20. ФОТОКОЛОРИМЕТРИЯ. ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ Fe (III)
В МИНЕРАЛИЗОВАННОЙ ПЛАЗМЕ КРОВИ (для лечебно-профилактического и педиатрического факультетов)
Железо по его биологической роли относится к биометаллам, а по количественному содержанию (до 5 мг в организме взрослого человека) – к микроэлементам. Содержится железо в составе гемоглобина (70%), в составе миоглобина (5-10 %), остальное – в составе Fe-содержащих белков (ферритина, трансферрина). Недостаток железа в организме приводит к анемии, избыток (сидероз) может привести к нарушению деятельности сердечнососудистой системы, печени, легких.
В плазме крови содержание железа в норме составляет 105 мкг% или 1050 мкг/л.
ЦЕЛЬ ЗАНЯТИЯ:
1.Ознакомиться с возможностями фотоколориметрического анализа.
2.Научиться работать на ФЭК.
3.Освоить методику приготовления проб на анализ.
4.Научиться пользоваться калибровочным графиком.
5.Научиться оценивать содержание железа (Ш) в исследуемом растворе.
ЗАДАНИЕ:
Выполните фотоколориметрическое определение содержания ионов Fe3+ в плазме крови, мкг/л, сравните с нормой, сделав вывод. Представьте отчет.
МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ВЫПОЛНЕНИЮ РАБОТЫ:
В основе фотометрического определения содержания ионов Fe3+ в плазме лежит образование прочных окрашенных комплексов:
Fe3+ + nSCN- ↔ [Fe(SCN)n]3-n
Оптическую плотность раствора, содержащего указанные комплексные ионы, определяют на ФЭК при λ = 500 нм (синезеленый светофильтр), т.к. оптическая плотность при этом максимальна.
73
В мерную колбу на 50 мл внесите пипеткой 5 мл плазмы № , прибавьте 2,5 мл раствора НС1 и перемешайте. Затем прибавьте 5 мл раствора NH4SCN и доведите объем раствора до метки водой. После перемешивания налейте раствор в кювету и измерьте оптическую плотность на ФЭК. Введите поправку на оптическую плотность «холостой» пробы. «Холостая» проба готовится аналогично, но она не содержит плазму.
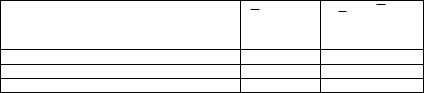
Из Dоп. вычтите Dхол. и по калибровочному графику определите содержание железа (Ш) в пробе. Определение повторите три раза. Результаты занесите в табл. 23.
По среднему значению массы железа в пробе рассчитайте содержание железа в 1 л исследуемой плазмы, мкг/л. Сравните с нормой. Оцените относительную ошибку определения.
Таблица 23
№ |
|
|
|
mFe3+, |
|
Dоп. |
Dхол. |
Dиссл. |
мкг в |
||
опыта |
|||||
|
|
|
пробе |
||
|
|
|
|
||
1 |
|
|
|
|
|
2 |
|
|
|
|
|
3 |
|
|
|
|
m |
mi |
, |
|
n |
|||
|
|
мкг в пробе
m |
(m mi ) |
, |
|
n |
|||
|
|
мкг
КОНТРОЛЬНЫЕ ВОПРОСЫ:
1.Предложите окислитель, который можно использовать при подготовке плазмы на анализ для перевода железа (П) в железо (Ш).
2.Как повлияет увеличение концентрации ионов SCN- на смещение равновесного процесса образования комплексного иона?
3.Дайте название комплексному иону.
ЛИТЕРАТУРА:
1. С. 279-281; 6. С. 349-351.
74
РАБОТА 21. ФОТОКОЛОРИМЕТРИЯ. ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ Fe (III)
В ПИТЬЕВОЙ ВОДЕ (для медикопрофилактического факультета)
Питьевая вода должна быть безопасна в эпидемическом отношении, безвредна по химическому составу и иметь благоприятные органолептические свойства. Концентрация химических веществ, влияющих на органолептические свойства, встречающихся в природных водах или добавляемых к воде в процессе ее обработки, не должна превышать нормативов. ГОСТ на воду питьевую допускает содержание железа не более 0,3 мг/л.
ЦЕЛЬ ЗАНЯТИЯ:
1.Ознакомиться с возможностями фотоколориметрического анализа.
2.Научиться работать на ФЭК.
3.Освоить методику приготовления проб на анализ.
4.Научиться пользоваться калибровочным графиком.
5.Научиться оценивать содержание железа (Ш) в исследуемом растворе.
ЗАДАНИЕ:
Выполните фотоколориметрическое определение содержания ионов Fe3+ в питьевой воде, мг/л, сравните с предельно допустимой концентрацией (ПДК), сделайте вывод. Представьте отчет по работе.
МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ВЫПОЛНЕНИЮ РАБОТЫ:
В основе фотометрического определения содержания ионов Fe3+
в плазме лежит образование прочных окрашенных комплексов:
Fe3+ + nSCN- ↔ [Fe(SCN)n]3-n
Оптическую плотность раствора, содержащего указанные комплексные ионы, определяют на ФЭК при λ = 500 нм (синезеленый светофильтр), т.к. оптическая плотность при этом максимальна.
В мерную колбу на 50 мл внесите пипеткой 5 мл воды, прибавьте 2,5 мл раствора НС1 и перемешайте. Затем прибавьте 5 мл
75