Материал: Практикум по общей химии
ПРЕДИСЛОВИЕ
Практикум содержит информацию о подготовке и проведении лабораторно-практических занятий по 10 темам.
К каждому занятию предпослано краткое обоснование изучения данной темы для формирования будущего специалиста-медика; указывается цель занятия, где дается представление о том, какие знания и умения должен приобрести студент на занятии. Контрольные вопросы ориентируют студента в самостоятельной работе с литературой, помогают лучше усвоить материал.
При подготовке к занятию рекомендуется пользоваться следующей литературой:
1.Ю.А.Ершов, В.А.Попков, А.С.Берлянд. Общая химия. М.: Высшая школа, 1993.
2. А.С.Ленский. Введение в бионеорганическую |
и |
биофизическую химию. М.: Высшая школа, 1989. |
|
3.М.И.Равич-Щербо, В.В.Новиков. Физическая и коллоидная химия. М.: Высшая школа, 1980.
4.А.В.Бабков и др. Практикум по общей химии с элементами количественного анализа. М.: Высшая школа, 1978.
5.А.И.Орехова, Р.П.Лелекова. Задачи и упражнения по общей и
бионеорганической химии. Под ред. А.И.Ореховой. Екатеринбург: УГМА, 2007.
6.В.И.Слесарев. Химия. Основы химии живого. С.-Пб.: Химиздат, 2000.
Письменное задание к занятию включает в себя вопросы и задачи для проверки усвоения материала, в то же время обязательное выполнение домашнего задания – это одна из форм самостоятельной работы студентов.
Лабораторная работа представлена описанием опытов и методическим указанием к их проведению. Лабораторная работа выполняется каждым студентом индивидуально. Для более глубокого осмысления лабораторной работы и экономии времени на занятии необходимо в процессе подготовки к занятию прочитать описание опытов, заготовить таблицы.
6
РАБОТА 1. ОПРЕДЕЛЕНИЕ ЭКВИВАЛЕНТА МЕТАЛЛА
Закон эквивалентов является одним из основных законов химии; используется при приготовлении реактивов и количественном определении веществ титриметрическим методом.
Закон эквивалентов имеет большое значение при анализе чистоты лекарственных препаратов, анализе питьевых и сточных вод, различных биологических жидкостей, при диагностике и контроле за ходом лечения ряда заболеваний.
ЦЕЛЬ ЗАНЯТИЯ:
Усвоить понятие эквивалента, ознакомиться с практическим расчетом эквивалента металла на основании экспериментальных данных по выделению им водорода из раствора кислоты.
ЗАДАНИЕ:
Проведите экспериментальное определение эквивалента металла по выделению им водорода из раствора кислоты. По величине эквивалента и его степени окисления назовите металл. Составьте отчет.
МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ВЫПОЛНЕНИЮ РАБОТЫ:
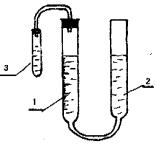
1.Соберите установку (рис. 1).
2.Получите у преподавателя навеску металла в папиросной бумаге, смочите ее водой и приклейте к внутренней стенке пробирки над кислотой, плотно присоедините пробирку к
прибору.
3. Проверьте герметичность прибора. Для этого опустите уравнительный сосуд так, чтобы уровень воды в нем был ниже уровня в бюретке, и закрепите его в штативе. Если через 1-3 мин понижения уровня воды в бюретке не произойдет, прибор герметичен.
Рис. 1
1)бюретка с водой;
2)уравнительный сосуд с водой;
7
3) пробирка с кислотой (5 мл H2SO4 Cэ=3 моль экв/л)
8
4.Установите уравнительный сосуд так, чтобы уровни в нем и бюретке были одинаковы, показания бюретки запишите. Встряхните пробирку так, чтобы металл попал в кислоту. Начинается выделение водорода, уровень воды в бюретке понижается. Дайте выдержку 10-15 мин, чтобы газ принял температуру окружающей среды.
5.Приведите к одному уровню воду в бюретке и уравнительном сосуде. Если он не изменяется, запишите новое показание бюретки. Данные для расчета запишите по форме (табл. 1)
m - масса металла, г,
V1 - показание бюретки до реакции, мл, V2 - показание бюретки после реакции, мл,
(V1-V2) - объем выделившегося водорода, мл,
Т
Р
РН
РН2
-температура опыта, К,
-атмосферное давление, мл рт ст.,
О- давление насыщенного пара воды возьмите из [5],
Р РН О – парциальное давление водорода.2 2
Объем выделившегося водорода при нормальных условиях рассчитайте по уравнению Менделеева-Клапейрона:
Р |
|
V |
|
P V |
; |
V |
|
P V T |
|
о |
o |
|
o |
||||
|
|
|
|
|
|
|||
|
T |
|
T |
|
o |
|
T P |
|
|
|
|
|
|
||||
|
|
o |
|
|
|
|
|
o |
Эквивалент металла рассчитайте по закону эквивалентов, зная
V0:
m |
|
|
V |
|
|
|
|
m |
Me |
V |
|
|
|
|
; |
Э |
|
|
|
Э |
|
||||
|
Me |
|
o |
|
|
|
|
H2 |
||||
|
|
|
|
|
|
|
|
|
|
|||
Э |
|
|
V |
|
|
|
Ме |
|
|
V |
|
|
Ме |
|
|
|
|
|
|
|
|
||||
|
|
Э |
H |
|
|
|
|
|
|
o |
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
6.Запишите уравнение реакции взаимодействия металла с кислотой. Назовите металл, зная величину его эквивалента и степень окисления, равную 2.
7.Сравните полученное и теоретическое значения эквивалента металла, рассчитайте относительную ошибку по формуле:
% Этеор. Ээксп. 100
Этеор.
9
КОНТРОЛЬНЫЕ ВОПРОСЫ:
1.Как рассчитать эквивалент элемента, зная его атомную массу, степень окисления?
2.Рассчитайте ЭAl в Al2О3; ЭCr в Cr2(SO4)3.
3.При действии НСl на 6 г металла выделится 5,6 л водорода
(н.у.). Определите молярную массу атома металла, если степень окисления его равна 2.
4.На сжигание 1 г металла требуется 560 мл кислорода. Найдите эквивалент металла.
5.Соединение кремния с кислородом содержит 47% кремния. Вычислите эквивалент кремния и степень его окисления.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Таблица 1 |
||
|
|
|
|
|
ФОРМА ОТЧЕТА |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
Название работы |
|
|
|
|
|
|
|
||||
металлаМасса, г |
|
Показания бюретки, мл |
ОбъемН2, мл |
,ТК |
Давление, |
|
|
ОбъемН2 |
.),у.н( мл |
|
ЭМе, |
Относительная ошибка, % |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
мм рт ст. |
|
|
|
|
г/моль |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
до реакции |
|
после реакции |
|
|
|
атмосферное |
нас. пара воды |
Н2 |
|
|
|
эксперимент. |
|
теоретич. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
2 |
|
3 |
4 |
5 |
|
6 |
7 |
8 |
|
9 |
|
10 |
|
11 |
12 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Уравнение химической реакции: Формулы для расчетов:
ЛИТЕРАТУРА:
4. С. 27-32.
10