Материал: Практикум по общей химии
Таблица 16
|
мл |
|
№ опыта |
иссл.р-ра, |
Vтр., мл |
|
V |
|
120,0
220,0
320,0
|
|
i |
|
|
V |
|
V |
,мл |
|
n |
||||
|
|
|||
|
(V V ) |
|
|
V |
i |
, |
|
n |
|||
|
|
||
МЛ |
|
|
Относит. ошибка
V |
100% |
|
V |
||
|
Жесткость воды, ммоль экв/л
КОНТРОЛЬНЫЕ ВОПРОСЫ:
1.Почему определение ионов Mg2+, Са2+ необходимо проводить в щелочной среде?
2.Как рассчитывается эквивалент определяемого элемента в методе трилонометрии?
3.Возможны ли другие аспекты применения комплексонов в биологии и в медицине, кроме аналитических целей?
4.Какие вам известны методы уменьшения жесткости воды?
ЛИТЕРАТУРА:
1. С. 250-252; 2. С. 226; 4. С. 151-155; 6. С. 263-265.
56
РАБОТА 14. МЕТОД КОМПЛЕКСОНОМЕТРИИ. ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ КАЛЬЦИЯ
В ПЛАЗМЕ КРОВИ (для лечебно-профилактического и
педиатрического факультетов)
Химический состав крови довольно стабилен, несмотря на то, что в кровь постоянно поступают и выводятся различные по составу и действию вещества. Любые сдвиги состава крови характеризуют определенные патологические изменения в организме. Вот почему исследования крови представляют особую важность для клиники и помогают врачу правильно поставить диагноз.
Биологическая функция кальция заключается в регулировании ферментных систем и, в частности, процессов свертывания крови. Содержание ионов кальция в крови 9,8 мг % или 98 мг/л.
ЦЕЛЬ ЗАНЯТИЯ:
1.Ознакомиться с возможностями метода трилонометрии.
2.Научиться записывать реакции образования внутрикомплексных соединений.
3.Ознакомиться с условиями проведения анализа, выбором индикатора.
4.Освоить методику титрования.
5.Овладеть методикой трилонометрического определения содержания ионов кальция в плазме крови.
6.Научиться на основании результатов титрования рассчитывать содержание ионов кальция (Са2+) в плазме.
ЗАДАНИЕ:
Выполните трилонометрическое определение и рассчитайте содержание ионов кальция в плазме крови в мг % и в мг/л. Представьте отчет по работе.
МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ВЫПОЛНЕНИЮ РАБОТЫ:
Рабочий раствор: трилон Б, Сэ = 0,01 моль экв/л. Исследуемый раствор: плазма крови.
Вспомогательный раствор: аммиачно-буферный (рН = 9,5-10). Индикатор: хромоген черный.
57
Способ титрования: прямой.
Для установления точки эквивалентности используется индикатор хромоген черный, который в зависимости от рН раствора ионизирует по-разному:
H3V |
↔ H2V- + H+ |
↔ HV2- + 2H+ |
↔ V3- + 3H+ |
рН<6 |
pH=6 |
pH=7-11 |
pH=11,5 |
|
винно-красный |
синий |
оранжевый |
При рН = 9,5-10 комплекс Са2+ с индикатором имеет виннокрасную окраску:
Са2+ + HV2- |
→ СаV- + H+ |
синий |
винно-красный |
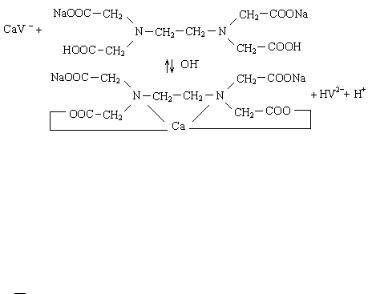
При титровании трилоном Б в точке эквивалентности наблюдается полный переход металла из непрочного комплекса
с индикатором |
в более |
прочный |
комплекс |
с |
трилоном |
Б |
|||
(бесцветным), и винно-красная окраска меняется на синюю: |
|
||||||||
- |
+ |
Na2H2I |
ОН |
|
Na2СаI |
+ |
2- |
+ H |
+ |
СаV |
|
HV |
|
||||||
винно-красн. |
б/цветн. |
|
|
б/цветн. |
|
синяя |
|
||
или:
В коническую колбу с помощью пипетки отмерьте 10 мл плазмы крови. Добавьте 5 мл буферного раствора мерной пробиркой и несколько кристалликов индикатора. Исследуемый раствор приобретает винно-красную окраску. Титруйте из бюретки трилоном Б до перехода винно-красного окрашивания в синее. Показания бюретки отметьте с точностью до 0,1 мл. Титрование повторите до получения трех результатов, отличающихся не более чем на 0,1±0,2 мл. Результаты титрования занесите в табл.
17.
По V тр. рассчитайте содержание ионов Са2+ в плазме, в мг % и мг/л, сравните с нормой, сделайте вывод.
58
Таблица 17
|
мл |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
опыта№ |
ра-р.иссл, |
мл,V.тр |
|
|
|
|
|
|
|
|
|
|
Относит. |
||||||
|
V |
|
|
|
|
(V Vi ) |
|
|
ошибка |
||||||||||
|
|
|
|
|
V |
, |
|
||||||||||||
|
|
|
V |
i |
,мл |
|
n |
|
|
|
|
|
|
|
|||||
|
|
|
n |
|
|
|
|
|
|
V |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
МЛ |
|
|
|
|
|
100% |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
V |
|||||
|
V |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
110,0
210,0
310,0
КОНТРОЛЬНЫЕ ВОПРОСЫ:
Содержание Са2+, мг/л
1.Почему определение ионов Са2+ необходимо проводить в щелочной среде?
2.Возможно ли применение метода трилонометрии для анализа магния, железа, других биогенных элементов в живых организмах?
3.Как рассчитывается эквивалент определяемого элемента в методе трилонометрии?
4.Рассчитайте содержание ионов Са2+ в исследуемой плазме в моль ион/л по результатам титрования.
5.Возможны ли другие аспекты применения комплексонов в биологии и в медицине, кроме аналитических целей?
ЛИТЕРАТУРА:
1. С. 250-252; 2. С. 226; 4. С. 151-155; 6. С. 263-265.
59
РАБОТА 15. МЕТОД КОМПЛЕКСОНОМЕТРИИ. ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ КАЛЬЦИЯ
В СЛЮНЕ (для стоматологического факультета)
Метод трилонометрии находит широкое применение в стоматологической практике. Стоматологи используют его для определения содержания кальция в биоптатах зубной эмали. По соотношению кальция и фосфора в биоптатах судят о резистентности эмали (устойчивости против кариозного разрушения) и ряде других заболеваний.
Слюна может обладать деминерализующей активностью. Состав ее может нарушить равновесие процессов де- и минерализации эмали и быть одним из пусковых механизмов возникновения кариеса зубов.
В норме содержание ионов Са2+ в слюне колеблется в пределах 5,2-9,7 мг/100 мл. При кариесе отклонений нет. При беременности и после родов наблюдается снижение содержания кальция в слюне.
ЦЕЛЬ ЗАНЯТИЯ:
1.Ознакомиться с возможностями метода трилонометрии.
2.Научиться записывать реакции образования внутрикомплексных соединений.
3.Ознакомиться с условиями проведения анализа, выбором индикатора.
4.Освоить методику титрования.
5.Овладеть методикой трилонометрического определения содержания ионов кальция в слюне.
6.Научиться на основании результатов титрования рассчитывать содержание ионов кальция (Са2+) в слюне.
ЗАДАНИЕ:
Выполните трилонометрическое определение и рассчитайте содержание ионов кальция в слюне в мг/100мл. Представьте отчет по работе.
МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ВЫПОЛНЕНИЮ РАБОТЫ:
Рабочий раствор: трилон Б, Сэ = 0,01 моль экв/л. Исследуемый раствор: слюна.
60