Материал: Практикум по общей химии
РАБОТА 11. СТРУКТУРООБРАЗОВАНИЕ. ИЗОЭЛЕКТРИЧЕСКАЯ ТОЧКА БЕЛКОВ
Ворганизме человека и животных многие жидкости и плотные ткани содержат высокомолекулярные соединения, среди которых наибольшее значение имеют белки. Белки – полимеры аминокислот – являются полиэлектролитами. Каждый белок характеризуется определенным значением рН, когда он является нейтральной частицей (рНИЭТ). Величина рНИЭТ различных белков колеблется в широких пределах.
Реакция крови сдвинута в щелочную сторону от рНИЭТ белков плазмы и гемоглобина, поэтому эти белки находятся в крови в виде анионов. Являясь сильными сопряженными основаниями, они связывают кислые продукты метаболизма и играют существенную роль в механизме буферного действия крови. В клиническом анализе при электрофоретическом разделении белков сыворотки крови, мочи, спинномозговой жидкости величину рНИЭТ необходимо знать при выборе поддерживающей среды.
Вживом организме примером студней, образованных ВМС, могут служить протоплазма клетки, хрусталик глаза. Процессы обезвоживания и набухания ВМС наблюдаются при регенерации тканей, отеках, воспалениях. Процессы старения белков связаны со структурообразованием полимеров. Биологическое значение процессов старения студней проявляется в изменении проницаемости клеточных мембран, что вызывает нарушение обмена клетки с окружающей средой. Образование слоистых камней в желчном пузыре и почках объясняется периодичностью химических реакций в студнях. Этим же свойством студней пользуются при иммунологических методах исследований плазменных и сывороточных белков (образование преципитатов при реакциях между антителами и антигенами).
Полученные знания помогут студентам-медикам при изучении курсов нормальной анатомии (создание искусственных органов), хирургии (применение искусственных органов), микробиологии
46
(искусственные среды), гигиены питания, фармакологии (изучение лекарственных форм).
ЦЕЛЬ ЗАНЯТИЯ:
1.Освоить экспериментальные методы определения изоэлектрической точки белков.
2.Научиться получать студни и гели.
3.Ознакомиться с явлениями синерезиса и периодических структур.
ЗАДАНИЕ:
Выполните пять опытов, дайте объяснения механизма и напишите уравнения реакций в демонстрационных опытах.
ЗАДАНИЕ 1.
Определите рН изоэлектрической точки по набуханию.
ЗАДАНИЕ 2.
Определите рН изоэлектрической точки по высаливанию (осаждение).
ЗАДАНИЕ 3.
Определите ИЭТ белка методом электрофореза (демонстрационный).
ЗАДАНИЕ 4.
Получите гель кремниевой кислоты, покажите необратимость процесса гелеобразования.
ЗАДАНИЕ 5.
Получите студень желатина и докажите обратимость студнеобразования.
ЗАДАНИЕ 6.
Дайте объяснение периодическим реакциям в студнях.
ЗАДАНИЕ 7.
Объясните явление синерезиса в студнях на примере крахмала.
МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ВЫПОЛНЕНИЮ РАБОТЫ:
ОПЫТ 1. Определение ИЭТ белка по набуханию
В пять сухих мерных пробирок насыпьте по 0,5 мл сухого измельченного желатина. К ним осторожно добавьте по 5 мл ацетатных буферов с рН 3,8; 4,4; 4,9; 5,4; 5,7 и перемешайте. Через 15-20 мин измерьте объем набухшего желатина в каждой пробирке. Результаты занесите в табл. 13.
Таблица 13
47
рН растворов |
3,8 |
4,4 |
4,9 |
5,4 |
5,7 |
Объем набухшего желатина, мл |
|
|
|
|
|
ВЫВОДЫ:
1.Укажите рНИЭТ желатина и обоснуйте ответ.
2.Объясните, почему при этом рН набухание минимальное.
ОПЫТ 2. Определение ИЭТ белка по высаливанию
В пять сухих мерных пробирок налейте по 2 мл ацетатных
буферных растворов с рН 3,8; 4,4; 4,9; 5,4; 5,7 и по 1 мл 0,5 % раствора желатина, перемешайте. Затем добавьте в каждую пробирку по 3 мл ацетона и снова быстро перемешайте. Занесите в табл. 14 результаты наблюдения, оценивая степень помутнения.
Таблица 14
рН растворов |
3,8 |
4,4 |
4,9 |
5,4 |
5,7 |
Степень помутнения |
|
|
|
|
|
ВЫВОДЫ:
1.Укажите рНИЭТ желатина на основании опытных данных.
2.Объясните, почему осаждение белка в этом случае максимально. При объяснении учтите механизм осаждения белка под действием ацетона
ОПЫТ 3. Определение ИЭТ белка методом электрофореза
В три U-образные трубки пипеткой налейте по 10 мл буферных
растворов с рН 3,8; 4,7; 5,7 и осторожно по 1 мл 0,4 % раствора казеина. Потом с помощью тонкого капилляра по стенке трубки добавьте дистиллированную воду (сохраните резкую границу раздела белка и воды). В воду погрузите два платиновых электрода и включите постоянный ток (100 В). Через 20-30 мин отметьте высаливание белка. Результаты опытов занесите в табл. 15.
|
|
|
Таблица 15 |
||
рН растворов |
3,8 |
4,4 |
|
4,9 |
|
Наличие осаждения |
|
|
|
|
|
Заряд частиц белка (+, −, 0) |
|
|
|
|
|
ВЫВОДЫ: |
|
|
|
|
|
1.Определите рНИЭТ казеина по результатам опыта.
2.Объясните механизм электрофореза белка.
48
3. Объясните, почему при рНИЭТ частицы белка наименее подвижны.
ОПЫТ 4. Получение геля
а) В пробирку налейте 5 мл 20 % раствора силиката натрия и при перемешивании стеклянной палочкой добавьте 3 мл 2 М H2SO4. Образуется аморфный продукт, через несколько минут переходящий в белый гель. При стоянии в течение часа на его поверхности появляются капли жидкости.
б) В пробирку поместите несколько кусочков ксерогеля кремниевой кислоты, добавьте 5 мл дистиллированной воды, сделайте вывод об обратимости или необратимости процесса гелеобразования.
ВЫВОДЫ:
1.Напишите уравнение реакции получения геля кремниевой кислоты.
2.Укажите строение мицеллы, полученной при избытке H2SO4.
3.Объясните, какой процесс происходит при стоянии геля.
ОПЫТ 5. Получение студня
а) Налейте в пробирку 2-3 мл горячего 6 % раствора желатина и охладите под струей воды из водопроводного крана. Объясните, почему желатин не выливается из пробирки.
б) К небольшому количеству измельченного желатина в пробирке добавьте 5 мл дистиллированной воды, перемешайте и дайте набухнуть при комнатной температуре. сделайте вывод об обратимости процесса студнеобразования.
ОПЫТ 6. Периодические реакции в студнях (демонстрационный)
Запишите реакцию между AgNO3 и K2Cr2O7, зарисуйте концентрические кольца бурого цвета, полученные в чашке Петри. Чем объясняется неравномерность распределения осадка в студне?
ОПЫТ 7. Явление синерезиса (демонстрационный)
К полученному при стоянии студня крахмала и раствору над ним добавьте I2. Что представляет собой явление синерезиса?
КОНТРОЛЬНЫЕ ВОПРОСЫ:
1. Если в смеси имеется два белка, рНИЭТ = 4,7; рНИЭТ = 9,5, к какому электроду они будут передвигаться при рН = 8,5?
49
2.У белка рНИЭТ = 9,7. Будет ли краситель, имеющий отрицательный заряд, взаимодействовать с этим белком в нейтральной среде?
3.Покажите, пользуясь схемой гелеобразования, является ли образование геля Fe(OH)3 обратимым.
4.Будет ли синерезис ускоряться, если при этом рН = рНИЭТ? дайте ответ, основываясь на структуре ВМС при рНИЭТ.
ОБРАЗЕЦ ОТВЕТА НА КОНТРОЛЬНЫЕ ВОПРОСЫ:
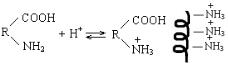
ВОПРОС: При каком рН надо делить белки на катионите? ОТВЕТ: На катионите можно отделить положительно заряженные ионы от нейтральных и отрицательных. При рН <
рНИЭТ частицы белка имеют заряд (+) и строение растянутой спирали:
Поэтому через катионит надо пропускать смесь белков в буферном растворе с таким значением рН, чтобы одни
находились в форме
R |
/ COOH |
|
|
||
|
||
|
\ N H |
|
|
3 |
(рН < рНИЭТ), а остальные при рН >
рНИЭТ или рН = рНИЭТ.
ЛИТЕРАТУРА:
1. С. 539-540, 544-545; 3. С. 215-218, 229-234, 239, 242-244; 5. С. 127-128; 6. С. 748-751.
50