Материал: Практикум по общей химии
РАБОТА 12. ХИМИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ И СПЛАВОВ
Актуальность темы обусловлена тем, что металлы и сплавы находят широкое применение в медицине. В терапевтической стоматологии сплавы металлов на основе ртути, галлия используются в качестве постоянных пломбировочных материалов. сплавы на основе золота, серебра, нержавеющей стали на основе железа с добавками хрома, никеля, кобальта, марганца используются для изготовления протезов в ортопедической стоматологии. В качестве материалов припоев для спаивания отдельных деталей протезов также применяются сплавы. Все используемые материалы должны обладать химической и электрохимической устойчивостью.
Знание о поведении металлов и сплавов в различных средах, их коррозионной устойчивости необходимо при последующем изучении курсов терапевтической и ортопедической стоматологии.
ЦЕЛЬ ЗАНЯТИЯ:
1.Ознакомиться с явлением электрохимической коррозии металлов в различных средах.
2.Научиться записывать электрохимические процессы на электродах.
3.Научиться оценивать возможность протекания анодного и катодного процессов.
4.Ознакомиться с явлением пассивации металла.
ЗАДАНИЕ:
Выполните три лабораторных опыта и составьте отчет по работе.
МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ВЫПОЛНЕНИЮ РАБОТЫ:
ОПЫТ 1. Коррозия металлов в нейтральной среде
Выполнение: в U-образную трубку налейте раствор NaCl, к которому добавьте 2-3 капли фенолфталеина и красной кровяной соли K3[Fe(CN)6]. В одно колено трубки опустите очищенный железный гвоздь, в другое – медную проволоку. Оба электрода соедините проводником. Что при этом наблюдаете?
ВЫВОДЫ:
51
1. Учитывая значения потенциалов Ео 2 |
/ Fe |
0,44B, |
Fe |
|
E |
o |
2 |
|
0,34B, |
|
Cu |
/ Cu |
||||
|
|
|
o |
|
|
|
E |
2H |
|
|
O |
2 |
O/ 4OH |
|
2 |
|
|
0,4B
,
напишите электрохимические процессы на электродах. Какой из металлов окисляется, т.е. подвергается коррозии и почему?
2.Объясните появление малинового окрашивания в колене с медным электродом.
3.Объясните, почему в колене с железным электродом раствор становится синим?
ОПЫТ 2. Коррозия металлов в кислой среде
Выполнение: а) в одну пробирку налейте 3 мл 0,1 М раствора
НС1, в другую – 3 мл 1 М раствора НС1. Опустите в эти пробирки кусочки железа (гвозди).
По выделению пузырьков водорода судите о протекании коррозии. Оцените, имеются ли различия в скорости коррозии железа в растворах с различной концентрацией ионов водорода.
б) Опустите в пробирку с кислотой медную проволочку. Убедитесь в отсутствии коррозии.
в) Поместите в эти же растворы кислот кусочки цинка. Оцените скорость коррозии цинка в разбавленном и концентрированном растворах кислот.
г) Коснитесь кусочка цинка в разбавленном растворе железным гвоздем. Наблюдайте интенсивное выделение водорода на железе. Опустите в раствор медную проволоку и наблюдайте выделение водорода на ней при касании цинка.
ВЫВОДЫ:
1.Напишите уравнения катодного и анодного процессов коррозии железа и цинка. Докажите возможности ее протекания, учитывая значения потенциалов процессов. Почему коррозия меди в кислоте не протекает?
2.Исходя из независимости скорости коррозии железа от концентрации кислоты и возрастания скорости коррозии цинка с концентрацией кислоты, определите, скорость какого процесса (катодного или анодного) определяет скорость коррозии.
52
3. Объясните, почему при касании цинка железом или медью скорость коррозии возрастает. На поверхности каких металлов происходит катодный и анодный процессы?
ОПЫТ 3. Пассивация железа
Выполнение: зачищенный гвоздь опустите в раствор K2CrO4, затем, промыв водой, в раствор CuSO4. Наблюдается ли изменение цвета поверхности гвоздя?
Потерев гвоздь о стенку сосуда, вновь опустите его в раствор с CuSO4. Что происходит?
ВЫВОДЫ:
1.Укажите, какая реакция может протекать на поверхности железа при погружении его в раствор сульфата меди.
2.Объясните, почему после обработки железа в растворе K2CrO4 медь не выделяется на поверхности железа?
3.Объясните влияние трения.
КОНТРОЛЬНЫЕ ВОПРОСЫ:
1.Корродирует ли железо в кислой среде? Корродирует ли медь в кислой среде? Протекает ли коррозия этих металлов в кислой среде в присутствии кислорода? Запишите уравнения анодного и катодного процессов.
2.Объясните, за счет чего происходит процесс электрохимической коррозии медной амальгамы в полости рта.
E |
o |
|
|
|
0,34B, |
E |
o |
|
|
|
Cu |
2 |
|
/ Cu |
Hg |
2 |
|
||||
|
|
|
||||||||
|
|
|
|
|
|
|
0,85B. / Hg
Чем можно объяснить высокую коррозионную устойчивость серебряной амальгамы?
EoAg / Ag 0,80B
3. Поясните, почему нежелательны стальные протезы при наличии металлических пломб в полости рта? Запишите уравнения возможных процессов.
ЛИТЕРАТУРА:
2. С. 234-237; 5. С. 98-100; 6. С. 654-661.
53
РАБОТА 13. МЕТОД КОМПЛЕКСОНОМЕТРИИ. ОПРЕДЕЛЕНИЕ ОБЩЕЙ ЖЕСТКОСТИ ВОДЫ (для медико-профилактического факультета)
Вода, содержащая большое количество солей кальция и магния, называется жесткой. Жесткость воды определяется количеством ммоль экв ионов кальция и магния в 1 л воды. Жесткость природных вод меняется в широких пределах. Она различна в различных водоемах и в разное время года. Имеется следующая примерная классификация вод: до 4 ммоль экв/л – мягкая; 4-8 – средней жесткости; 8-12 – жесткая: 12 – очень жесткая.
Очень жесткая вода при нагревании дает накипь, затрудняет окраску и стирку, не годится для ряда производств. Установлено, что жесткость воды влияет на состояние и деятельность сердечно-сосудистой системы.
ЦЕЛЬ ЗАНЯТИЯ:
1.Ознакомиться с возможностями метода трилонометрии.
2.Научиться записывать реакции образования внутрикомплексных соединений.
3.Познакомиться с условиями проведения анализа, выбором индикатора.
4.Освоить методику трилонометрического титрования.
5.Овладеть методикой трилонометрического определения содержания ионов кальция и магния в водопроводной воде.
6.Научиться на основании результатов титрования рассчитывать содержание ионов Са2+ и Mg2+ в воде.
ЗАДАНИЕ:
Выполните трилонометрическое определение содержания ионов Са2+ и Mg2+ и рассчитайте жесткость воды в ммоль экв/л. Представьте отчет.
МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ВЫПОЛНЕНИЮ РАБОТЫ:
Рабочий раствор: трилон Б СЭ = 0,01 моль экв/л. Вспомогательный раствор: аммиачно-буферный (рН = 9,5-10,0). Индикатор: хромоген черный.
Способ титрования: прямой.
54
Для установления точки эквивалентности используется индикатор хромоген черный, который в зависимости от рН раствора ионизирует по-разному:
H3V |
↔ H2V- + H+ |
↔ HV2- + 2H+ |
↔ V3- + 3H+ |
рН<6 |
pH=6 |
pH=7-11 |
pH>11,5 |
|
винно-красный |
синий |
оранжевый |
При рН = 9,5-10,0 комплекс Mg2+ и Са2+ (Ме2+) с индикатором имеет винно-красную окраску:
Ме2+ + HV2- |
→ MeV- + H+ |
синий |
винно-красный |
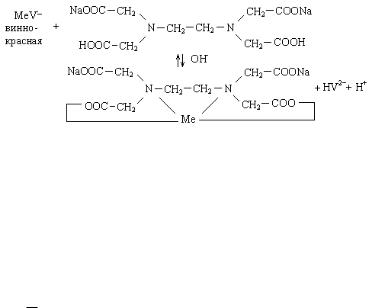
При титровании трилоном Б в точке эквивалентности наблюдается полный переход металла из непрочного комплекса с индикатором в более прочный комплекс с трилоном Б, и винно-
красная окраска меняется на синюю: |
|
|
|
|||||
MeV |
- |
+ |
Na2H2I |
ОН |
|
Na2MeI + |
2- |
+ |
|
|
HV |
+ H |
|||||
винно-красн. |
б/цветн. |
|
|
б/цветн. |
синяя |
|||
или:
В коническую колбу с помощью цилиндра отмерьте 20 мл воды. Добавьте 5 мл буферного раствора мерной пробиркой и несколько кристалликов индикатора. Исследуемый раствор приобретает винно-красную окраску. титруйте из бюретки трилоном до перехода винно-красной окраски в синюю. Показания бюретки отметьте с точностью до 0,1 мл. Титрование повторите до получения трех результатов, отличающихся не более чем на 0,1±0,2 мл. Результаты титрования занесите в табл.
16.
Исследуемый раствор: вода
По V тр. рассчитайте содержание ионов Mg2+, Са2+ в ммоль экв/л, т.е. жесткость воды, сделайте вывод.
55