Материал: Пат. анатомия боевых поражений_2002

Т Р А В М А
Активация симпатической нервной системы Стимуляция гипоталамо-гипофизарно-адреналовой системы
Системные нарушения гемодинамики |
Катаболический эффект |
||
Кровопотеря и шок |
Микробное загрязнение |
Эндотоксикация |
|
Вовлечение иммунной системы в реализацию общего адаптационного синдрома Активация и антигенная стимуляция
Неспецифическая фаза |
Специфическая фаза |
||
Активация биосинтеза |
Фагоцитоз |
|
Бласттрансформация |
|
И М М У Н О Г Е Н Е З |
||
Коммитация |
Приобретение цитотоксичности |
Антителогенез |
|
Центральные органы |
Периферические органы и ткани |
||
Усиление пролиферации и системное перераспределение клеток |
|||
Акцидентальная трансформация, миелоз и плазматизация |
|||
Становление гуморальных и клеточных реакций иммунитета |
|||
Посттравматическая |
|
|
Адаптивная оптимизация |
иммуносупрессия |
|
иммунобиологического надзора |
|
Иммунологическое обеспечение воспаления и регенерации
Формирование грануляционной ткани и заживление ран
Рис. 36. Действие эндокринных и иммунных механизмов в патогенезе травматической болезни у раненых (по В.С. Сидорину /100/)
Следует учитывать влияние на иммунную и эндокринную системы стрес- сорных ситуационно обусловленных воздействий, которые находят свое отраже- ние в т. н. фоновых процессах перестройки иммунно-эндокринного статуса воен- нослужащего, как атрофического, так и гиперпластического характера /33, 100/.
Гемокоагуляционные реакции первого периода ТБ выражаются в волно- образных изменениях коагулирующей активности крови с чередованием пе- риодов гипер- и гипокоагуляции. Их пусковыми моментами могут быть как ги- пертромбопластинемия, так и гиперфибринолиз.
ДВС-синдром характеризуется закупоркой кровеносных капилляров внутренних органов, обычно, почек (рис. 37), легких, надпочечников тромбами в виде компактных червеобразных свертков фибрина с тромбоцитами. Их сле- дует отличать от посмертных кровяных свертков и сгустков, образующихся в консервированной крови, переливаемой пострадавшим.
51
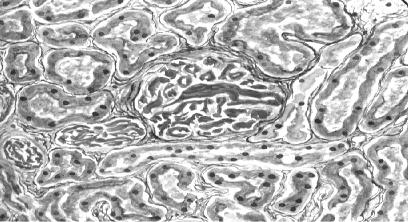
Рис. 37. Микропрепарат почки: закупорка капилля- ров клубочка фибриновы- ми тромбами (окраска хро- мотропом 2 Б — водным голубым, × 400), рисунок Н. Д. Клочкова
При клинико-анатомической трактовке летальных исходов у раненых с ге- мокоагуляционными нарушениями необходимо учитывать значения показате- лей, характеризующих системы свертывания крови и фибринолиза. ДВС- синдром всегда сопровождается усилением фибринолитической активности кро- ви (от 20 до 100 %) и гипофибриногенемией (менее 3 г × л–1). Очаги кровоизлия- ний в области ранения или операционного поля при этом практически не содер- жат волокон фибрина.
Ускорение времени рекальцификации, рост протромбинового индекса и количества фибриногена, появление фибриногена Б, снижение фибринолитиче- ской активности указывают на развитие у раненого предтромботического со- стояния, которое чаще всего реализуется в виде флеботромбоза.
Систематические исследования легких у умерших после огнестрельных ранений позволили по-новому подойти к оценке танатогенетической значимости микротромбоэмболии сосудов легких, источником которой являются тромбиро- ванные межмышечные венулы нижних конечностей. Гематологические сдвиги проявляются развитием лейкоцитоза сосудов микроциркуляторного русла лег- ких, печени, головного мозга, других органов, что, вероятно, связано не только с ускоренным выбросом лейкоцитов из костного мозга, но также с изменением по- верхностно-активных свойств лейкоцитов и сосудистого эндотелия.
Указанная выше характеристика первого периода ТБ в «чистом» виде свойственна случаям ранений, не осложненных клинически значимой кровопо- терей (не превышающей 0,5 л). При наличии таковой патогенез ТБ становится тесно связанным с системной гипотензией и гиповолемией.
Непосредственными причинами смерти (НПС) в первом периоде ТБ явля-
ются огнестрельные повреждения жизненно важных органов с развитием их первичной недостаточности: сердечной и дыхательной, а также мозговой комы. При сочетанных и множественных ранениях и тяжелых минно-взрывных повре- ждениях эта недостаточность нередко принимает полиорганный характер. Часто НПС служат острая кровопотеря и постгеморрагическая анемия, гемо- и пневмо- торакс, разлитой «каловый» перитонит (реактивная фаза); реже — воздушная, жировая (рис. 38, а, б) и тромбоэмболия, а также другие причины (рис. 32).
52
а |
|
б |
|
|
|
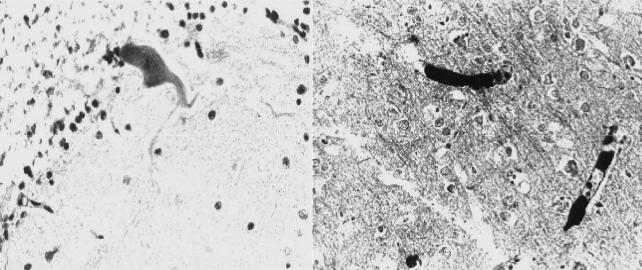
Рис. 38. Микропрепарат головного мозга (взрывная травма, подрыв на мест- ности, смерть через 1,5 сут от жировой эмболии сосудов головного мозга): а — на- бухание отростков клеток Пуркинье, некроз зернистого слоя мозжечка (окраска ге- матоксилином и эозином, × 500); б — жировые эмболы (черного цвета) в сосудах коры головного мозга (окраска суданом черным, × 500); рисунок Н. Д. Клочкова
Особое место в системных гипотензивных реакциях при ТБ занимает травматический шок, который возникает, даже если при отсутствии кровопотери не удается предупредить депонирование крови в микроциркуляторном русле. Возникающая при шоке гипотензия бывает связана как с уменьшением ОЦК, так и с сердечной недостаточностью, приводящей к синдрому малого выброса.
1.4.2. П е р и о д т р а в м а т и ч е с к о г о ш о к а
Второй период — травматического шока не является обязательным в тече- нии ТБ. При этом пролонгированный генерализованный спазм пре- и посткапил- лярных сфинктеров (эректильная фаза) сменяется их последовательным стойким парезом (торпидная фаза), что связано с нарастанием гипоксии и ацидоза. Сниже- ние регионарной перфузии внутренних органов, начинающееся в периоде первич- ных реакций, при шоке достигает своего максимума. Сердечная постнагрузка уже не компенсируется открытием артериовенозных шунтов, а более длительное со-
хранение спазма посткапиллярных сфинктеров по сравнению с прекапиллярными приводит к «заболачиванию» микроциркуляторного русла кровью с высоким ге- матокритом. В клинической картине этому соответствует стойкое снижение арте- риального давления. Важнейшим анатомическим субстратом шока является ха- рактерное полнокровие капиллярного сектора микроциркуляторного русла парен- химатозных органов (легких, сердца, печени, почек, селезенки, головного мозга, кишок). Однако указанные гистологические признаки микроциркуляторных на- рушений при шоке на вскрытии регистрируют редко, так как большинство ране- ных успевает получить тот или иной объем противошоковой терапии.
53
Таким образом, травматический шок рассматривают как крайнее кли- ническое выражение неадекватной капиллярной перфузии. Прямым ее следст-
вием оказываются ишемические повреждения паренхиматозных элементов конкретных гистионов. Поэтому патологоанатомическая диагностика травма-
тического шока базируется на результатах комплексного исследования с учетом не только признаков расстройств микроциркуляции, но и их ближайших по- следствий в виде ишемических повреждений.
В головном мозге снижение кровотока при шоке приводит к появлению ишемически измененных невроцитов — ишемической энцефалопатии (рис. 39).
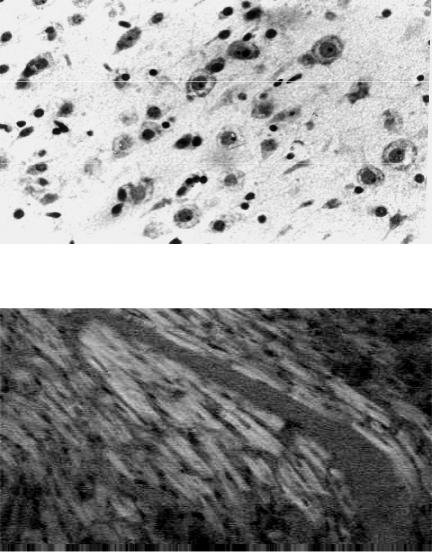
Рис. 39. Микропрепарат
головного мозга при ишемической энцефало- патии: очаговый
лизис нейронов в слое пирамидных клеток серо- го вещества коры голов- ного мозга (окраска гема- токсилином и эозином, × 500), рисунок Н.Д.
Клочкова
В миокарде наблюдают (рис. 40) фрагментацию кардиомиоцитов и их контрактурные изменения (ишемическую кардиомиопатию).
Рис. 40. Микропрепарат сердца при ишемиче- ской кардиомиопатии: в миокарде в поляризо- ванном свете — усиле- ние анизотропии, свиде- тельствующее о кон-
трактурных изменениях кардиомиоцитов (окра-
ска гематоксилином и эозином, × 500), рисунок М. В. Рогачева
Влегких снижение венозного возврата крови вызывает появление моза- ичных ателектазов, получивших название гемодинамических.
Впочках отмечают набухание и зернистую дистрофию эпителия про- ксимальных канальцев и восходящих отделов петель Генле (ишемическую нефропатию).
Впечени на фоне предшествовавшего в первом периоде ТБ болезни спазма артериол и шунтирования кровотока обнаруживают (рис. 41) моноцел- люлярные и групповые некрозы гепатоцитов (ишемическую гепатопатию).
54
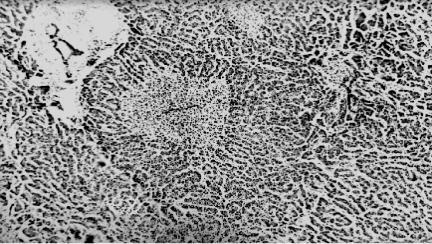
Рис. 41. Микропрепарат печени при ишемиче- ской гепатопатии: мо- ноцеллюлярные и груп- повые некрозы гепато- цитов (окраска гематок- силином и эозином, × 100), рисунок С.А.
Повзуна
Указанные ишемические изменения могут быть связаны с кровопотерей, однако для танатогенетически значимой кровопотери характерно не полнокро- вие микроциркуляторного русла (если не считать синдрома массивных транс- фузий), а, напротив, — его малокровие.
Патоморфология кровопотери определяется объемом и скоростью крово- течения, временем, прошедшим после его остановки и/или восполнения кровопо- тери. В соответствии с этим выделяют три варианта изменений, характерных:
1)для смерти при большой скорости кровотечения (при ранении сердца, магистральных сосудов) и плохом восполнении кровопотери;
2)для замедленной смерти при неполном восполнении кровопотери (смерть через 1,5 — 2 ч);
3)для смерти через 1 — 2 суток, обычно уже при избыточном восполне- нии кровопотери.
В первом случае имеет место малокровие большинства внутренних ор- ганов, за исключением головного мозга, легких и желез внутренней секреции.
Во втором случае при восстановлении перфузии внутренних органов от- мечают уменьшение их массы и наличие распространенных лейкостазов.
Наконец, в третьем случае наблюдают увеличение массы внутренних ор- ганов, переполнение их сосудов кровью, отечные изменения.
В основе морфогенеза изменений внутренних органов при смерти от кро- вопотери лежат последствия нарушений организменной (системной) и, особен- но, внутриорганной гемодинамики, приводящие к возникновению гипоксиче- ских повреждений паренхиматозных элементов гистионов. Общим для всех ва-
риантов летальных исходов при кровопотере является развитие ишемических изменений внутренних органов, выраженность которых зависит от времени, прошедшего после получения ранения.
В головном мозге кровопотеря приводит к расширению рестриктивных сосудов, которое, однако, не предупреждает обескровливания мозга и развития ишемических изменений нейронов (рис. 42).
55