Материал: конспект физика
3.3. Елементарна кінетична теорія газів
Ідеальний газ – це сукупність однакових молекул, які хаотично рухаються і не взаємодіють між собою на відстані. Розміри молекул настільки малі, що їх сумарним об’ємом можна знехтувати порівняно з об’ємом посудини.
Основне рівняння молекулярно-кінетичної теорії для тиску. Тиск газу на стінки посудини обумовлений співударами молекул зі стінками і передачею їм імпульсу. При цьому виникає тиск газу на стінки, який дорівнює
p=n k T,
де n – кількість молекул в одиниці об’єму, k=R / N0 – стала Больцмана, R =8,31 Дж / (K моль) – універсальна газова стала, N0 =6,023 10 23 моль–1 число Авогадро (кількість молекул в одному молі речовини).
Ступені вільності. Ступенями вільності механічної системи називаються незалежні змінні, які потрібно задати, щоб визначити положення системи у просторі.
Матеріальна точка має три ступеня вільності – це її координати (x,y,z). Тверде тіло має шість ступенів вільності: три координати центра інерції тіла (xс , yс , zс) і три кути (, , ) які визначають положення у просторі двох пов’язаних з тілом взаємно перпендикулярних осей, які проходять через центр інерції тіла (див. рис. 3.2, а). Величини (xс , yс , zс) змінюються у процесі поступального руху тіла і називаються поступальними ступенями вільності. Кути (, , ) змінюються у процесі обертального руху тіла і називаються обертальними ступенями вільності.
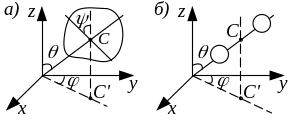
Рис. 3.2
Система двох жорстко зв’язаних між собою матеріальних точок (двохатомна молекула) має п’ять ступенів вільності (xс , yс , zс , , ) (див. рис. 3.2, б). При обертанні навколо власної осі положення молекули не змінюється, тому необхідно задавати тільки два кути.
Принцип рівнорозподілу енергії за ступенями вільності. Ні один з видів руху молекули не має переваги перед іншими, тому на будь-яку ступінь вільності молекули у середньому припадає однакова енергія:
![]() .
.
Тоді середня енергія теплового руху молекул:
![]() ,
,
де
i = nпост +nоб +2nкол , (3.2)
nпост – кількість поступальних ступенів вільності; nоб – обертальних, nкол – коливальних (коливальні ступені вільності мають вдвічі більшу енергоємність, ніж поступальні й обертальні, і тому у формулу (3.2) вони входять подвійно). При невисоких температурах коливальні ступені вільності не збуджені і число ступенів вільності дорівнює: i = 3– для одноатомних молекул; i = 5 – для двохатомних молекул; i = 6 – для трьох (і вище) атомних молекул (тобто як і для твердого тіла).
Внутрішня енергія ідеального газу складається з енергії теплового руху окремих молекул і для довільної маси газу m визначається формулою
![]() .
.
Теплоємність газів. Для газів розрізняють два типи теплоємностей: при сталому об’ємі – CV і при сталому тиску – Cp .
Молярні теплоємності, тобто теплоємності одного моля газу, визначаються формулами:
![]() , Cp
= CV+R.
, Cp
= CV+R.
Адіабатний
процес
– це процес, який протікає без теплообміну
газу із зовнішнім середовищем (тобто
d Q=0).
Якщо покласти d Q=0
у рівнянні першого закону термодинаміки
![]() ,
то отримаємо рівняння адіабати ідеального
газу:
,
то отримаємо рівняння адіабати ідеального
газу:
pV = const, (3.3)
де = Cp / CV = (i+2)/i, – коефіцієнт адіабати, який визначається кількістю ступенів вільності i молекули. Формула (3.3) носить назву рівняння Пуассона.
3.4. Розподіл молекул за швидкостями і потенціальними енергіями
Розподіл молекул за швидкостями. Молекули газу рухаються з різними швидкостями. При цьому величини і напрямки швидкостей кожної молекули безперервно змінюються через зіткнення. Можливі значення швидкості молекул лежать у межах від 0 до ∞. Дуже великі і дуже малі порівняно з середніми швидкості мало ймовірні.
Розподіл молекул газу за швидкостями визначається функцією розподілу Максвелла, яка має вигляд:
![]() , (3.4)
, (3.4)
де m – маса молекули, v – її швидкість, А – стала, яка залежить від m та T . Графік цієї функції схематично показано на рис. 3.3. Функція розподілу f (v) визначає густину ймовірності, тобто ймовірність того, що швидкість молекул лежить у заданому одиничному інтервалі швидкостей. Тоді f (v)v визначає ймовірність того, що швидкість молекул лежить в інтервалі швидкостей від v до v +v (v – інтервал швидкостей). Одночасно f (v)v визначає відносну кількість молекул, швидкості яких лежать в інтервалі швидкості від v до v +v.
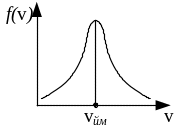
Рис. 3.3
Швидкість, що відповідає максимуму функції розподілу f (v), називається найбільш ймовірною швидкістю
![]() ,
,
де m – маса молекули, k – стала Больцмана, T – абсолютна температура. Знаючи розподіл молекул за швидкостями, можна визначити середнє значення швидкості молекул газу:
![]() .
.
Функція (3.4) розподілу молекул газу за швидкостями одночасно є і функцією розподілу молекул газу за кінетичними енергіями:
![]() ,
,
де k– кінетична енергія молекул, А – стала, що залежить від m та T .
Розподіл молекул за потенціальними енергіями описується функцією розподілу Больцмана (див. рис. 3.4):
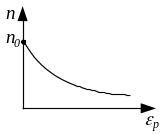
Рис. 3.4
![]() ,
,
де n – кількість молекул в одиниці об’єму з потенціальною енергією k ; n0 – кількість молекул в одиниці об’єму з потенціальною енергією p=0. Молекули розподілені з більшою густиною там, де менша їх потенціальна енергія.
Середня
довжина вільного пробігу молекул газу.
Мінімальна
відстань, на яку наближаються при
співударі центри двох молекул, називається
ефективним діаметром молекули (див.
рис. 3.5). Величина
![]() – ефективний переріз молекули. Ефективний
діаметр молекули зменшується із
зростанням температури, бо при цьому
зростають швидкості теплового руху
молекул газу. Середній шлях між двома
послідовними співударами
– ефективний переріз молекули. Ефективний
діаметр молекули зменшується із
зростанням температури, бо при цьому
зростають швидкості теплового руху
молекул газу. Середній шлях між двома
послідовними співударами
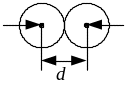
Рис. 3.5
молекули називається середньою довжиною вільного пробігу і визначається за формулою
![]() .
.
Оскільки при T=const кількість молекул в одиниці об’єму n p, то 1/p, тобто із зниженням тиску середня довжина вільного пробігу збільшується.
3.5. Явища переносу
Це явища, які виникають при відхилені газу від стану рівноваги. До них відносяться: внутрішнє тертя, теплопровідність і дифузія.
Внутрішнє тертя. Якщо швидкості впорядкованого руху молекул у потоці газу змінюються від шару до шару (тобто шари рухаються з різними швидкостями), то між шарами газу виникають сили внутрішнього тертя (див. рис. 3.6), які визначаються за формулою
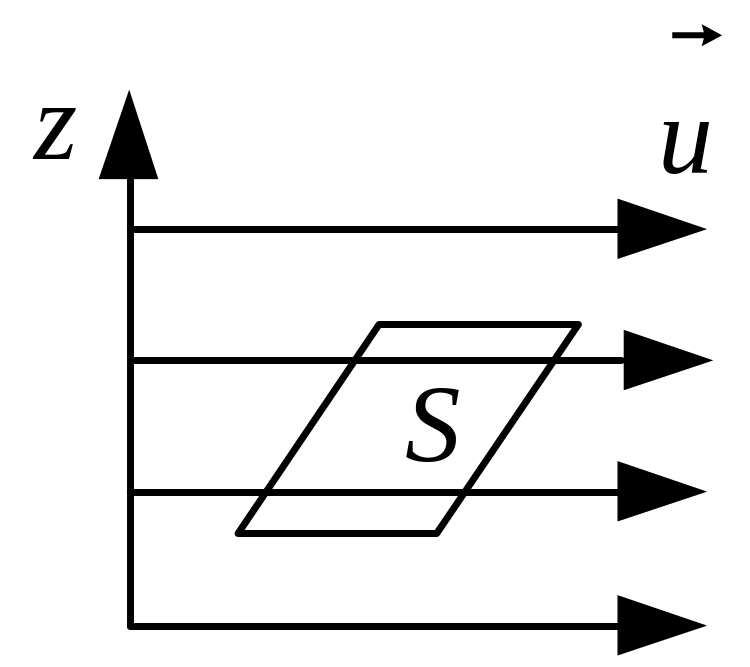
Рис. 3.6
![]() ,
,
де
– коефіцієнт внутрішнього тертя,
![]() – градієнт швидкості впорядкованого
руху молекул, який характеризує зміну
швидкості у поперечному напрямку z,
S
– площа шарів. Коефіцієнт внутрішнього
тертя чисельно рівний силі, що діє на
одиничну площадку при одиничному
градієнті швидкості.
– градієнт швидкості впорядкованого
руху молекул, який характеризує зміну
швидкості у поперечному напрямку z,
S
– площа шарів. Коефіцієнт внутрішнього
тертя чисельно рівний силі, що діє на
одиничну площадку при одиничному
градієнті швидкості.
Молекули газу переходять внаслідок теплового руху з шару в шар і переносять з собою імпульс. У результаті імпульс більш повільного шару зростає, а більш швидкого зменшується. Перенесення імпульсу з шару в шар і обумовлює виникнення внутрішнього тертя.
У молекулярно-кінетичній теорії є формула для коефіцієнта внутрішнього тертя
![]() ,
,
де – густина газу; <v> – середня швидкість теплового руху молекул; – середня довжина вільного пробігу молекул.
Теплопровідність газів. Якщо в газі вздовж деякого напрямку z (див. рис. 3.7) температура не залишається сталою, то вздовж цього напрямку встановлюється потік q тепла в напрямку зменшення температури.
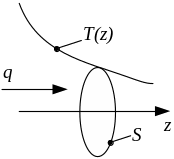
Рис. 3.7
![]() ,
,
де
![]() – потік теплоти, тобто кількість тепла,
яка переноситься через площадку S
у одиницю часу,
– потік теплоти, тобто кількість тепла,
яка переноситься через площадку S
у одиницю часу,
![]() – градієнт температури, який характеризує
швидкість зміни температури вздовж
осі z,
S
–
– градієнт температури, який характеризує
швидкість зміни температури вздовж
осі z,
S
–
площа ділянки S, – коефіцієнт теплопровідності, який дорівнює потоку тепла через одиничну площадку при одиничному градієнті температури.
Теплопровідність обумовлена тим, що переміщуючись внаслідок теплового руху, кожна молекула переносить з місця з більшою температурою в місце з меншою температурою енергію < >=ikT/2. У результаті теплопровідності температура менш нагрітих місць підвищується, а температура більш нагрітих – зменшується. Коли температури вирівнюються, теплопровідність припиняється.
Дифузія у газах. Якщо концентрація С (тобто, маса в одиниці об’єму) газу вздовж деякого напрямку z у просторі (див. рис. 3.8) змінюється, то внаслідок теплового руху молекул буде виникати процес вирівнювання концентрацій, який супроводжується переносом маси. У результаті в напрямку зменшення концентрації виникає потік маси:
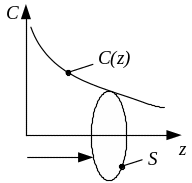
Рис. 3.8
![]() ,
,
де
– потік маси, тобто маса, що переноситься
через площадку
![]() в одиницю часу,
в одиницю часу,
![]() –градієнт концентрації, який характеризує
швидкість зміни концентрації вздовж
осі
z,
S
– плоска
перпендикулярна до осі z
площадка; D
– коефіцієнт дифузії,
–градієнт концентрації, який характеризує
швидкість зміни концентрації вздовж
осі
z,
S
– плоска
перпендикулярна до осі z
площадка; D
– коефіцієнт дифузії,
який чисельно рівний потоку маси через одиничну площадку при одиничному градієнті концентрації. Коли концентрація вирівнюється, дифузія припиняється.