Материал: file000247
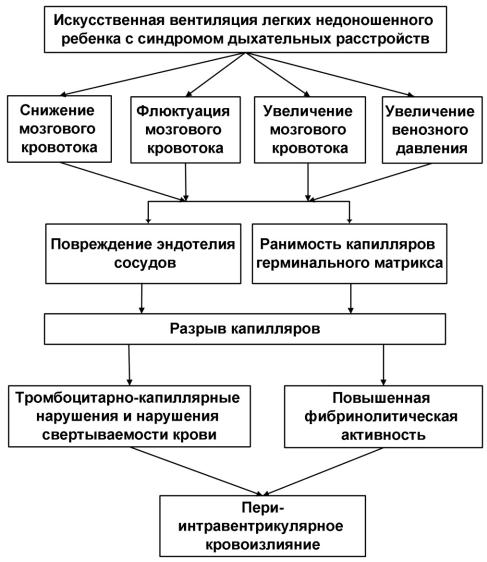
Взаимодействие внутрисосудистых, сосудистых и внесосудистых факторов в развитии ПИВК схематично можно представить следующими образом.
Рис. 5. Схема патогенеза периинтравентрикулярных кровоизлияний (Volpe J.J., 2001).
Как видно, из приведенных выше фактов о патогенезе ПИВК, значительную роль в развитии геморрагий играют действия медицинского персонала, то есть ятрогенные факторы. В ниже приведенной таблице систематизированы механизмы действия ятрогенных факторов в развитии ПИВК.
|
|
Таблица 10 |
|
Ятрогенные факторы риска возникновения ПИВК |
|
|
|
|
|
Фактор риска |
Причина |
Флуктуация мозгового кровотока |
Неадекватная ИВЛ |
|
Повышение |
церебрального кровотока |
Болезненные манипуляции, санации трахеи, |
на фоне системной гипертензии |
пневмоторакс, высокая скорость инфузии, бы- |
|
|
|
строе введение коллоидов, закрытие артериаль- |
|
|
ного протока, гиперкарбия, судороги |
Повышение |
церебрального венозного |
Пневмоторакс, асфиксия в родах, синдром дыха- |
давления |
|
тельных расстройств |
Снижение церебрального кровотока |
Системная гипотензия (сепсис, гиповолемия) |
|
20
5.КЛИНИЧЕСКАЯ КАРТИНА
Вмеждународной классификации болезней Х пересмотра рассматриваются следующие степени поражений головного мозга в рубрике P52 – внутричерепное нетравматическое кровоизлияние у плода и новорожденного выделены:
Р52.0 внутрижелудочковое кровоизлияние I степени (субэпендимальное СЭК);
Р52.1 внутрижелудочковое кровоизлияние II степени (СЭК с распространением в желудочки);
Р52.2 внутрижелудочковое кровоизлияние III степени (СЭК с распространением в желудочки и ткани мозга).
Как видно из этой классификации, ПИВК разделены по степени распространенности, а не по клинической картине заболевания.
В клинической же картине ПИВК выделяют три типа течения заболевания: катастрофический; скачкообразный; клинически «немой».
Для катастрофического течения ПИВК характерно неумолимое прогрессирование симптоматики в течение минут или часов. Отмечается тяжелое угнетение сознание (ступор, кома); нарушения дыхания (нарушения ритма дыхания, гиповентиляция, апноэ); генерализованные тонические судороги (от 15 до 35% случаев); деребрационная поза; вялый тетрапарез; нарушения фотореакций, нарушения глазодвигательных реакций на вестибулярную стимуляцию) (Amiel C., 1964: Volpe J.J., 2001). Выше описанные признаки основного симптомокомплекса катастрофического течения ПИВК могут быть ассоциированы с рядом других клинических проявлений: выбухание родничка, брадикардия, артериальная гипотензия, нарушения терморегуляции; а также метаболическими расстройствами: снижением гематокрита, ацидозом, гипо- и гипергликемией, изменением объема циркулирующей жидкости, нарушением продукции антидиуретического гормона. Последовательность нарушений, по мнению J.J.Volpe (2001), обусловлена движением крови по желудочковой системе с закономерным вовлечением диэнцефальной области, среднего и продолговатого мозга и варолиева моста. В течение нескольких суток может развиться острая гидроцефалия и острой внутричерепной гипертензией, что было описано выше. При данном течении заболевания отмечается неблагоприятный прогноз и зависит от характера церебральных паренхиматозных изменений.
Скачкообразное течение ПИВК характеризуется беспорядочным развитием симптоматики. Наиболее типичными признаками данного течения ПИВК являются различные степени нарушения сознания, разнообразные качественные и количественные изменения спонтанной и вызванной двигательной активности, мышечная гипотония (особо значимо изменение подколенного угла), мягкие глазодвигательные нарушения (косоглазие, вертикальный парез взора, ограничение горизонтального движения глаз, феномен «кукольных глаз»). У 10% детей выявляется менингеальная симптоматика. Скачкообразность клинической картины может длиться сутки и более, прогноз при ней не столь пессимистичен
итакже зависит от поражения вещества головного мозга (Volpe J.J., 1978; Volpe J.J., 1979).
21
При клинически «немом» течении ПИВК неврологическая симптоматика может быть настолько мягкой, что иногда остается незамеченной. Только в 50% случаев по клинической симптоматика данной формы ПИВК было корректно предположено наличие кровоизлияния и в таких случаях решающее значение имела нейровизуализация (Lazzara A. и соавт., 1980). При «немом» течении ПИВК наиболее информативным признаком служит падение уровня гематокрита и недостаточный подъем уровня гематокрита после гемотрансфузии.
В соответствии с синдромологическим принципом, доминирующим в отечественной неонатальной неврологии, Неижко Л.Ю. и соавт. (1990) отмечают, что впервые сутки ПИВК у недоношенных детей преобладают явления угнетения (72% cлучаев), повышенная возбудимость выявляется в 15–22.6%, очаговая симптоматика – у 3.4%. В первые две недели синдром угнетения трансформируется в другие неврологические синдромы: повышенной нервно-рефлекторной возбудимости, двигательных расстройств, судорожный, вегетативновисцеральный.
По нашим наблюдениям, недоношенные дети, перенесшие одноили двухсторонние субэпендимальные кровоизлияния, в неонатальном периоде не имели специфических неврологических симптомов и диагноз основывался на нейросонографической картине.
У детей с ПИВК II степени на первом месяце жизни не отмечалось глубокого угнетения сознания (лишь в 10% случаев отмечалось угнетение сознания в виде комы до 4-го дня жизни с последующим восстановлением), отсутствовали судороги, однако в 15% случаев на первой неделе жизни выявлена повышенная двигательная активность с симптомами раздражения ЦНС (тремор конечностей, патологическая установка пальцев рук и ног, раздраженный плач). Изменение мышечного тонуса в виде гипотонии до 14 дня жизни отмечено в 75% случаев (с последующим восстановлением к 1 месяцу жизни). К концу 1-го месяца жизни в 41% случаев мы наблюдали гипертонус флексоров верхних конечностей. Вентрикулодилятация при ПИВК II степени развилась в 84% случаев, но большая часть детей не нуждалась в антидиуретической терапии или нейрохирургическом наблюдении. В 6% размеры желудочков значимо не увеличились при длительном наблюдении до 1 года жизни. Однако в 10% случаев мы наблюдали развитие выраженной гидроцефалии, требующей длительной терапии диакарбом, причем 1 ребенок из 12 детей с ПИВК II степени развил медленнопрогрессирующую окклюзионную гидроцефалию, потребовавшую проведения ликворошунтирующей операции.
ПИВК III и IV степени сопровождаются выраженной клинической симптоматикой в большинстве случаев. По нашим данным, среди детей с ПИВК III степени до 7-го дня жизни в 32% случаев наблюдалось угнетение сознания в виде комы, в 64% – угнетение в виде ступора; апноэ отмечено у половины детей. Судорожный синдром в первый месяц жизни в отмечен у 5 детей из 19 детей. При последующем наблюдении у всех детей с судорожным синдромом состоялся неблагоприятный неврологический исход: 1 ребенок сформировал детский церебральный паралич, 4 детей развили окклюзионную гидроцефалию (проведено вентрикулоперитонеальное шунтирование) и имели грубый невро-
22
логический дефицит. Изменения мышечного тонуса в неонатальном периоде у детей с ПИВК III степени отмечены в виде: мышечной гипотонии до 14 суток жизни у 62% новорожденных, к концу первого месяца жизни гипотония сохранялась у половины детей. У части детей (16% случаев) на 1-м месяце жизни выявлен гипертонус аддукторов и флексоров конечностей, что оказалось прогностически неблагоприятным фактором: эти дети к году имели грубую задержку моторного развития или ДЦП.
В группе детей с ПИВК IV степени в остром периоде мы наблюдали угнетение сознание в виде комы (у всех детей до 4-х суток жизни; в 50% случаев – до 14 суток жизни), судорожный синдром, сохраняющийся до 1 месяца жизни, отмечен в 75% случаев, и прогностически сопровождался неблагополучным исходом: ДЦП, окклюзионная гидроцефалия, грубая задержка психомоторного развития. Диффузная мышечная гипотония в первые 2 недели жизни отмечена в 70% случаев, до 1 месяца жизни – у половины детей. Гипертонус в нижних конечностях к 1 месяцу жизни выявлен в 30% случаев. У детей с односторонним ПИВК IV степени, у которых впоследствии развились гемипаретические формы детского церебрального паралича, на первом году жизни (до 8 10 месяцев), выявить асимметрию мышечного тонуса и рефлексов не удалось, что объясняется двухсторонним (контр- и ипсилатеральным) контролем центральных проводников движений на ранних стадиях онтогенеза (см. ниже).
Все дети с ПИВК III и IV степени развили вентрикулодилятацию различной степени: увеличение размеров боковых желудочков в сагиттальных срезах более 20 мм, при ПИВК IV степени визуализировались порэнцефалические кисты на месте паренхиматозного повреждения, формирующиеся к 4–6 неделям жизни. Впоследствии при нейросонографическом динамическом обследовании кисты «прорываются» в полость бокового желудочка, приводя к деформации контура желудочка. Окклюзионная гидроцефалия в нашем исследовании сформировалась с частотой 34%, остальные дети с ПИВК III и IV степеней имели статическую гидроцефалию, причем размеры желудочков сохранялись увеличенными в течение всего периода наблюдения (до 2-х летнего возраста) (Федо-
рова Л.А., 2003).
Как видно, из приведенных выше фактов, особое значение в клинической картине как острого, так и резидуального периодов ПИВК, приобретают гидро-
цефалия и вентрикулодилятация.
До настоящего времени, нет единства в терминологии относительно данного процесса и в профессиональном обиходе используют понятия «гидроцефалия», «вентрикулодилятация», «вентрикуломегалия». В целом, надо иметь в виду, что
гидроцефалия – это увеличение в объеме ликворных пространств с увеличением в них содержания церебро-спинальной жидкости. Вентрикулодилятация и вентрикуломегалия не подразумевают в своем определении какие-то изменения со стороны объема церебро-спинальной жидкости.
Причиной развития гидроцефалии вследствие ПИВК могут быть острая окклюзия отверстия Monroe сгустком крови, хроническое нарушение резорбции ликвора в задней черепной ямке и окклюзия сильвиева водопровода. Типичным для постгеморрагической гидроцефалии у недоношенных детей является разви-
23
тие в первые 3 недели после кровоизлияния, динамика соответствующая тяжести кровоизлияния, быстрый прирост окружности головы, клинические признаки внутричерепной гипертензии. Как правило, задние рога боковых желудочков увеличиваются в объеме раньше и в большей степени, чем передние рога. Острое развитие гидроцефалии, как правило, обусловлено окклюзией кровяным сгустком, подостро-хроническое – поражением пахионовых грануляций и нарушением резорбции церебро-спинальной жидкости в задней черепной ямке (Volpe J.J., 2001). На следующих рисунках представлены динамика состояния внутричерепного давления и размеров желудочков у 87 недоношенных новорожденных, перенесших ПИВК и механизмы постгеморрагической гидроцефа-
лии (Hill A. и соавт., 1981).
Как видно из представленных рисунков, в цепочке изменений состояний размеров желудочков и внутричерепного давления есть этап, при котором вентрикулодилятация не сопровождается внутричерепной гипертензией, то есть отмечается нормотензионная вентрикулодилятация.
При остро возникшей окклюзии, развивающейся в первые 2 недели после кровоизлияния, наблюдается выбухание родничка, расхождение швов, стремительный прирост окружности головы, симптом Грефе, а также ухудшение состояния в виде вялости, мышечной гипотонии, апноэ, судорожного синдрома. Клиническое ухудшение связано с дисфункцией ствола мозга за счет нарушения кровоснабжения ствола мозга вследствие ухудшения венозного оттока из задней черепной ямки (Шабалов Н.П., 2004)
По собственным данным в редких случаях отмечено появление пареза n.facialis. У младенцев с острой окклюзионной гидроцефалией судорожный синдром выявлен в 90% случаев, апноэ в 85%, трансформация мышечной гипотонии в раннем неонатальном периоде в мышечную гипертонию в конечностях к концу первого месяца жизни в 68%. (Федорова Л.А., 2003).
Вентрикулодилятация (вентрикуломегалия), то есть увеличение желудочков без повышения внутричерепного давления, может быть осложнением не только ПИВК, но также других поражений головного мозга, сопровождающихся атрофией мозгового вещества. Вентрикулодилятация повышает риск развития моторных и когнитивных нарушений у детей, поскольку сопровождается сочетанным повреждением не только белого, но и серого вещества мозга. В работе Kuban K. и соавт. (1999) представлены данные о том, что ПИВК и вентрикуломегалия (развившаяся как на фоне ПИВК, так и без него) сопровождаются повреждением белого вещества мозга (диагностика проводилась с помощью нейросонографии и определялось повышение эхоплотности или эхосвечения). В исследование включено 1605 детей с массой тела при рождении 500 1500 г, из которых у 129 (8%) выявлена высокая эхоплотность на нейросонограммах до 8 недель жизни. При статистическом анализе, показано, что риск повреждения белого вещества мозга у детей, перенесших ПИВК, увеличивается в 5 9 раз, а у детей имеющих вентрикуломегалию (с ПИВК или без них) в 18 29 раз по сравнению с недоношенными детьми, не имеющих указанных поражений.
Эти нарушения прослеживаются не только в грудном, но и в старшем возрасте. Исследования Stewart A. и соавт. (1996) продемонстрировали связь вен-
24