Материал: file000247
Во многих исследованиях показано, что гипотензия ассоциируется с ПИВК и ПВЛ у недоношенных детей, однако Watkins A.M.C. и соавт. (1989) выявили четкую связь системной гипотензии только с ПИВК, но не с ПВЛ, объясняя это феноменом реперфузии. К реперфузии, в частности, может приводить агрессивная медикаментозная коррекция гипотензии. Антонов А.Г. и соавт. (2001) показали, что использование у глубоконедоношенных детей таких препаратов, как дофамин, трентал, курантил, поддерживающих системное давление, может приводить к резким колебаниям церебрального кровотока, приводя к возникновению ПИВК. Так, даже диуретические дозы инотропов (дофамин) увеличивает в сердечный выброс в среднем на 30%.
Профилактика и лечение нарушений гемостаза проводится назначением свежезамороженной плазмы 10 мл/кг массы, что снижает частоту возникновения ПИВК с 41 до 14% (Beverley D.W. и соавт., 1985).
Медикаментозная терапия ПИВК является предметом противоречивых по своим результатам исследований.
Этамзилат – повышает целостность капилляров, в том числе в герминальном матриксе, а также является ингибитором синтеза простагландинов (способствуя закрытию ОАП). Влияет на микроциркуляцию за счет вазоконстрикии, повышения агрегации тромбоцитов. В мультицентровом исследовании, проведенном двойным слепым плацебо-контролируемым методом, было показано снижение частоты возникновения тяжелых ПИВК на 40% при применении этамзилата в группе детей с массой тела при рождении менее 1500 г. Однако при изучении отдаленного катамнеза детей в возрасте 3,5 4 лет не было получено достоверной разницы в развитии детского церебрального паралича и снижения когнитивного индекса по шкале McCarthy в обеих группах. (J. Schulte и соавт., 2005). В США препарат не используется у новорожденных с профилактической целью, в Великобритании этамзилат назначается недоношенным детям с ОНМТ в дозе 12,5 мг/кг в/м или в/в в течении 4 дней. В тех исследованиях, где показан позитивный эффект препарата, этот результат был получен при введении первой дозы от 1 до 4 часов сразу после рождения (Volpe J.J., 2001).
Назначение фенобарбитала аргументировалось возможностью барбитуратов снижать риск ПИВК опосредованно, влияя на системную артериальную гипертензию и моторную активность ребенка. Кроме того, фенобарбитал уменьшает капиллярный кровоток и интенсивность метаболизма мозга (блокада потока Na+ и Сl в нервную клетку, предотвращая ее повреждение). Однако результаты исследований не подтвердили необходимости использования препарата с профилактической целью (Whitelaw A., 1983). Более того, в работе Kuban K.C. и соавт. (1986) показано, что фенобарбитал незначительно повышает риск развития ПИВК.
Витамин Е ( -токоферола ацетат) является поглотителем свободных радикалов, защищая эндотелиальные клетки сосудов, в том числе герминального матрикса, от гипоксически-ишеического стресса, а также предотвращает повреждающее воздействие аниона супероксида, провоцирующего ПИВК в эксперименте (Ment L.R. и соавт., 1985; Poland R.L., 1990). В отношении данного препарата, как и в отношении ранее упомянутых средств, имеются противоре-
40
чивые сведения. Начальный оптимизм, связанный с трехкратным снижением развития тяжелых ПИВК после внутримышечного назначения витамина Е в первые 12 часов жизни (Chiswick M.L. и соавт., 1983), а также уменьшение частоты ПИВК любой степени тяжести (Kuban K. и соавт., 1986), сменился определенным скепсисом, обусловленным исследованием, показавшим повышение частоты возникновения ПИВК после назначения токоферола (Phelps D.L. и со-
авт., 1987).
Индометацин cнижает продукцию циклооксигеназы (простагландинсинтетазы), что используется в течение десятилетий в неонатологии с целью закрытия открытого артериального протока. Наряду с этим, снижая продукцию вазодилататора простациклина, индометацин уменьшает церебральный кровоток и его флюктуацию (Ment L.R., 1983). Показано, что назначение индометацина недоношенным новорожденным детям уменьшает интенсивность мозгового кровотока на 24%, что частично опосредовано закрытием открытого артериального протока (Pryds O. и соавт., 1988). Воздействуя, по своему основному механизму, на циклоксигеназу и снижая эндотелиальный воспалительный ответ, индометацин уменьшает активность фосфолипазы, поток Ca2+ в нервную клетку и активность свободных радикалов, осуществляя, таким образом, нейропротективный эффект (Pourcyrous M. и соавт., 1993). Вдобавок, индометацин ускоряет созревание и микроваскуляризацию сосудов герминального матрикса
(Ment L.R. и соавт., 1992).
Эффективность профилактики ПИВК с помощью индометацина доказана во многих исследованиях (Ment L.R. и соавт., 1985; Hanigan W.C. и соавт., 1988). Эти исследования подтверждают значительное снижение частоты развития ПИВК, в том числе и тяжелых, у недоношенных детей, получивших индометацин (Bada H.S., и соавт., 1989). Однако индометацин, влияя на периферическую сосудистую циркуляцию и оксигенацию за счет вазоконстрикции и приводя к гипоперфузии органов, может приводить к ряду побочных эффектов: почечной недостаточности, некротическому энтероколиту, перфорации кишечника. Тяжелые нарушения коагуляции рассматриваются как противопоказания к назначению индометацина, так как препарат влияет на функцию тромбоцитов. (Современная терапия в неонатологии, 2000). В системном обзоре и метаанализе P.W. Fowlie и соавт. (2003) доказана эффективность профилактического назначения индометацина для закрытия открытого артериального протока, снижения частоты возникновения ПИВК, в том числе тяжелых степеней. При метаанализе не было получено достоверного увеличения частоты некротически-язвенного энтероколита, олигурии, перфорации кишечника. Однако, при изучении отдаленного неврологического исхода (грубая задержка психомоторного развития, церебральный паралич, слепота и глухота) в группах детей, получивших индометацин и контрольной, не выявлено достоверной разницы. Показано, что индометацин имеет разную эффективность у мальчиков и девочек. Индометацин снижает смертность от ПИВК у мальчиков, а не у девочек (L. Ment и соавт.,
2004).
В настоящее время проводятся работы, по исследованию ибупрофена, не имеющего в отличие от индометацина, повреждающих эффектов на перифери-
41
ческую циркуляцию и оксигенацию. G Naulaers и соавт. (2005) с помощью спектроскопии было доказано, что ибупрофен не приводит к изменению объема церебрального кровотока, скорости церебрального кровотока и нарушению тканевой оксигенации.
Недоношенным со сроком гестации при рождении менее 32 недель, находящимся на ИВЛ, вводят 3 дозы индометацина по 100 мкг/кг массы внутривенно с интервалом 24 часа.
При установленном открытом артериальном протоке нагрузочная доза составляет 200 мкг/кг массы в/в однократно с последующим введением 5 доз по 100 мкг/кг с интервалом 24 часа. (Шабалов Н.П., 2004). Противопоказаниями к введению индометацина являются кровотечения, снижение уровня тромбоцитов менее 80000 мм-3, признаки некротически-язвенного энтероколита, повышение уровня креатинина в крови более 1,6 мг/децилитр, олигурия менее 0,5 мл/час в первые сутки после введения препарата.
7.3. Лечение и профилактика окклюзионной гидроцефалии
Консервативное лечение диакарбом, который снижает продукцию ликвора в сосудистых сплетениях, ингибируя карбангидразу, и фуросемидом, увеличивающим активный транспорт путем реабсорбции Na+ и Cl в проксимальной части петли Генле, в настоящее время подвергнуты ревизии. В обзоре Whitelaw A. и соавт. (2004) проанализированы результаты лечения с помощью диуретиков (диакарб или фуросемид или их сочетание), детей с постгеморрагической гидроцефалией по следующим направлениям: потребность в вентрикулоперитонеальном шунтировании или наружном вентрикулярном дренаже, вентрикулостомии, резервуара; летальные исходы в возрасте 1 3 лет; наличие грубого моторного дефицита в возрасте и грубой задержки умственного развития в этом же возрасте. На фоне проводимой диуретической терапии оценены следующие показатели: потребность в люмбальных, вентрикулярных пункциях, а также такие осложнения терапии, как биохимические нарушения (ацидоз, электролитные расстройства), нефрокальциноз. Представленные результаты можно систематизировать следующим образом:
1.Летальный исход: мета-анализ не выявил значимых влияний диуретиков на смертность детей до 3 лет.
2.Вентрикуло-перитонеальное шунтирование: необходимость в постановке шунта не уменьшалась в группе детей, получивших диуретики.
3.Другие нейрохирургические вмешательства (наружный дренаж, вентрикулярный резервуар): потребность одинакова в основной и контрольной группах.
4.Моторные нарушения к возрасту 1 года среди выживших недоношенных: моторные нарушения развивались чаще у детей, пролеченных диуретиками.
5.Задержка умственного развития (в сочетании с моторным дефицитом): была чаще в группе пролеченных диуретиками детей.
6.Осложнения диуретической терапии: у части детей лечение диуретиками было прекращено из-за развития электролитных нарушений, ацидоза.
42
7. Нефрокальционоз: формировался достоверно чаще – показано, что в группе детей, пролеченных диуретиками.
Побочные эффекты диуретиков в виде летаргии, ацидоза, водных, электролитных и почечных расстройств, а также изменения церебрального кровотока диктуют осторожность при их выборе. Кроме того, у недоношенных детей с идиопатическим апноэ использование диакарба значительно снижает pH и pCO2 (и при этом без эффективности лечения апноэ). У детей, имеющие гидроцефалию на фоне бронхо-легочной дисплазии при назначении диакарба развивается гипрекарбия и увеличение скорости церебрального кровотока, что, как это было уже показано, крайне не благоприятно для детей нарушениями ауторегуляции церебральной перфузии.
Таким образом, назначение диакарба и/или фуросемида не эффективно для лечения постгеморрагической гидроцефалии, не уменьшает потребность в частоте ВПШ, но увеличивает риск таких осложнений, как нефрокальциноз и биохимические расстройства.
В исследовании Whitelaw A. и соавт. (2007) обследовано 70 недоношенных детей со сроком гестации 24 34 недели с прогрессирующей постгеморрагической вентрикулодилатацией. Поскольку лечение постгеморрагической гидроцефалии на ранних этапах с помощью шунтирования практически невозможно из-за высокого содержания крови и белка в церебро-спинальной жидкости в остром периоде, авторы попытались использовать различные профилактические меры для снижения частоты осложнений массивных ПИВК. Были оценены результаты лечения в 2 группах детей с массивными ПИВК с помощью различных методик: в I группе детям был налажен наружный вентрикулярный дренаж, через который осуществлялась фибринолитическая терапия (рекомбинантный тканевой активатор плазминогена), с профилактической целью вводились антибиотики (ванкомицин и гентамицин), а также проводилась ирригация с целью быстрейшей санации ликвора. Дети II группы получали стандартное лечение (лечебно-диагностические люмбальные пункции), а при прогрессировании гидроцефалии следовала постановка резервуара Оммая. Результаты свидетельствуют, что фибринолитическая терапия, санационное «промывание» желудочков не улучшает прогноз и не уменьшает потребность в вентрикулоперитонеальном шунтировании.
Использование серийных «разгрузочных» или «санационных» люмбальных пункций для профилактики окклюзионной гидроцефалии не показало должной эффективности (Mantovani J.F., 1980). Серийные вентрикулярные пункции при наличии разобщения церебральных и спинальных пространств опасны риском повторного кровоизлияния, возникновением постпункционных порэнцефалических кист, а также неконтролируемыми потерями электролитов и белков. Одним из методов лечения окклюзии является вентрикулосубгалеальное дренирование с помощью резервуар-катетера (Иова А.С., 2003) (Иова А.С. 2003, патент на изобретение №2240151 «Устройство для дренирования внутричерепных полостей») с целью временного дренирования желудочков (отведение жидкости из желудочка мозга в «субгалеальный карман» полость между надкостницей и апоневрозом), продолжающегося до санации церебро-cпинальной жидкости
43
(в среднем 1,5 месяца). После лизиса свертков крови в желудочках проводится тест на «проходимость ликворных путей» с обязательным динамическим нейросонографическим исследованием. При имеющихся признаках окклюзии ребенку выполняют II этап нейрохирургического лечения – вентрикулоперитонеальное шунтирование с отведением избыточной церебро-спинальной жидкости в брюшную полость.
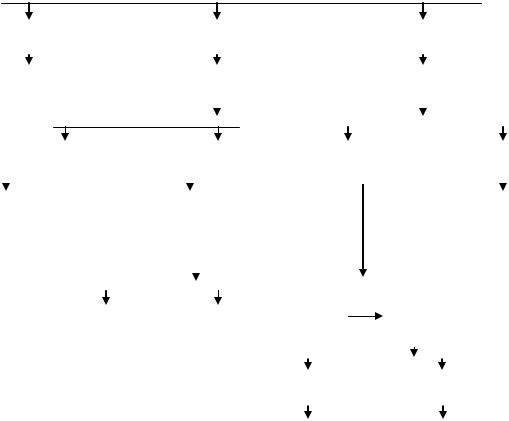
Схема ведения недоношенных детей с ПИВК систематизированы J.J.Volpe (1995) (рис. 13)
Внутрижелудочковые кровоизлияния герминального матрикса
Непрогрессирующая |
Медленно прогрессирующая |
Быстро прогрессирующая |
||||||||||
вентрикулодилатация |
вентрикулодилатация |
|
вентрикулодилатация |
|||||||||
Без дальнейшего |
Наблюдение в течение |
|
Серийные люмбальные |
|||||||||
лечения |
|
4 недель |
|
|
|
|
|
пункции (?) |
||||
|
|
|
|
|
|
|
|
|
|
|||
Прекращение |
Продолжающаяся |
|
|
Продолжающаяся |
Остановка |
|||||||
дилатации |
дилатации |
|
|
дилатации |
дилатации |
|||||||
Без дальнейшего |
Серийные люмбальные |
|
|
Без дальнейшего |
||||||||
лечения. |
пункции |
|
|
|
|
|
|
лечения. |
||||
Наблюдение 1 год |
+/- медикаментозная |
|
|
Наблюдение 1 год |
||||||||
|
|
|
терапия |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Прекращение |
Продолжающаяся |
|
Вентрикулярный |
|||||||||
дилатации |
дилатация |
|
дренаж |
|||||||||
|
|
|
|
|
||||||||
Без дальнейшего |
Продолжающаяся |
Прекращение |
||||||||||
лечения. |
|
|
дилатация |
|
|
дилатации |
||||||
Наблюдение 1 год. |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
Вентрикуло- |
|
Без дальнейшего |
|||||
|
|
|
|
перитонеальный |
|
лечения. |
||||||
|
|
|
|
|
|
шунт |
|
Наблюдение 1 год. |
||||
Рис.13. Схема рациональной последовательности менеджмента недоношенных детей с внутрижелудочковыми кровоизлияниями (Volpe J.J., 1995).
8. ПРОГНОЗ
Прогноз развития детей с ПИВК зависит от ряда факторов, и в частности, от механизма повреждения мозга, наиболее важными являются первичный гипок- сически-ишемический инсульт, постгеморрагическая гидроцефалия и перивентрикулярный геморрагический инфаркт. Тщательная оценка результатов ультразвукового исследования является важным прогностическим знаком. Краткосрочный прогноз при ПИВК связан с тяжестью кровоизлияния и при ПИВК III степени в 10% приводит к летальному исходу, в 20% к развитию гидроцефа-
44