Материал: Черешнев ВА, Шилов, Черешнева. Экспериментальные модели в патологии
|
|
|
|
|
|
|
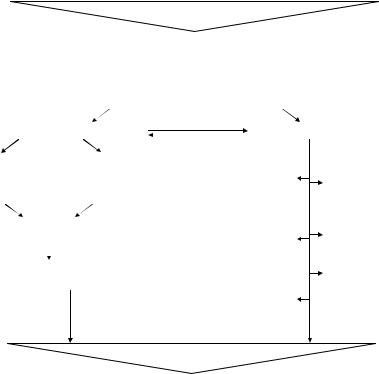
ПРОНИКАЮЩЕЕ РАНЕНИЕ ГЛАЗА |
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
РЕГУЛЯТОРНЫЕ СИСТЕМЫ ОРГАНИЗМА |
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
нервная |
|
|
эндокринная |
|
иммунная |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
ПРОФЕТАЛЬ |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
ТРАВМАТИЧЕСКИЕ ИЗМЕНЕНИЯ |
|
|
|
|
|
|
СТРЕССОРНЫЕ ИЗМЕНЕНИЯ |
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
СТИМУЛЯЦИЯ |
|
|
СНИЖЕНИЕ |
|
|
ТОРМОЖЕНИЕ ПОЗДНЕЙ |
|
|
АКТИВАЦИЯ ФАГОЦИТАРНОЙ |
|||||||||||||
ПРОЛИФЕРАЦИИ КЛЕ- |
|
ФОРМИРОВАНИЯ |
|
|
СТИМУЛЯЦИИ РЕАКЦИИ |
|
|
АКТИВНОСТИ МОНОЦИТОВ |
||||||||||||||
ТОК МНОГОСЛОЙНОГО |
|
ГРУБОЙ РУБЦОВОЙ |
|
|
ГИПЕРЧУВСТВИТЕЛЬНОСТИ |
|
|
ПЕРИФЕРИЧЕСКОЙ КРОВИ |
||||||||||||||
ПЛОСКОГО ЭПИТЕЛИЯ |
|
|
ТКАНИ |
|
|
ЗАМЕДЛЕННОГО ТИПА |
|
|
И ПЕРИТОНЕАЛЬНЫХ |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
МАКРОФАГОВ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
УСКОРЕНИЕ ЭПИТЕЛИЗАЦИИ |
|
|
|
ТОРМОЖЕНИЕ ПОЗДНЕЙ |
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
АКТИВАЦИЯ NK-КЛЕТОК |
||||||||||||||
|
|
ЗОНЫ ПОВРЕЖДЕНИЯ |
|
|
|
|
|
СТИМУЛЯЦИИ |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
АНТИТЕЛООБРАЗОВАНИЯ |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
ОПТИМИЗАЦИЯ |
|
|
|
|
|
|
|
|
|
|
|
|
АКТИВАЦИЯ СОЗРЕВАНИЯ |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
РЕПАРАТИВНОЙ РЕГЕНЕРАЦИИ |
|
|
|
СНИЖЕНИЕ УРОВНЯ |
|
|
|
ДЕНДРИТНЫХ КЛЕТОК |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
АНТИТЕЛ К АНТИГЕНАМ |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ГЛАЗА |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
ОПТИМИЗАЦИЯ ТЕЧЕНИЯ ВОСПАЛЕНИЯ |
|
|
|
|||||||||||||
Рис. 33. Механизм действия профеталя в патогенетической терапии проникающего ранения глаза
используются не только энергия, полученная в ходе катаболизма, но и указанные строительные блоки.
Разделение отдельных метаболических путей на процессы углеводного, липидного, аминокислотного и др. обменов весьма ус ловно, так как в организме они тесно взаимосвязаны как на уровне общего энергообеспечения клетки, так и на уровне общих ключевых метаболитов. Взаимосвязь на уровне общего энергообеспечения пред полагает конкуренцию разных метаболических путей за источники энергии. Поэтому, если в организме происходит, например, синтез триацилгицеролов в жировой ткани, этот процесс параллельно сопро вождается окислением в той же ткани глюкозы, которая обеспечивает синтез жира как энергетически за счет образования АТФ и НАДФН+H+, так и пластически – за счет образования ацетил-КоА. Таких примеров можно приводить множество. Но главная особенность
– это тесная координация различных метаболических путей в зависи мости от конкретного физиологического состояния организма.
Координация разных метаболических путей в организме носит многоуровневый характер. На уровне отдельных клеток, тканей и ор ганов регуляция отдельных метаболических путей осуществляется, во первых, по механизму положительных и отрицательных обратных свя зей метаболитами, которые могут выступать в роли аллостерических активаторов или ингибиторов отдельных ключевых ферментов, либо конкурентных ингибиторов – механизмы, хорошо изложенные в кур сах биохимии; во-вторых, наш организм унаследовал и такие филоге нетически древние механизмы регуляции, играющие очень важную роль у бактерий, как регуляцию на генетическом уровне (или на уров не транскрипции) синтеза тех или иных ферментов метаболитами. Пример – активация в печени синтеза глюкуронилтрансферазы, фер ментов микросомального окисления как эндогенными токсическими веществами, так и экзогенными – этанолом, барбитуратами, многими лекарственными препаратами. Однако на уровне целого организма ведущая роль принадлежит нейроэндокринным механизмам. Гормоны участвуют в регуляции метаболических путей, во-первых, за счет из менения активности отдельных ферментов, во-вторых, за счет регуля ции их синтеза на генетическом уровне, в-третьих, за счет изменения проницаемости клеточных мембран для ключевых метаболитов угле водного, жирового и аминокислотного обменов. Эти механизмы дей ствия гормонов во многом реализуются через внутриклеточные сиг нальные пути, связанные с образованием циклических нуклеотидов, инозитолтрифосфата, диацилглицерола и других посредников, в ре
286
зультате чего образуются активные протеинкиназы, которые фосфори лируют различные белки. В качестве последних могут выступать фер менты (ковалентная активация или ингибирование ферментов за счет присоединения фосфорной кислоты), ядерные факторы и регулятор ные белки хромосом (изменения биосинтеза белков и ферментов на генетическом уровне), белки рибосом (изменение биосинтеза белка на уровне трансляции), белки мембран (изменения проницаемости кле точных мембран для ключевых метаболитов углеводного, жирового, аминокислотного обменов).
Следует подчеркнуть, что сами ключевые метаболиты активно участвуют в регуляции обмена веществ по принципу обратных связей на многих уровнях нейроэндокринной системы. К таким ключевым метаболитам, концентрация которых поддерживается в узких гомео статических пределах, относится в углеводном обмене глюкоза крови (концентрация натощак – 3,33–5,55 ммоль/л). Внутриклеточно она всегда представлена в виде другого ключевого или центрального ме таболита всего углеводного обмена – глюкозо-6-фосфата. Если рас сматривать регуляцию обмена веществ с позиций функциональной системы П. К. Анохина, то именно уровень глюкозы в периферической крови – это наиболее важный сигнал, изменяющий по принципу об ратной афферентации весь метаболизм. Действие и восприятие этого сигнала в нейроэндокринной системе носит многоуровневый характер.
Во-первых, повышение концентрации глюкозы приводит не посредственно на уровне -клеток поджелудочной железы к усилению синтеза и секреции инсулина (рис. 34). Этот эффект связывают, преж де всего, с регуляцией глюкозой экзоцитоза содержащих инсулин гра нул β-клеток. Глюкоза проникает через наружную мембрану β-клеток с помощью белка GLUT2, транспортирующего глюкозу. У мышей с генетическим дефектом GLUT2 развивается гипергликемия и гипоин сулинемия, сопровождающаяся нарушением первой фазы секреции инсулина. Степень выраженности секреции инсулина β-клетками на ходится в прямой зависимости от уровня метаболизма в них глюкозы. Лимитирующим ферментом скорости катаболизма глюкозы в клетках является глюкокиназа, катализирующая превращение глюкозы в глюкозо-6-фосфат (во многих других клетках эта реакция катализи руется преимущественно гексокиназой). Доказано, что выраженность экзоцитоза гранул и высвобождения инсулина определяется концен трацией в -клетках промежуточных метаболитов обмена глюкозы, в частности пирувата и фосфоенолпирувата (метаболиты гликолиза), а также отношениями концентраций АТФ/АДФ и НАДФH+H+/НАДФ+.
287
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ca2+ |
|
|
|
|
|
|
Аргинин |
|
KАТФ- |
|
|
|
|
|
|
|
|
|
|
|
|
Потенциал- |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
каналы |
|
|
|
|
|
|
|
|
|
|
зависимые |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ca2+-каналы |
|
||
Лейцин |
|
|
|
|
|
|
|
|
|
|
-K+ |
Vm |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
+ |
|
Глюкагон, GLP1, GIP |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
НАДФ+ |
- |
|
|
|
Gs АЦ |
|
Симпатическая |
||||||||||||||
|
|
|
|
|
|
|
|
|
нервнаясистема |
|||||||||||||||||
|
|
|
Пентозный |
- |
|
+ Ca |
2+ цАМФ |
|
Катехоламины |
|||||||||||||||||
GLUT2 |
цикл |
|
|
|
|
|
|
|
|
|
|
|
Gi АЦ |
|
Парасимпатическая |
|||||||||||
|
|
|
|
|
|
|
|
|
|
PKA |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
цАМФ |
нервнаясистема |
|||||||||
Глюкоза |
|
|
Гл6ф |
НАДФН+Н |
|
|
|
|
|
|
|
|
Ацетилхолин |
|||||||||||||
|
|
|
АТФ/АДФ |
Ca2+ |
|
|
IP3 |
|
||||||||||||||||||
|
|
|
|
|
PIP2 |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
Пируват |
|
|
|
|
|
|
|
|
|
|
|
|
|
PLC |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
Ацетил-КоА |
|
|
|
PKC |
|
|
DAG |
PI3K |
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
ЦиклКребса |
|
|
|
|
|
|
|
|
|
|
|
|
|
IRS |
Рецепторк |
|||||||
|
|
|
|
Тканевое дыхание |
|
|
|
|
|
|
|
|
|
инсулину |
||||||||||||
|
|
|
|
Окислительное |
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|||||||||
|
|
|
|
фосфорилирование |
|
|
|
|
|
Akt |
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Инсулин |
||||||
Митохондрии
 Экзоцитозивысвобождение инсулинаизклетки
Экзоцитозивысвобождение инсулинаизклетки
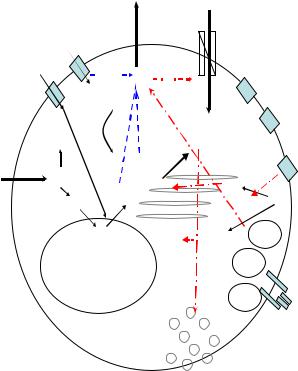
Рис. 34. Регуляция синтеза и секреции инсулина -клетками поджелудочной железы:
Гл6ф – глюкозо-6-фосфат, АЦ – аденилатциклаза, цАМФ – циклический АМФ, Vm – деполяризация или гипополяризация мембраны, Gs – G-протеин, активирующий адени латциклазу, Gi – G-протеин, ингибирующий аденилатциклазу, – повышение уровня,
– снижение уровня, PKA – протеинкиназа А, PKC – протеинкиназа C, PIP2 – фосфатиди линозитол-4,5-дифосфат, IP3 – инозитол-1,4,5-трифосфат, DAG – диацилглицерол, PLC – фосфолипаза C, PI3K – фосфатидилинозитол-3-киназа, IRS – субстрат рецептора к инсу лину (англ. insulin receptor substrate), Akt – `Akt-киназа (синоним: протеинкиназа B), GLUT2 – белок, транспортирующий глюкозу (англ. glucose transporter 2), GLP1 – глюка гоноподобный пептид-1 (англ. glucagon-like peptide-1; синоним: энтероглюкагон), GIP – глюкозозависимый инсулинотропный пептид (синонимы: гастроингибиторный пептид, гастроингибиторный полипептид), пунктирные линии без точки – закрытие каналов, пунктирные линии с точкой – активация процесса или открытие каналов, сплошные линии – последовательность реакций метаболизма и сигнальных путей
288
Для поиска новых антидиабетических препаратов существенны иссле дования последних лет роли в высвобождении инсулина -клетками пируват-цитратного, пируват-малатного и/или пируват-изоцитратного циклов, а также участия длинноцепочечных жирных кислот в качестве эндогенных лигандов ядерных рецепторов PPARs (англ. peroxisome- proliferator-activated receptors), которые на внутриклеточном уровне функционируют как сенсоры в регуляции обмена липидов на уровне изменения экспрессии генов. Показано, что увеличение уровня АТФ приводит к закрытию АТФ-зависимых SUR1/Kir6.2 калиевых каналов (KАТФ-каналов), что ведет к деполяризации мембраны. Деполяризация вызывает открытие потенциал-зависимых кальциевых каналов, что приводит к повышению проникновения Ca2+ в клетку. Увеличение уровня Ca2+ в клетке активирует фосфолипазу C, которая расщепляет фосфатидилинозитол-4,5-дифосфат на инозитол-1,4,5-трифосфат и диацилглицерол. Инозитолтрифосфат связывается с рецепторными белками эндоплазматического ретикулума. Это приводит к высвобож дению связанного внутриклеточного Ca2+ и резкому повышению его концентрации. Значительное увеличение концентрации в клетке Ca2+ приводит к высвобождению заранее синтезированного инсулина, хра нящегося в секреторных гранулах. Увеличение уровня НАДФH+H+, образующегося в пентозном цикле, приводит как к прямому увеличе нию экзоцитоза содержащих инсулин гранул, так и к усилению Ca2+- и АТФ-зависимого ответа за счет удлинения времени инактивации по тенциал-зависимых K+-каналов, реполяризующих клеточную мембра ну после ее деполяризации закрытием KАТФ-каналов. Гормоны и ме диаторы, повышающие уровень внутриклеточного циклического АМФ (цАМФ), также повышают секрецию инсулина β-клетками. Увеличе ние концентрации цАМФ приводит к повышению уровня внутрикле точного Ca2+ как непосредственно через активацию L-типа кальциевых каналов, так и через активацию протеинкиназы А. Последняя фосфо рилирует и закрывает KАТФ-каналы, что приводит к деполяризации плазматической мембраны. Помимо этого цАМФ повышает чувстви тельность внутриклеточных компонентов, ответственных за секрецию инсулина, к уровню внутриклеточного Ca2+, в результате чего Ca2+ индуцированная секреция усиливается при более низкой концентрации Ca2+. Протеинкиназа А также быстро фосфорилирует белки, ответст венные за секрецию инсулина. Наконец, цАМФ стимулирует экспрес сию инсулиновых генов как непосредственно за счет связывания с цАМФ-отвечающими элементами или CRE (англ. cAMP response elements) промотора инсулинового гена, так и опосредованно – за счет фосфорилирования транскрипционного фактора CREB (англ. cAMP
289