Материал: Черешнев ВА, Шилов, Черешнева. Экспериментальные модели в патологии
Большинство факторов свертывания синтезируется в печени. В зависимости от участия витамина K в этом процессе их разделяют на две группы:
1)витамин-K-зависимые – ф. II, VII, IX, X;
2)витамин-K-независимые – ф. I, V, XI – их образование не требует витамина K.
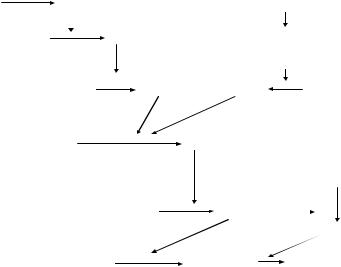
Процесс свертывания крови проходит три фазы, при этом су ществует два механизма активации коагуляционного каскада – внут ренний и внешний (рис. 28).
Внутренний |
|
|
Внешний путь |
|
путь |
|
|
свертывания |
|
свертывания |
|
крови |
||
крови |
|
|
Повреждение |
|
XII |
XIIa |
|
||
|
тканей |
|
||
XI |
XIa |
|
III (тканевый |
|
|
|
|
фактор), Ca2+ |
|
|
IX |
IXa |
VIIa |
VII |
Тромбоцитарный |
|
|
|
|
фактор 3, Ca2+, VIIIa |
|
|
|
|
|
X |
|
Xa |
|
|
Тромбоцитарный |
|
XIII |
|
|
фактор 3, Ca2+, |
|
||
|
Va |
|
|
|
|
II (протромбин) |
IIa (тромбин) |
|
|
|
|
|
|
XIIIa |
I (фибриноген) |
|
Is (фибрин |
Ii (фибрин |
|
|
|
|
растворимый) |
нерастворимый) |
Рис. 28. Схема коагуляционного гемостаза
Выделяют следующие фазы свертывания крови.
I фаза – образование активного кровяного тромбопластина.
IIфаза – превращение протромбина в тромбин. III фаза – превращение фибриногена в фибрин.
255
I фаза. Во внутреннем механизме пусковым фактором являет ся фактор XII (фактор контакта, фактор Хагемана), активация которо го происходит вследствие контакта крови с базальной мембраной со судов при их повреждении. Кроме того, активация этого фактора мо жет осуществляться с помощью его ферментативного расщепления (калликреином, плазмином). В свою очередь, фактор XII является уни версальным активатором всех плазменных протеолитических систем: свертывающей, калликреин-кининовой, фибринолитической и систе мы комплемента. XIIa-фактор последовательно активирует XI и IX факторы. Последние два активируют фактор X, при этом действие фактора IX на фактор X усиливается в несколько тысяч раз фактором VIII. Фактор V и пластиночный фактор 3, играющий роль фосфоли пидной матрицы, в совокупности повышают активность кровяного тромбопластина (фактора Ха) в 300000 раз. Образованием активного кровяного тромбопластина (протромбиназы) заканчивается I фаза внутреннего механизма коагуляционного гемостаза. Внешний механизм свертывания крови стимулируется поступлением в плазму из по врежденных тканей тканевого тромбопластина (ф. III), превращающе го фактор VII в VIIа, который активирует фактор X. На образовании фактора Ха смыкаются внешний и внутренний пути активации коагу ляционного гемостаза. II и III фазы свертывания крови являются об щими.
II фаза. Фактор Ха последовательно отщепляет от фактора II (протромбина) 2 фрагмента, превращая его в фактор IIа (тромбин); его образование является итогом этой фазы.
III фаза. Тромбин отщепляет от молекулы фактора I (фибри ногена) четыре пептида, превращая его в мономеры фибрина, которые полимеризуются с образованием растворимого, а затем нерастворимо го фибрин-полимера под влиянием фактора XIII (фибринстабилизи рующего), активируемого тромбином.
Противосвертывающая (антикоагулянтная) система
Свертыванию крови противодействует противосвертывающая система, которая включает в себя первичные и вторичные антикоагу лянты.
Первичные антикоагулянты
1.Гепарин – гетерополисахарид, образующийся во всех орга нах и тканях; наибольший синтез его происходит в легких и печени. Гепарин тормозит все три фазы свертывания крови.
2.Антитромбин III – универсальный антикоагулянт. На его долю приходится более 75% всей антикоагулянтной активности плаз
256
мы, причем без должного уровня этого белка гепарин не работает. При снижении количества антитромбина III возникает тяжелое тромбофи лическое состояние, характеризующееся рецидивирующими тромбо зами магистральных вен конечностей и внутренних органов, тромбо эмболиями легочной артерии, инфарктами органов. При уровне анти тромбина ниже 30% больные часто погибают в молодом возрасте от тромбоэмболии. Скрытая наклонность к тромбозам возникает при снижении антитромбина ниже 70%.
3. Протеин C – инактиватор неферментных факторов сверты вания (ф. VIII и ф. V); его кофактором является протеин S. На долю системы протеина C приходится около 15% антикоагулянтной актив ности плазмы.
Вторичные антикоагулянты
Вторичные физиологические антикоагулянты образуются в процессе свертывания крови и фибринолиза в результате дальнейшей ферментативной деградации ряда факторов свертывания крови.
1.Фибрин. Адсорбирует и инактивирует большое количество тромбина, т.е. является как фактором свертывания, так и антикоагу лянтом, обозначается как антитромбин I.
2.Продукты деграции фибриногена/фибрина. Образуются в результате фибринолиза, оказывают влияние на проницаемость и то нус кровеносных сосудов, свойства эндотелия, ингибируют агрегацию тромбоцитов и самосборку мономеров фибрина, т.е. действуют как антиагреганты и антикоагулянты, тормозят фибринолиз, активируют макрофаги.
3.Тромбин. Способен превращаться из основного фактора свертывания крови в активатор важнейшего противосвертывающего механизма. Значительная часть тромбина, образующегося при актива ции свертывающей системы крови, связывается с тромбомодулином сосудистой стенки и утрачивает при этом способность вызывать обра зование фибрина и активировать фактор XIII. Вместе с тем, такой за блокированный тромбомодулином тромбин сохраняет способность активировать систему важнейших антикоагулянтов – протеинов C и S.
Фибринолитическая (плазминовая) система
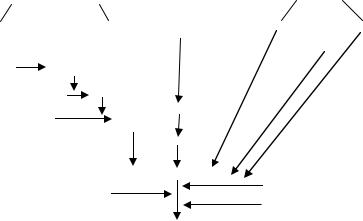
Ферментная система, вызывающая расщепление фибри на/фибриногена на все более и более мелкие фрагменты, обозначается как фибринолитическая или плазминовая система (рис. 29). Главным компонентом этой системы является фермент плазмин (фибриноли зин), содержащийся в плазме в виде профермента – плазминогена. Ак тивный плазмин быстро блокируется антиплазминами и элиминирует-
257
|
Внутренний |
Внешний |
||||||
|
механизм |
|
|
|
|
механизм |
||
|
|
|
|
|
|
|
||
|
|
|
|
|
||||
Фактор XII |
|
Фактор XII |
Эндотелиальные Из Тканевые |
|||||
|
|
|
|
|
|
|
клеток |
|
(Хагеман)- |
|
(Хагеман) |
||||||
|
крови |
|||||||
зависимый |
|
независимый |
||||||
|
|
|
||||||
XII |
XIIa |
|
|
|
|
|
|
|
Прекалликреин |
Калликреин |
|
|
|||||
ВМ кинино |
|
ВМ Проактиватор |
||||||
ген |
|
|
кининАктиватор |
|
|
|||
|
ПЛАЗМИНОГЕН |
Антиплазмины I ряда |
Ингибитор |
|
|
|
Ингибиторы II ряда |
|
трансформации |
|
ПЛАЗМИН
Рис. 29. Схема фибринолиза
ся из кровотока. В организме активация фибринолиза может осущест вляться двумя путями.
Внутренняя активация фибринолиза осуществляется двумя механизмами: Хагеман-зависимый фибринолиз, который обусловлива ется активированным фактором XII в комплексе с калликреином и высокомолекулярным кининогеном, и Хагеман-независимый фибри нолиз, при котором плазминоген активируется активаторами, цирку лирующими в крови. На долю Хагеман-зависимого фибринолиза при ходится 75% фибринолитической активности плазмы крови.
Внешняя активация фибринолиза осуществляется в основном синтезируемым в сосудистом эндотелии белковым активатором ткане вого типа (тканевым активатором плазминогена). Его интенсивный выброс происходит при всех видах закупорки сосудов, физических нагрузках, под влиянием вазоактивных веществ и ряда лекарственных препаратов (никотиновой кислоты, адреналина, норадреналина, анало гов вазопрессина и др.). Мощные активаторы плазминогена содержат ся в эритроцитах, тромбоцитах, лейкоцитах. Гранулоциты и макрофа ги могут секретировать внутриклеточные киназы, которые сами по себе, без участия плазмина, расщепляют фибрин. Активаторы плазми ногена содержатся также в различных тканях, экскретах и секретах (моче, желчи, молоке, слюне).
258
Методы исследования состояния системы гемостаза
Долабораторная оценка состояния системы гемостаза при геморрагических диатезах по типу кровоточивости
1.Петехиально-пятнистый – (синячковый, микроциркулятор ный) характерен для тромбоцитопений, тромбоцитопатий, болезни Виллебранда.
2.Гематомный – типичен для гемофилии, характеризуется болезненными напряженными кровоизлияниями в мягкие ткани и сус тавы.
3.Смешанный синячково-гематомный – характерен для ДВС синдрома, тяжелого дефицита факторов протромбинового комплекса, тяжелой формы болезни Виллебранда, передозировки антикоагулян тов и фибринолитиков.
4.Васкулитно-пурпурный – характеризуется геморрагиями в виде сыпи или эритемы на воспалительной основе, наблюдается при инфекционных и иммунных васкулитах.
5.Ангиоматозный – наблюдается при телеангиэктазиях, ан
гиомах.
Лабораторные исследования состояния системы гемостаза
Исследование сосудисто-тромбоцитарного гемостаза
1.Время кровотечения (проба Дьюка). Норма – 2–5 мин. Уд линение времени капиллярного кровотечения наблюдается при тром боцитопениях, тромбоцитопатиях, болезни Виллебранда.
2.Количество тромбоцитов. Норма – 180–360 109/л.
3.Резистентность капилляров (манжеточная проба). Увеличе ние количества петехий на участке кожи в зоне наложения манжеты тонометра больше допустимого по методике свидетельствует о пони жении резистентности сосудистой стенки и характерно для тромбоци топений, тромбоцитопатий и вазопатий.
4.Агрегация тромбоцитов. Оценка проводится с помощью агрегометра. Повышение агрегационной активности тромбоцитов ха рактерно для претромботических состояний, идиопатического тром боцитоза, тромбозов, инфарктов органов, атеросклероза, васкулитов, беременности. Снижение агрегации наблюдается при тромбоцитопа тиях (тромбастении Гланцмана, болезни Бернара-Сулье).
5.Ретракция кровяного сгустка. В норме сгустки крови начи нают сжиматься через 30–60 мин. Отсутствие ретракции сгустка на блюдается при выраженных тромбоцитопениях и тромбоцитопатиях.
259