Материал: Черешнев ВА, Шилов, Черешнева. Экспериментальные модели в патологии
и изменения жизненно важных параметров среды, например гипоксия, нарушения кислотно-щёлочного равновесия и температурного режи ма; паразитирование со стороны вирусов и других внутриклеточных организмов. Все эти факторы способны повреждать клетку непосред ственно и являются повреждающими агентами по определению.
Во-вторых, это действие на клетку, а точнее на клеточные ре цепторы, молекул, несущих информацию о возможности повреждения. Эти молекулы «предупреждают» клетку о наличии микроорганизмов или иных факторов, представляющих потенциальную опасность. По средством контакта обозначенных молекул с рецепторами клетка рас познает принципиальный образ опасных для неё явлений. Молекуляр ная основа подобного распознавания – взаимодействие рассмотренных в гл. XVI паттерн-распознающих рецепторов (PRR) с PAMP и/или DAMP. В качестве PAMP выступают консервативные структуры мик роорганизмов, не имеющие строгой видовой специфичности, а DAMP
– молекулы эндогенного происхождения, свидетельствующие о нали чии тканевого повреждения: продукты деградации коллагена, некото рые ядерные белки, фрагменты РНК и ДНК, мембранные фосфолипи ды, тканевой фактор и ряд других продуктов повреждения клеток и межклеточного матрикса. Эндогенные молекулы-паттерны являются для клеток маркерами продуктов тканевой деградации и, следователь но, информируют их через PRR о повреждении других клеток. Прак тически любая клетка и даже тромбоциты содержит тот или иной ре пертуар PRR и, следовательно, может реагировать на действие подоб ного рода факторов повреждения. Микробные PAMP и эндогенные DAMP могут действовать как через специализированные, так и общие рецепторы. К последним структурам можно отнести большинство Toll-подобных рецепторов человека (TLR). Некоторые микробные и эндогенные паттерны могут непосредственно активировать системы комплемента и гемостаза.
В-третьих, это действие на клетки антигенспецифичных фак торов иммунного ответа, например взаимодействие иммунного ком плекса с Fc-рецепторами или взаимодействие Т-клеточного рецептора с комплексом антигенный пептид+MHC I и II классов. Данные взаи модействия обеспечивают выраженную активацию клеток определён ных клеточных популяций – «профессиональных» участников иммун ной и воспалительной реактивности. Прежде всего, это лимфоциты, нейтрофилы, макрофаги и тучные клетки.
Сопоставляя действие трёх типов факторов повреждения, сле дует отметить, что более сильное влияние на клетки оказывают лиган ды, действующие на клеточные рецепторы, ассоциированные с той
145
или иной системой внутриклеточных посредников. При этом большое число рецепторов (более 500), взаимодействующих с PAMP и DAMP, продуктами иммунного ответа, медиаторами воспаления и участвую щих в активационных контактных взаимодействиях между клетками, в конечном итоге активируют внутри клетки ограниченное число транс крипционных факторов. Ключевая роль среди них принадлежит NF κB, вовлекающему в процесс транскрипции более 200 индуцибельных генов. При этом транскрипционные факторы клеточного стресса могут активироваться не только через системы вторичных посредников раз личных рецепторов, но и такими неспецифическими воздействиями как гипоксия, ацидоз, накопление во внутриклеточной среде свобод ных радикалов.
Таким образом, сигналы, несущие информацию клеткам о на личии или угрозе повреждения, весьма разнообразны. Их действие приводит как к активации специфических, присущих определённому типу клеток функций (например, процесс фагоцитоза), так и типовым изменениям при клеточном стрессе – повышению основного обмена, развитию оксидантного стресса, продукции различных белков (напри мер, белков теплового шока), которые неспецифично усиливают ус тойчивость клетки к повреждающим воздействиям различной приро ды. При получении сигнала о наличии или возможности повреждения в клетках активируются сотни «молчащих» в физиологических усло виях структурных генов. Продуктами их экспрессии являются инду цибельные белки, определяющие развитие экстремальных программ на уровне клетки и процесса воспаления на уровне повреждённой тка ни и организма в целом.
Действие факторов повреждения на клетку инициирует её ак тивацию, но для полноценного развития клеточной стресс-реакции и тем более кооперации отдельных клеток при развитии воспалительно го процесса необходимы и другие стимулы через медиаторы воспале ния, которые клетка получает аутокринно или паракринно. В качестве медиаторов воспаления выступают цитокины, биогенные амины, эйко заноиды и ряд других регуляторных межклеточных посредников. В этом плане можно говорить о феномене «заразительности» воспали тельной реакции на клеточном уровне. Любая активированная клетка способна продуцировать тот или иной спектр медиаторов воспаления, но наиболее активно это делают «клетки-профессионалы» воспали тельного процесса. Грань между факторами повреждения и медиато рами воспаления до определённой степени условна. Так, ряд эндоген ных факторов, действующих, в частности, через TLR, например белки теплового шока (Hsp60, Hsp72) и ядерный белок HMGB1 (англ. high
146
mobility group box 1), в большом количестве выделяются во внекле точную среду при разрушении различных ядросодержащих клеток, но могут и секретироваться в качестве медиаторов различными активиро ванными популяциями лейкоцитов, макрофагами и клетками микросо судов. В целом при развитии воспаления в качестве причинных факто ров ключевую роль играют маркеры повреждения, а медиаторы воспа ления являются следствием их действия, и после исчезновения агентов альтерации воспалительный процесс завершается.
Итак, развитие воспалительной реактивности можно рассмот реть с позиции клеточного стресса, решающего две основные задачи:
1)увеличение устойчивости клетки к действию повреждаю щих факторов различной природы;
2)формирование межклеточных коопераций в процессе раз вития программы воспалительного ответа.
Между тем, понятие «клеточный стресс» не вполне конкретно
иприменительно к воспалительному процессу требует подразделения на три принципиально различные по своему качеству стадии.
1-я стадия – активация специализированных физиологических функций, присущих соответствующему типу клеток. Эта стадия кле точного стресса характеризуется, прежде всего, проявлением «внеш них» по отношению к очагу воспаления механизмов. Развитие этой стадии не требует воздействия на клетку агентов повреждения и может инициироваться, например, нейроэндокринными регуляторными фак торами.
2-я стадия – стадия «воспалительной» трансформации, ответ клеток на повреждение или угрозу повреждения в виде усиления ос новного обмена, с вовлечением индуцибельных генов, связанных с синтезом медиаторов воспаления, белков теплового шока, других стресс-молекул, действие которых направлено на увеличение устойчи вости клетки к действию повреждающих факторов. На этой стадии характер информационного межклеточного обмена качественно меня ется за счёт продукции большого количества индуцибельных стресс молекул: медиаторов, рецепторов и их внутриклеточных посредников. Вторая стадия характерна для развития «внутренних» механизмов на уровне отдельных клеток.
3-я стадия – депрессивная – результат гиперактивации клеток, превышающей их адаптационные возможности. Для этой стадии ха рактерно снижение основного обмена, синтеза стресс-молекул, интен сивности межклеточного обмена информацией, переход к пассивной защите от действия неблагоприятных факторов.
Вторая и третья стадия клеточного стресса характеризуются
147
нарушением физиологических функций, что является атрибутным при знаком клеток-резидентов в очаге воспаления. При этом доминирова ние в воспалительном инфильтрате макрофагов и лейкоцитов, нахо дящихся в третьей стадии клеточного стресса, может привести к несо стоятельности барьерной функции очага воспаления.
Теперь мы вплотную подошли к определению сути системно го воспаления. Прежде всего, основным условием развития системно го воспаления является генерализация в кровотоке факторов повреж дения, способных индуцировать «воспалительный» клеточный стресс на системном уровне. В свою очередь, генерализация 2–3-й стадий клеточного стресса составляет клеточную основу развития системного воспаления, а превалирование той или иной стадии определяет дина мику типового патологического процесса, а именно смену фаз систем ного воспаления: гиперэргической, или, иначе, флогогенного (иниции рованного воспалением) удара, и депрессивной, или гипоэргической, фазы. При волнообразном течении процесса фазы могут повторяться неоднократно. (Более подробно, фазы системного воспаления будут охарактеризованы ниже.)
Если бы любое проникновение повреждающих факторов во внутрисосудистую среду сопровождалось развитием системного вос паления, то жизнь человека была бы мимолетной. Следовательно, ме жду действием факторов повреждения и развитием системного воспа ления должны быть биологические барьеры, которые можно обозна чить как факторы антивоспалительной резистентности. Механизмы антивоспалительной резистентности можно свести к следующим со ставляющим.
1.Наличие определённого порога реагирования на действие факторов повреждения – игнорирование клеткой допороговых раздра жителей.
2.Удаление из системного кровотока бактериальных антиге нов и продуктов тканевой деградации за счёт неактивационного фаго цитоза со стороны сосудистых стромальных макрофагов.
3.Блокирование начальных системных проявлений «внутрен них» механизмов воспалительной реакции со стороны антипротеиназ ной и антиоксидантной систем организма, ингибиторов отдельных компонентов систем гемостаза и комплемента и других антивоспали тельных механизмов.
Таким образом, для развития системного воспаления генера лизованное действие повреждающих факторов должно превышать по силе воздействия компенсаторные возможности факторов антивоспа лительной резистентности.
148
В целом системный клеточный стресс является своеобразным фоном, на котором развивается системное воспаление. Однако воспа лительный процесс нельзя представить только как реакцию отдельных клеток без выделения ключевых и второстепенных механизмов меж клеточной взаимосвязи.
С этих позиций системное воспаление можно характеризовать как генерализованное задействование «внутренней» программы воспа лительного процесса. Однако невозможно даже представить организм человека в виде «большого очага воспаления». Очевидно, что генера лизация базовых механизмов воспаления на системном уровне будет подчиняться тем же закономерностям межклеточного взаимодействия, но проявляться они должны как-то иначе.
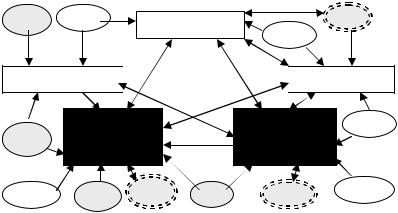
Основные звенья «внутренней» программы очага воспаления – система гемостаза и комплемента, эндотелиоциты и другие клетки микрососудов, мастоциты и фагоцитирующие клетки воспалительного инфильтрата – схематично отображены на рис. 19. Стрелками показа ны основные направления их взаимной активации, а также взаимодей ствие с гуморальными и клеточными факторами иммунного ответа и паттернами повреждения.
IgM |
ЛПС |
Эндотелиоциты |
Th |
|
|
|
ПТД |
Система комплемента Система гемостаза
Система гемостаза
|
Мастоциты, |
|
|
Макрофаги, |
ЛПС |
IgG |
базофилы, |
|
|
нейтрофилы |
|
|
эозинофилы |
|
|
|
|
ЛПС |
IgE |
Th2 |
IgG |
Th1 |
ПТД |
Рис. 19. Ключевые механизмы воспалительной реактивности «внутреннего» или базового уровня, реализуемого в очаге классического воспаления: стрелка ми, обозначены непосредственные потенцирующие воздействия; ЛПС – липополисаха риды и другие микробные паттерны; ПТД – продукты тканевой деградации. В затемнён ных кружках обозначены антигенспецифические факторы неоиммунитета
149