Материал: GMP_prefinal
40. Требования к качеству технологической воды в производстве ле-карственных средств. Методы очистки.
Из презентации
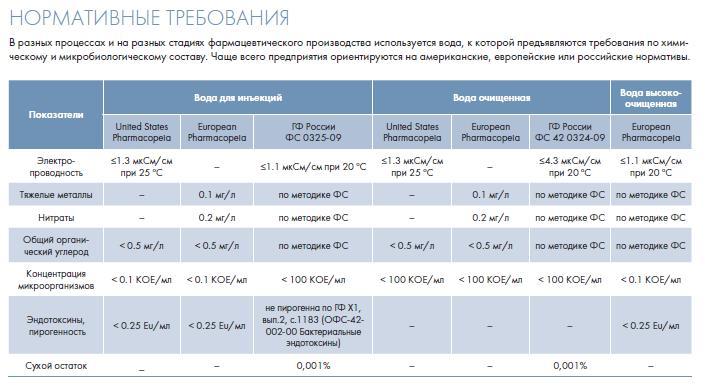
Требования к качеству воды регламентируется фармакопейными статьями (ФС.2.2.0020.15 «Вода очищенная» и ФС.2.2.0019.15 «Вода для инъекций»).
Методы очистки (этапы водоподготовки)
-
грубая очистка от механических включений фильтрацией;
-
фильтрация через угольный фильтр;
-
умягчение воды (извлечения из воды солей Ca2+ и Mg2+);
-
деионизация
-
обратный осмос
-
дистилляция
Системы предварительной подготовки воды
Автоматические фильтры механической очистки, удаления железа и марганца, умягчения, дехлорирования
Установки механической фильтрации
-
Предназначены для удаления из воды взвешенных и коллоидных частиц, содержа-щихся в исходной воде. В большинстве случаев промышленной водоподготовки механи-ческая фильтрация является предварительным этапом в общей схеме обессоливания воды
-
производится после ее осветления в отстойниках, флотаторах или осветлителях.
-
Сущность механической фильтрации заключается в пропускании жидкости, со-держащей примеси, через фильтрующий материал, проницаемый для жидкости и не про-
42
ницаемый для твердых частиц. В качестве фильтрующего материала используются сетки, ткани, различные пористые материалы, кварцевый песок, антрацит и др.
Метод обратного осмоса
Обратный осмос – это процесс перехода растворителя (воды) из раствора через по-лупроницаемую мембрану под действием внешнего давления. Избыточное рабочее давле-ние солевого раствора в этом случае намного больше осмотического. Движущей силой обратного осмоса является разность давлений.
Поток воды продавливается через обратноосмотическую мембрану. Происходит полное удаление солей из жидкости.
Установки электродеионизации
-
помощью процесса электродеионизации возможно удаление минеральных ве-ществ. Метод электродеионизации целесообразно использовать после стадии обратного осмоса. Процентное содержание общих растворенных в воде веществ снижается более чем на 99%, удельная электропроводность снижается более чем в 15 раз
43
41. Критерии отбора персонала при приеме на работу.
Из методички АБ.
Сотрудники фармацевтического предприятия должны:
-
иметь спокойный, уравновешенный характер;
-
сознательно и ответственно относиться к выполняемой работе;
-
быть дисциплинированными, аккуратными, пунктуальными и правдивыми;
-
быть готовыми к перенесению неудобств, связанных с условиями работы (работа в помещениях без естественного освещения, ношение комплекта технологической одежды, выполнение монотонно повторяющихся операций и другие).
-
соблюдать правила личной гигиены и иметь склонность к поддержанию чистоты и порядка на рабочем месте; хорошей практикой является составление гигиенического обя-зательства на этапе приема на работу, в котором каждый работник знакомится с ключе-выми требованиями гигиены и, подписывая, соглашается на привлечение к дисциплинар-ной и административной ответственности за возможные нарушения.
-
после принятия решения о приеме претендента на работу на него должна быть за-ведена учетная карточка, которая должна храниться в отделе кадров.
Состояние здоровья
-
На предприятии должны быть разработаны и выполняться инструкции (процеду-ры), регламентирующие состояние здоровья персонала, порядок проведения медицинских осмотров и правила допуска сотрудников в помещения для производства, контроля и хра-нения.
-
Весь персонал предприятия, включая временно работающих, должен проходить периодические медицинские осмотры. Частота проведения осмотров зависит от характера производства и условий работы персонала.
-
На каждого сотрудника предприятия должна быть заведена медицинская карта, в которой указывают дату посещения врача, диагноз, рекомендации, фамилию врача.
-
Сотрудники отдела обеспечения качества или отдела по работе с персоналом должны регулярно проверять периодичность проведения медицинских обследований и наличие записей в медицинской книжке.
-
Персонал, осуществляющий визуальный контроль инъекционных препаратов, дол-жен проходить регулярные осмотры врачами окулистами.
-
Рекомендуется проверять аллергическую чувствительность персонала к продуктам
-
материалам, с которыми он работает.
-
К работе, связанной с производством и контролем лекарственных средств не долж-ны допускаться носители патогенной микрофлоры; люди, страдающие аллергическими и кожными заболеваниями или имеющие аллергические реакции на продукты и материалы, с которыми они работают; сотрудники с повышенным отделением перхоти.
-
Временно, до нормализации состояния здоровья, к работе не должны допускаться сотрудники, чувствующие легкие недомогания или простуду, больные инфекционными заболеваниями или имеющие повреждения кожи различной степени на открытых участках тела.
-
Персонал должен ставить в известность своего руководителя о любых недомогани-ях (кожные, острые респираторные и другие заболевания), способных оказать нежела-тельное воздействие на качество лекарственных средств.
-
Ответственность за допуск к работе и своевременное направление работников на периодические медицинские осмотры несут руководители подразделений и начальник от-дела кадров. Персоналу вменено в обязанность сообщать руководителю своего подразде-ления о малейших признаках заболевания; в этом случае он отстраняется от работы и направляется в лечебно-профилактическое учреждение.
44
42. Правила обучения персонала на фармацевтическом предприятии.
Из методички АБ
План обучения работников Предприятия должен быть составлен в соответствии с мировыми стандартами качества. Для этого необходимо предусмотреть специальные по-мещения, где будет происходить обучение новых работников, практикантов, контролеров качества и повышение квалификации менеджеров Предприятия.
Пример трехуровневой системы, по которой проводится обучение персонала (по группам в зависимости от занимаемых должностей и подразделения):
-
Обучение по общим вопросам в форме лекций, просмотра видеофильмов. Тематика занятий включает вопросы GMP, охраны окружающей среды, личной гигиены, правила санитарного режима на предприятии, общие принципы обеспечения гарантии ка-чества производства ЛС, общие вопросы охраны труда и т.д. (не менее 1 раза в 2 месяца).
-
Профессиональное обучение по стандартным операционным процедурам (SOP) – раз в квартал в форме инструктажа .
-
Обучение по вопросам охраны труда, техники безопасности и пожарной безопасности (вводный инструктаж при поступлении на работу, ежеквартальный инструк-таж по SOP и др.) 1 раз в квартал.
-
Производитель должен обеспечить обучение всего персонала, чьи служеб-ные обязанности предполагают их пребывание в производственных зонах или контроль-ных лабораториях (включая технический и обслуживающий персонал, а также сотрудни-ков, производящих уборку), и другого персонала, чья деятельность может оказать влияние на качество продукции.
-
Кроме основного обучения, включающего теорию и практику GMP, вновь принятый на работу персонал должен пройти обучение в соответствии с обязанностями, которые за ним закреплены. Следует также проводить последующее обучение, периоди-чески оценивая его практическую эффективность. Должны иметься учебные программы, утвержденные соответственно либо руководителем производства, либо руководителем отдела контроля качества. Протоколы обучения должны сохраняться.
-
Предпочтительно, чтобы посетители или не прошедший обучения персонал не допускался в зоны производства и контроля качества. Если это неизбежно, то они должны предварительно получить инструктаж, в частности по личной гигиене и исполь-зованию требуемой защитной одежды. За ними необходим тщательный надзор.
-
Ответственность за организацию и функционирование системы обучения на фармацевтическом предприятии несет Исполнительный директор; начальник ООК обес-печивает и контролирует проведение обучения персонала предприятия.
-
Главный инженер отвечает за организацию и проведение обучения по охране труда, промышленной санитарии, противопожарной безопасности.
-
Внутреннее обучение персонала включает проведение первичного, периоди-ческого, специального и внепланового обучения. Внутреннее обучение завершается атте-стацией сотрудников. Обучение персонала на предприятии осуществляют руководители подразделений или квалифицированные специалисты.
-
Практическое обучение персонала проводится на рабочих местах квалифи-цированными работниками. Обучение персонала проводится на основании Программ под-готовки и повышения квалификации рабочих, разработанных по каждой профессии.
45
43. Опишите круг обязанностей руководящих работников фармацев-тического предприятия.
Из презентации
Руководители производства, руководитель службы (отдела) контроля качества и Уполномоченное лицо (лица) должны быть заняты на предприятии полный рабочий день. Руководители производства и службы (отдела) контроля качества должны быть независи-мыми друг от друга. На больших предприятиях часть функций передается, при необходи-мости, другим сотрудникам.
Обязанности Уполномоченных лиц
-
a) Для лекарственных средств, выпущенных в Российской Федерации, Уполномо-ченное лицо должно гарантировать, что каждая серия продукции была произведена и про-верена в соответствии с установленными требованиями;
-
b) Для лекарственных средств, выпущенных вне Российской Федерации, Уполно-моченное лицо должно гарантировать, что импортируемая серия продукции прошла про-верку в порядке, установленном для России;
-
c) До выдачи разрешения на выпуск лекарственных средств в сферу обращения Уполномоченное лицо должно документально подтвердить, что каждая серия продукции удовлетворяет соответствующим документам.
-
Квалификация Уполномоченного лица должна соответствовать установленным требованиям. Уполномоченное лицо должно входить в штат предприятия - производителя лекарственных средств. Его обязанности могут быть переданы только лицам, имеющим статус Уполномоченного лица.
Основные обязанности руководителя производства
-
Организация производства и хранения продукции в соответствии с документацией
-
целью обеспечения требуемого качества.
-
Утверждение инструкций, связанных с производственным процессом, и обеспече-ние их точного выполнения.
-
Контроль за рассмотрением и подписанием всех производственных протоколов ли-цами, имеющими необходимые полномочия, до передачи их в службу контроля качества.
-
Контроль за работой своего подразделения, содержанием помещений, эксплуата-цией и техническим обслуживанием оборудования.
-
Контроль за проведением работ по аттестации (валидации).
-
Организация первичного и последующего обучения производственного персонала.
Основные обязанности руководителя службы контроля качества
-
Утверждение или отклонение исходных и упаковочных материалов, промежуточ-ной, нерасфасованной и готовой продукции.
-
Оценка протоколов на серию продукции.
-
Проведение необходимых испытаний.
-
Утверждение спецификаций, инструкций по отбору проб, методик испытаний и других методик по контролю качества.
-
Допуск к работе специалистов-аналитиков, работающих по контракту, и контроль за их деятельностью.
-
Контроль работы подведомственного отдела, обслуживания его помещений и обо-рудования.
-
Контроль проведения аттестации (валидации).
46
-
Организация первичного и последующего обучения персонала подведомственного отдела.
Руководители производства и отдела контроля качества имеют ряд совместных обязанностей, относящихся к обеспечению качества продукции. Эти обязанности с учетом действующих норм и правил могут включать в себя следующее:
-
утверждение письменных инструкций, методик и других документов, в т.ч. внесе-ние изменений в них;
-
контроль за окружающей средой на производстве;
-
контроль за соблюдением правил производственной гигиены;
-
аттестацию (валидацию) процессов;
-
обучение персонала;
-
утверждение и контроль за поставщиками исходных материалов;
-
утверждение и контроль за производителями, работающими по контракту;
-
определение условий хранения материалов, продукции и контроль за их соблюде-
нием;
-
хранение протоколов;
-
постоянный контроль соответствия требованиям настоящего стандарта;
-
проведение инспекций, расследований и отборов проб с целью выявления факто-ров, способных повлиять на качество продукции.
-
Обязанности уполномоченного лица:
а) уполномоченное лицо должно подтвердить, что каждая серия лекарственных средств, произведенная в Российской Федерации, произведена и испытана в соответствии
-
действующим законодательством Российской Федерации и требованиями регистрацион-ного досье;
б) в отношении лекарственных средств, выпущенных за пределами Российской Фе-дерации, уполномоченное лицо должно подтвердить, что каждая импортируемая серия продукции прошла проверку в порядке, установленном в Российской Федерации;
в) уполномоченное лицо должно документально подтвердить, что процесс производ-ства осуществлен в соответствии с настоящими Правилами, а также удостоверить перед выдачей каждого разрешения на выпуск, что каждая серия продукции произведена и (или) испытана в соответствии с требованиями регистрационного досье.
Квалификация уполномоченного лица должна соответствовать требованиям, уста-новленным законодательством Российской Федерации. Уполномоченное лицо должно со-стоять в штате производителя. Его обязанности могут быть переданы только другому уполномоченному(ым) лицу(ам).
-
Основные обязанности руководителя производства:
а) обеспечивать производство и хранение продукции в соответствии с утвержденной документацией для достижения необходимого качества;
б) утверждать инструкции, касающиеся производственных операций, и обеспечивать их точное выполнение;
в) обеспечивать оценку и подписание производственных записей уполномоченным на это персоналом перед их передачей в подразделение контроля качества;
г) контролировать работу подчиненного структурного подразделения, содержание помещений, эксплуатацию и техническое обслуживание оборудования;
д) обеспечивать проведение соответствующей валидации;
47
е) обеспечивать проведение необходимого первичного и последующего непрерывно-го обучения персонала подчиненного структурного подразделения.
3.Основные обязанности руководителя подразделения контроля качества:
а) одобрять или отклонять исходное сырье, упаковочные материалы, а также проме-жуточную, нерасфасованную и готовую продукцию;
б) оценивать досье на серию;
в) обеспечивать проведение всех необходимых испытаний;
г) утверждать спецификации, инструкции по отбору проб, методы испытаний и дру-гие процедуры по контролю качества;
д) утверждение и мониторинг исполнителей по договорам;
е) контролировать работу подчиненного структурного подразделения, содержание помещений, эксплуатацию и техническое обслуживание оборудования;
ж) обеспечивать проведение соответствующей валидации;
з) обеспечивать проведение необходимого первичного и последующего непрерывно-го обучения персонала подчиненного структурного подразделения.
Руководители производства и подразделения контроля качества имеют общие или совместно выполняемые обязанности, относящиеся к качеству, которые включают в себя,
-
частности, следующее:
-
утверждение процедур и других документов, включая внесение изменений в них; мониторинг и 2) контроль производственной среды;
-
контроль производственной гигиены; валидацию процессов;
-
обучение персонала;
-
утверждение и мониторинг поставщиков исходного сырья и упаковочных матери-
алов;
-
утверждение и мониторинг исполнителей по договорам
-
определение и мониторинг условий хранения исходного сырья и продукции; хра-нение записей;
-
мониторинг соответствия требованиям настоящих Правил;
-
проверку, исследование и взятие проб в целях мониторинга факторов, способных влиять на качество продукции.