Материал: GMP_prefinal
5.8. Следует проводить проверки выходов и материального баланса, чтобы убедить-ся в отсутствии расхождений с допустимыми пределами.
5.9. Не допускается одновременное или последовательное проведение операций с различными продуктами в одном и том же помещении за исключением тех случаев, когда не существует риска перепутывания или перекрестной контаминации.
5.10. Продукция и материалы должны быть защищены от микробной и другой кон-таминации на всех стадиях производства.
5.11. При работе с сухими материалами и продукцией необходимо принимать осо-бые меры предосторожности по предотвращению образования и распространения пыли. Это особенно важно при работе с высоко активными и сенсибилизирующими веществами.
5.12. В течение всего времени процесса производства все используемые материалы, тара для нерасфасованной продукции, основные единицы оборудования и, при необходи-мости, помещения должны быть маркированы этикетками или иным способом с указани-ем производимой продукции или обрабатываемых материалов, а также их дозировки (где применимо) и номера серии. Там, где это приемлемо, такая маркировка должна также ука-зывать стадию технологического процесса.
5.13. Этикетки, прикрепленные к контейнерам, оборудованию или помещениям, должны быть четкими, однозначными, установленной на предприятии формы. Часто по-лезно в дополнение к информации на этикетках для указания статуса (например: в каран-тине, принято, отклонено, чистое и др.) использовать цвета.
5.14. Следует контролировать правильность соединения трубопроводов и других ча-стей оборудования, применяемых для транспортирования продукции из одной зоны в дру-гую. 5.15. Не допускаются любые отклонения от инструкций или процедур. Если произо-шло отклонение от них, то оно должно быть письменно санкционировано лицом, имею-щим соответствующие полномочия, с привлечением при необходимости подразделения контроля качества.
5.16. В производственные помещения может входить только персонал, имеющий право доступа в них.
Эффективность или коэффициент проскока фильтров определяются по счетной кон-центрации наиболее проникающих частиц до и после фильтра. Значение эффективности фильтра, полученное другими методами, кроме метода оценки по размеру наиболее про-никающих частиц, не может служить для целей классификации фильтров по данному стандарту. Интегральные значения эффективности и коэффициента проскока характери-зуются усредненными значениями соответствующих показателей по всей рабочей поверх-ности фильтра. Локальное значение характеризуется значением показателя в данной точке фильтра.
32. Объекты, документация и методы самоинспекции.
Самоинспекция - проверка производителем деятельности своего предприятия с це-лью оценки его соответствия всем аспектам Правил организации производства и кон-троля качества лекарственных средств (GMP).
Объекты самоинспекции:
-персонал;
-помещения, включая помещения для подготовки персонала;
-эксплуатация зданий и оборудования;
-хранение сырья и готовых продуктов;
-контроль производства и постадийный контроль;
-контроль поступления, хранения и использования упаковочных и маркировочных материалов;
-контроль качества;
-документация;
-санитария и гигиена;
-программы по проведению валидации и ревалидации; -калибровка инструментов и измерительных приборов; -процедура отзыва продуктов с рынка; -порядок рассмотрения рекламаций;
-результаты проведения предыдущих самоинспекций и принятые меры.
Документация системы самоинспекции.
-СОП о проведении самоинспекции
-Опросники, памятки, методички
-Заполняемые формы (регистрация несоответствий, отчет о выполнении корректи-рующих мероприятий)
-Отчеты о самоинспекции
-План-график самоинспекции
-Планы корректирующих мероприятий-Положение (инструкция) о группе самоинспекции и аудиторе
Методы самоинспекции.
-Опросники и памятки.
-Интервью
33. Принципы управления рисками для качества лекарственных средств.
Оценка риска качества должна базироваться на научных знаниях и в итоге должна быть связана с защитой пациента.
Уровень затраченных усилий, использования формализованных подходов и доку-ментирования процесса управления рисками качества должен быть соразмерен уровню риска.
Схема управления рисками для качества (ICH Q9)
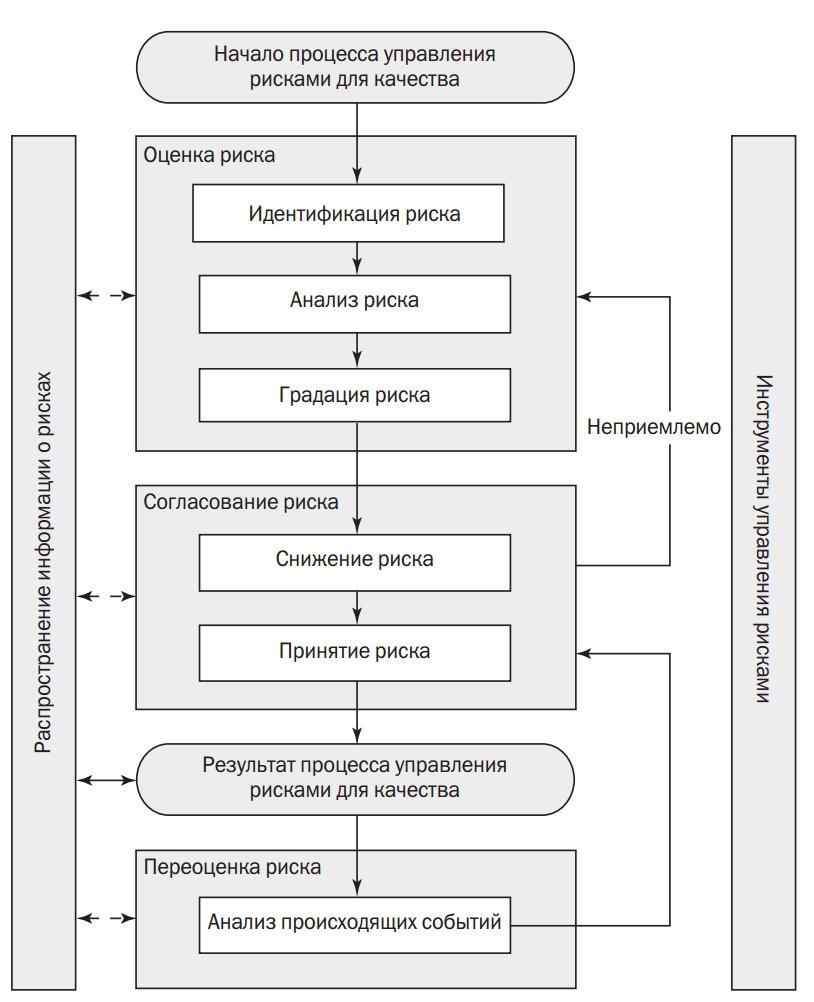

34. Основные правила планировки производственных зданий в соот-ветствии с gmp.
Помещения и оборудование необходимо располагать, проектировать, строить, осна-щать и эксплуатировать таким образом, чтобы они соответствовали проводимым операци-ям.
Их планировочное решение и конструкция должны сводить к минимуму риск оши-бок и обеспечивать возможность эффективной очистки и обслуживания в целях исключе-ния перекрестной контаминации, накопления пыли или грязи и любых неблагоприятных факторов для качества продукции.
Помещения должны быть расположены так, чтобы минимизировать риск перекрест-ного загрязнения, т.е. НЕ располагать их рядом с металлургическими заводами с высоким уровнем взвешенной пыли
Планировочные решения помещений должны соответствовать логической последо-вательности производственных операций и требуемым уровням чистоты.
35
Планировочные решения рабочих зон и внутрипроизводственных зон хранения должны обеспечивать последовательное и логичное размещение оборудования и материа-лов, сводящее к минимуму риск перепутывания различных лекарственных препаратов или их компонентов,
обеспечивающее отсутствие перекрестной контаминации и сводящее к минимуму риск пропуска или неправильного осуществления любого этапа при производстве или контроле.
35. Виды производственных зон фармацевтического предприятия и требования к ним.
-Производственная зона
-Складские зоны
-Зоны контроля качества
-Вспомогательные зоны
Требования к производственным зонам:
-
Расположение и конструкция помещений должны сводить к минимуму риск оши-
бок
-
обеспечивать возможность эффективной очистки и обслуживания в целях исклю-
чения перекрестной контаминации, накопления пыли или грязи и любых неблагопри-
ятных факторов для качества продукции.
-
Температура и относительная влажность должны контролироваться, наблюдаться в соответствии с СОП, а результаты - фиксироваться.
-
Стерильную продукцию необходимо производить в чистых зонах, доступ в кото-рые персонала и/или поступление оборудования, исходного сырья и материалов должны осуществляться через воздушные шлюзы. В чистых помещениях (зонах) должен поддер-живаться уровень чистоты, отвечающий соответствующему стандарту чистоты, в них необходимо подавать воздух, который прошел через фильтры соответствующей эффек-тивности.
-
Запрещается производство ядов технического назначения, таких как пестициды и гербициды, в помещениях, используемых для производства лекарственных препаратов.
Требования к складским зонам:
-
Складские зоны должны быть достаточно вместительными, чтобы обеспечить упо-рядоченное хранение различных категорий материалов и продукции: исходного сырья и упаковочных материалов, промежуточной, нерасфасованной и готовой продукции, а так-же продукции, находящейся в карантине, продукции, разрешенной для выпуска, отбрако-ванной, возвращенной или отозванной.
-
Складские зоны должны быть чистыми и сухими, в них должна поддерживаться требуемая температура.
-
Раздельные участки приема и отправки
-
Материалы и продукты защищены от воздействия погодных условий.
-
Должна быть предусмотрена зона для очистки поступающих материалов
Требования к зонам взвешивания(зоны взвешивания могут находиться как в склад-ских, так и производственных зонах):
-
Взвешивание исходного сырья и определение выхода путем взвешивания обычно должны проводиться в отдельных зонах для взвешивания, предусматривающих меры про-тив запыленности (включая вытяжку пыли и воздуха).
-
Обеспечение контроля загрязненности
36
-
Гладкие, непроницаемые, надежные, легко очищаемые покрытия
-
Процедуры очистки и их регистрация
-
Документация, книги учета и регистрация
-
Погрешность весов и другого измерительного оборудования должна соответство-вать производственным и контрольным операциям, в которых они используются.
Требования к зонам упаковки:
-
Достаточные площади для складирования всех категорий материалов (промежу-точные продукты, конечные продукты, упаковочный материал, вкладыши и.т.п.)
-
Разделение первичной и вторичной упаковки
-
Предоставление зон для переделки поддонов
-
Контролированные условия складирования - чистота, безопасность, защита
-
Определение и контроль за:
• частицами
• температурой
• Относительной влажностью
• Давление в помещении
Требования к вспомогательным зонам:
-
Комнаты отдыха и приема пищи должны быть отделены от других зон.
-
Помещения для переодевания, туалеты и душевые кабины должны иметь удобный доступ; их планировка и размеры должны соответствовать численности персонала. Не до-пускается, чтобы туалеты непосредственно сообщались с производственными или склад-скими зонами.