Материал: Biokhimia_Bilety_1-1968421400-1498556783
По физическим свойствам аминокислоты резко отличаются от соответствующих кислот и оснований. Все они кристаллические вещества, лучше растворяются в воде, чем в органических растворителях, имеют достаточно высокие температуры плавления; многие из них имеют сладкий вкус. Эти свойства отчётливо указывают насолеобразный характер этих соединений. Особенности физических и химических свойств аминокислот обусловлены их строением — присутствием одновременно двух противоположных по свойствам функциональных групп: кислотной и основной. α-аминокислоты являются амфотерными электролитами.
3 Витамин с Витамин с
Аскорбиновая кислота, антискорбутный витамин (скорбут = цинга).
Является лактоном. Легко окисляется:
Енольные гидроксилы неустойчивы, особенно в присутствии кислорода. В кислой среде витамин С сохраняется лучше.
Роль витамина с в обмене веществ
1. участвует в реакциях гидроксилирования (ЛИЗ→ОЛИ, ПРО→ОПР), что требуется для "сшивок" молекул коллагена в соединительной ткани;
2. участвует в триптофана и диоксиметила с образованием нейромедиаторов (норадреналин и др.);
3. необходим для синтеза кортикостероидов;
4. необходим для образования нейромедиаторов.
Гиповитаминоз С проявляется поражением соединительной ткани – повышенная хрупкость сосудов, пипехии (точечные кровоизлияния на коже), кровоточивость десен.
Авитаминоз С – цинга (скорбут): кровоизлияния во внутренние органы, более выраженные повреждения соединительной ткани.
Суточная потребность витамина С 100-150 мг. Она возрастает при инфекционных заболеваниях, стрессовых состояниях, лактации, беременности – до 300 мг/сут.
Источники витамина С: овощи, фрукты, зеленые растения; главные – черная смородина, шиповник, грецкий орех, цитрусовые. В России основным источником его является картофель (10 мг/100 г) и квашенная капуста.
Причины гиповитаминоза С:
1. витамин С неустойчив;
2. он необходим в относительно больших количествах;
3. в организме отсутствуют запасы витамина С
4 Дыхательная функция крови
Кровь осуществляет свою дыхательную функцию прежде всего благодаря наличию в ней гемоглобина. Физиологическая функция гемоглобина как переносчика кислорода основана на способности обратимо связывать кислород в зависимости от его напряжения в крови. Поэтому в легочных капиллярах происходит насыщение крови кислородом, а в тканевых капиллярах, где парциальное давление кислорода резко снижено, осуществляется отдача кислорода тканям.
В состоянии покоя ткани и органы человека потребляют около 200 мл кислорода в минуту. При тяжелой физической работе количество потребляемого тканями кислорода возрастает в 10 и более раз (до 2-3 л O2 в 1 мин). Доставка от легких к тканям такого количества кислорода в виде газа, физически растворенного в плазме, невозможна вследствие малой растворимости кислорода в воде и плазме крови
функцию переносчика кислорода в организме выполняет гемоглобин
№ 37.
1 Функции и транспорт жиров.
Жиры выполняют следующие функции: 1)Структурную (в состав каждой клетки входит холестерин, при этом содержится он обычно в клеточной мембране. При отсутствии достаточного количества холестерина клеточная мембрана теряет свои свойства и, в конце концов, может привести к гибели клетки. Кроме этого жиры входят в состав нервной ткани); 2)Энергетическая (примерно 30% от всей вырабатываемой в организме энергии получается в процессе окисления именно жиров (при окислении 1г жиров высвобождается 9ккал энергии); 3)Запасающая (жиры при избыточном поступлении в организм откладываются в организме. Именно благодаря этой функции человек в среднем может прожить около 30 дней без еды); 4)Защитная (жиры участвуют в защите организма от чужеродных микроорганизмов, а также обеспечивают некоторую долю протекции от воздействия невысоких доз радиационного излучения); 5)Гормональная (жиры вырабатывают цитокины, а также женские половые гормоны. Особенно велика гормональная роль жировой ткани в постменопаузе. Именно тогда жиры обеспечивают большую часть выработки женских половых гормонов. Однако и в репродуктивном периоде жировая ткань очень важна. Так достоверно известно, что снижения общей доли жировой ткани в организме ниже уровня в 10-15% приводит нарушение баланса между выработкой в женском организме мужских и женских гормонов в пользу первых. В результате возможно развитие аменореи, а иногда и бесплодия (чаще обратимого); 6)Транспортная (жиры способствуют всасыванию микроэлементов, а также так называемых жирорастворимых витаминов (A,D,E и K); 7)Гемостатическая (арахидоновая кислота является одним из активаторов свёртывающей и противосвёртывающей систем крови); 8)Улучшают вкусовые качества пищи, тем самым вызывая активацию центра голода в продолговатом мозге. Жирные кислоты, обладая способностью проникать через мембраны клеток, легко диффундируют через мембраны адипоцитов жировой ткани в клетки печени. Оказавшись внутри клеток, жирные кислоты вновь превращаются в триглицериды, взаимодействуя с глицеролом, образующимся в результате метаболических процессов в клетках, выполняющих функции депонирования (что будет рассмотрено далее). Липопротеин-липаза вызывает также гидролиз фосфолипидов, что, в свою очередь, приводит к выделению жирных кислот, преобразующихся в триглицериды и депонирующихся, как уже обсуждалось.
2 Роль креатинфосфата.
Креатин – вещество скелетных мышц, миокарда, нервной ткани. В виде креатинфосфатакреатин является "депо" макроэргических связей, используется для быстрого ресинтеза АТФ во время работы клетки.
Креатинфосфорная кислота — 2-[метил-(N'-фосфонокарбоимидоил)амино]уксусная кислота. Бесцветные кристаллы, растворимые в воде, легко гидролизуется с расщеплением фосфамидной связи N-P в кислой среде, устойчива в щелочной.
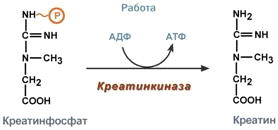 Креатинфосфат обеспечивает
срочный ресинтез
АТФ в
первые секунды работы (5‑10 сек), когда
никакие другие источники энергии
(анаэробный
гликолиз, аэробное
окисление глюкозы, β-окисление
жирных кислот) еще
не активированы, и кровоснабжение мышцы
не увеличено. В клетках нервной ткани
креатинфосфат поддерживает жизнеспособность
клеток при отсутствии кислорода.
Креатинфосфат обеспечивает
срочный ресинтез
АТФ в
первые секунды работы (5‑10 сек), когда
никакие другие источники энергии
(анаэробный
гликолиз, аэробное
окисление глюкозы, β-окисление
жирных кислот) еще
не активированы, и кровоснабжение мышцы
не увеличено. В клетках нервной ткани
креатинфосфат поддерживает жизнеспособность
клеток при отсутствии кислорода.
3 Биотин.
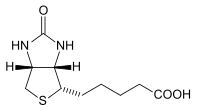
Витамин н (биотин)
Антисеборейный витамин. Структура: тиофен, соединеный с мочевиной+ боковая цепь (валериановая кислота).
Устойчив при нагревании.
Роль биотина в обмене веществ
Биотин – кофермент карбоксилирования (превращение ацетил-КоА в малонил-КоА в синтезе ВЖК) и кофермент транскарбоксилирования в синтезе пуриновых оснований.
Авитаминоз Н – себорея: покраснение и шелушение сальной кожи на волосистой части головы.
Суточная потребность витамина Н 0,010 мг.
Источники: печень, яйца, молоко.
Авитаминоз бывает при употреблении сырых яиц, содержащих авидин (антивитамин Н).
4 Гемоглобин, аномальный гемоглобин,в частности hb
Гемоглоби́н (от др.-греч. αἷμα — кровь и лат. globus — шар) — сложный железосодержащий белок , обладающих кровообращением, способный обратимо связываться с кислородом, обеспечивая его перенос в ткани. Нормальным содержанием гемоглобина в крови человека считается: у мужчин — 130—160 г/л (нижний предел — 120, верхний предел — 180 г/л), у женщин — 120—150 г/л
Главная функция гемоглобина состоит в переносе кислорода.
Гем — простетическая группагемоглобина
Аномальный гемоглобин
гемоглобин, имеющий аномальное строение вследствие мутации всоответствующем локусе хромосом.
№38 1.окисление жиров молока у детей
Окисление молочного жира и фосфолииидов молока вызывается ферментами, но чаще происходит химическим путем — под действием кислорода воздуха и света. Окисление жиров молока происходит при соприкосновении с воздухом, например, когда молоко перемешивается при дойки, при переливании, сепарировании, обработке. Сливки и сливочное масло – это концентрат окисленных жиров. При грудном вскармливании окисления не происходит, т.к. ребёнок (телёнок, козлёнок..) естественным путём, как это предусмотрела природа, высасывает молоко из груди (вымени) без соприкосновения с воздухом. Жиры должны поступать к нам в организм неокисленными.
-
В12 и фолеевая кислота
Кобаламин. Антианемический витамин.
Имеет красный цвет. На свету разлагается.
Роль кобаламина в обмене веществ
- транспорт метильных групп;
- участвует в транспорте водорода;
- превращение рибозы в дезоксирибозу;
- участвует в синтезе метионина.
{Т.е., кобаламин нужен для обмена белков и нуклеиновых кислот.}
Недостаток кобаламина: анемия, поражение нервной системы, снижение кислотности желудочного сока.
Суточная потребность в кобаламине 0,003 мг.
Источники: печень, рыба, яйца, молоко, + синтезируется микрофлорой. (в дрожжах – нет)
Недостаток кобаламина может возникать при заболеваниях желудка, в котором вырабатывается внутренний фактор Касла (транскоррин), необходимый для всасывания витамина В12.
Фолиевая кислота́ (витамин B9; лат. acidum folicum от лат. folium — лист) — водорастворимый витамин, необходимый для роста и развития кровеносной и иммунной систем.
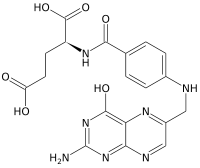
Недостаток фолиевой кислоты может вызвать мегалобластную анемию у взрослых, а при беременности повышает риск развития дефектов нервной трубки.
-
Декарбоксилирование аминокислот, биогенный амин
Процесс отщепления карбоксильной группы аминокислот в виде CO2 получил название декарбоксилирования. Несмотря на ограниченный круг аминокислот и их производных, подвергающихся декарбоксилированию в животных тканях, образующиеся продукты реакции — биогенные амины (т. н. «трупные яды») — оказывают сильное фармакологическое действие на множество физиологических функций человека и животных. В живых организмах открыты 4 типа декарбоксилирования аминокислот:
1. α-Декарбоксилирование,:
2. ω-Декарбоксилирование, свойственное микроорганизмам.:
3. Декарбоксилирование, связанное с реакцией трансаминирования:
4. Декарбоксилирование, связанное с реакцией конденсации двух молекул:
Реакции декарбоксилирования в отличие от других процессов промежуточного обмена аминокислот являются необратимыми. Биоге́нные ами́ны — вещества, образующиеся в организме животных или растений из аминокислот при их декарбоксилировании (удалении карбоксильной группы) ферментами декарбоксилазами и обладающие высокой биологической активностью. К биогенным аминам относятся дофамин, норадреналин и адреналин серотонин,
4. Распад гемоглобина
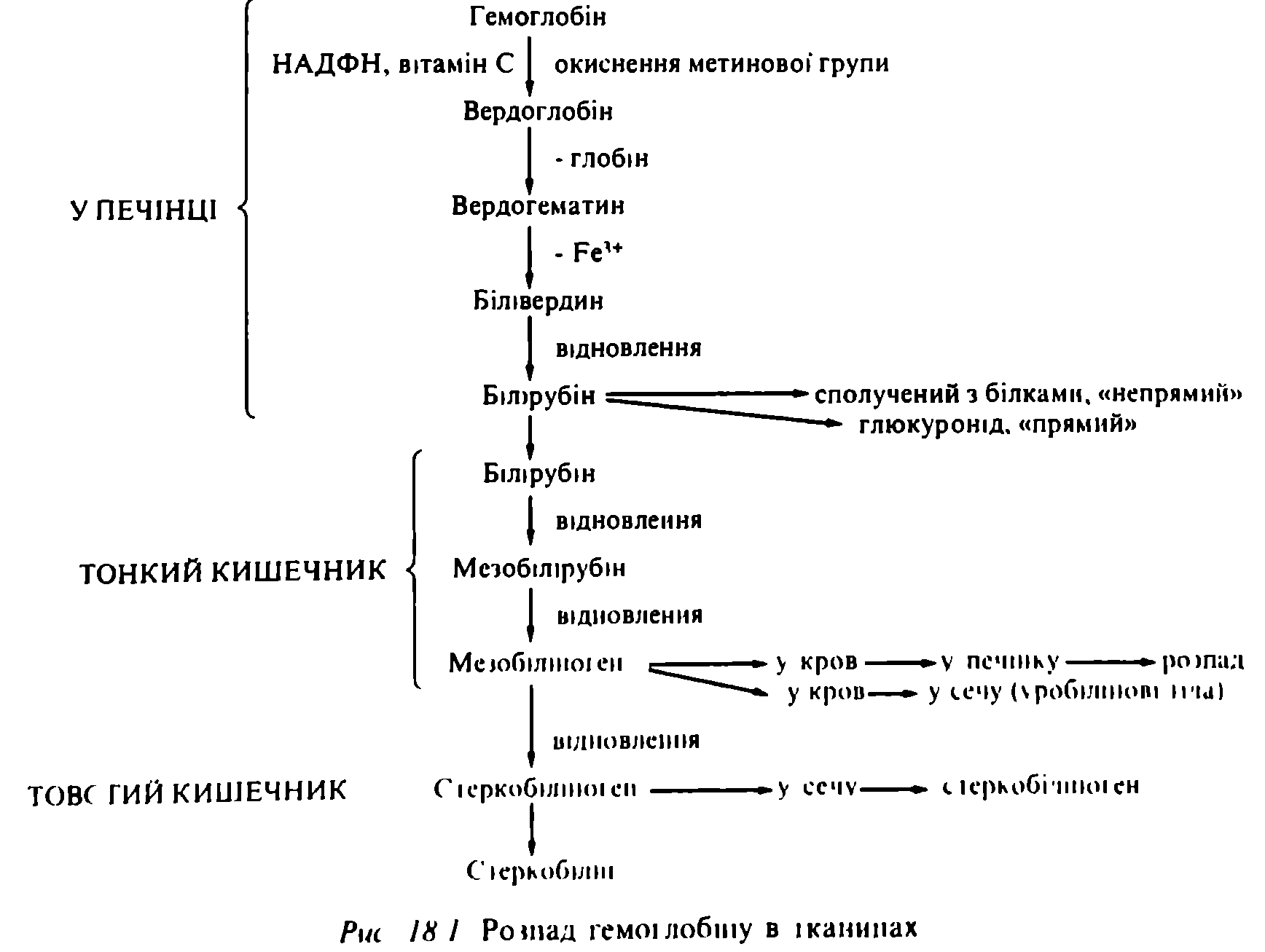
5.Патологические процессы при обмене веществ
Молекулярные патологии обменов или энзимопатии чаще всего представляют собой наследственные нарушения транспортной системы мембран, либо синтеза отдельных ферментов.
Нарушения углеводного обмена
Молекулярные нарушения связаны с врожденной недостаточностью ферментов. К ним относятся врожденная недостаточность лактазы, сахаразы и пр. ферментов, расщепляющих дисахариды до моносахаридов, в связи с чем последние не могут всасываться в кровь и выводятся из организма с калом.
Основным клиническим биохимическим показателем нарушений углеводного обмена является изменение концентрации в крови глюкозы.
Гипергликемия – увеличение содержания глюкозы в крови.
Наиболее распространенная форма патологической гипергликемии – сахарный диабет, обусловленный дефицитом инсулина.
№39
1 Биоэнергетика окисления глицерина.
Окисление глицерина в тканях и клетках протекает при участии фосфорной кислоты.
2 Пути утилизации аммиака.


3 Витамины группы д.
Витамин D
Антирахитический витамин. Существуют два витамера:
D2 – эргокальциферол и D3 – холекальциферол.
Витамин D2 содержится в грибах. Витамин D3 синтезируется в организме под действием УФО (ультрафиолетового облучения):
7-дегидрохолестерол → холекальциферол (D3)
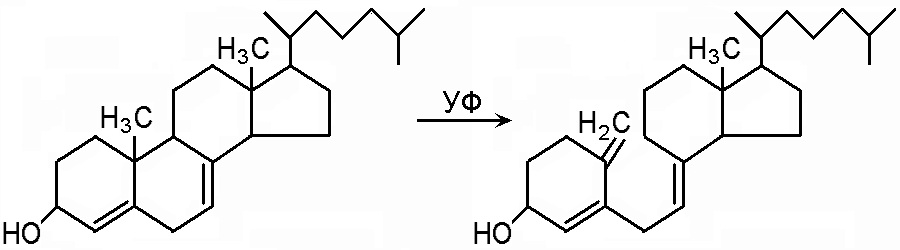
Роль витамина D в обмене веществ:
Витамин D3 (холекальциферол) подвергается в организме превращению. Он поступает в печень, где под действием 25-гидроксилазы превращается в 25-гидроксихолекальциферол, затем в почках под действием ПТГ и 1-гидроксилазы – в 1,25-дигидроксихолекальциферол (гормон кальцитриол)
Гиповитаминоз D приводит к снижению уровня кальция в крови, снижению кальция и фосфора в межклеточном пространстве, нарушению минерализации костной ткани.