Материал: Bilet_1
2.Определение аминокислотной последовательности белков с помощью секвенаторов.
Секвенирование по Эдману (1960).
0)Необходимо разорвать все дисульфидные связи и защитить цистеины от повторного замыкания, всё очень хорошо почистить.
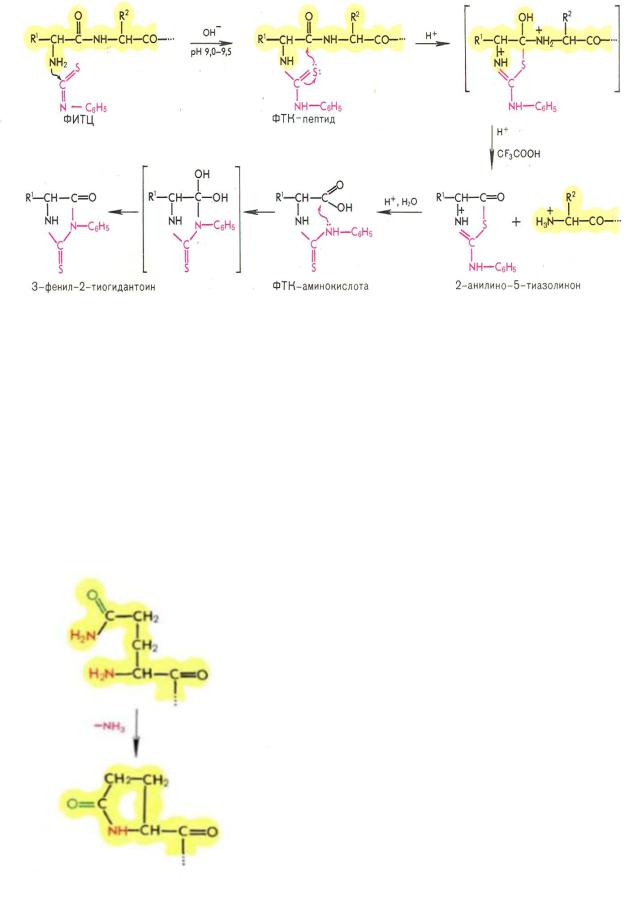
1)ФИТЦ (фенилизотиоцианат, мощный электрофильный агент) реагирует с незаряженной N-концевой аминокислотой в слабощелочных условиях, формируя ФТКпроизводное (фенилтиокарбомоил-производное).
Побочная реакция- в присутствии кислорода ФТКпроизводное пептидов десульфируется и не расщепляется. Также возможно блокирование аминогруппы альдегидами, находящимися в растворе с образованием основания Шиффа
2)При нагревании в безводной кислой среде происходит перестройка, циклизация продукта и отщепление пептида с образованием анилино-тиозолинон-производного и освобождении альфа аминогруппы.
Проблема здесь: если следующая аминокислота глутамин, то возможно превращение в пироглутамин, блокируется дальнейшая деградация.
А в случае связи Asn-Gly происходит образование циклического имида,затем альфа,бетатранспептидация, в итоге Эдман также блокируется.

Аминогруппа треонина серина легко гидролизуется в водной среде.Побочные реакии по остаткам аргинина и гистидина.
3) Анилино-тиазолинон экстрагируют из органического растворителя и добавляют к раствору водной кислоты, где формируется фенил-тиогидантоин – устойчивое производное аминокислоты, которое можно регистрировать с помощью хроматографии.
Существует большое число аналогов ФИТЦ, которые образуют тиогидантоины, обладающие рядом преимуществ по сравнению с ФТГ.
Наибольшее распространение получил (ДАБИТЦ).
В 1976 Эдманом и Бэггом был создан прототип автоматического жидкофазного секвенатора, где реакции были стандартизированы, был исключён контакт образца (нанесён на
твёрдую подложку из квадрола (нековалентно связан)) с воздухом, что привело к увеличению выхода реакции отщепления до 95%.
Далее группой под руководством Ларсена было придумана иммобилизация белка через различные боковые радикалы (в том числе по С-концу) на полистирольную матрицу (ковалентная иммобилизация). В 1981 году Худ и Ханкепиллер сконструировали газофазный секвенатор. Хитрая конструкция позволила значительно уменьшить расход реактивов, растворителей и исследуемого образца белка (до 100-500 пмоль).
Подробнее – со стр. 57 учебника Овчинникова.
3. N- и O-гликозилирование белков в гликопротеинах.
Гликопротеины – белки, содержащие ковалентно связанный углеводный компонент. Делят на 2 класса по количеству связанных олигосахаридных цепочек: протеогликаны – много сахара; собственно гликопротеины – много белка.
N-гликопротеины: Углеводный остаток присоединяется к амидному азоту остатка аспарагина (желательна непосредственная близость гидроксиаминокислот). Первым моносахаридом обычно оказывается N-ацетилглюкозамин, так что «узел» присоединения имеет следующую структуру:
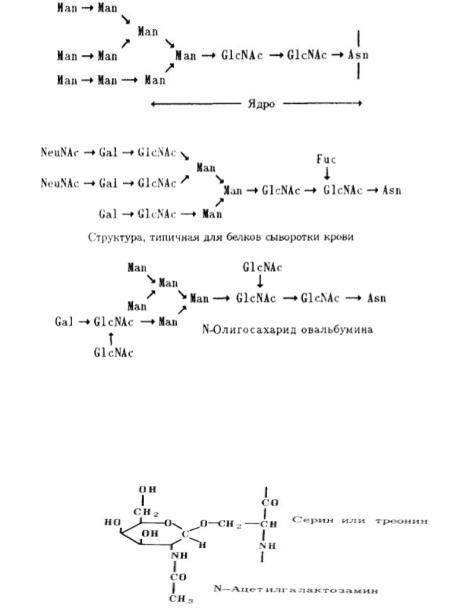
N-гликозидная связь легко расщепляется в кислой среде. В гликопротеинах этого типа к остатку аспарагина присоединен олигосахарид, в котором к «узловому» остатку N ацетилглюкозамина присоединен еще один остаток N-ацетилглюкозамина, далее следуют несколько остатков маннозы, галактозы, нейраминовой кислоты, фукозы и др. . Биосинтез N-гликопротеинов происходит в шероховатом ретикулуме, причём на амидную группу Asn переносится сразу большой-большой олигосахарид, включающий глюкозу, маннозу, ацетилглюкозамин, который подвергается процессингу (обязательное удаление глюкозы и удаление/добавление других сахаров).
Остается ядро, к которому присоединяются другие сахара.
Дальнейшие реакции специфичны, вот как пример
N-гликозилирование характерно для секреторных белков, попадающих в ЭПР, хотя оно не является непременной предпосылкой секреции.
O-гликопротеины
Углеводный остаток присоединяется к оксигруппе Ser или Thr (однозначного сиквенса для гликозилирования нет). Первый моносахарид – N-ацетилгалактозамин.
Биосинтез ступенчатый, всё по порядку, количество моносахаридов не такое большое. О- гликозилирование свойственно веществам, определяющим группу крови (муцины).
Углеводный компонент почти никогда не входит в состав каталитического центра, наличие гликозилирования обычно не влияет на скорость ферментативной реакции. Зато олигосахариды в составе гликопротеинов участвуют в процессах межклеточного узнавания, дифференциации, трансформации клеток, связывании гормонов с рецепторными белками.
Билет 10 1. Сортинг белков в эу-клетке. Сигнальные пептиды. Везикулярный транспорт.
Контрансляционный транспорт в ЭПР Осуществляется по мере синтеза белка. Сигнальная последовательность – 5-10 обычно
гидрофобных аминокислот на N-конце + последовательность для протеазки на удалённом участке. После синтеза сигнальной последовательности в цитоплазме, комплекс SRP (signal-recognition particle) блокирует трансляцию и связывает рибосому с SRP-рецептором на ЭПР. Далее комплекс мРНК-рибосома-SRP связывается с транслокатором, происходит диссоциация SRP, трансляция возобновляется, белок направляется внутрь ЭПР. После окончания трансляции рибосома уходит в цитозоль, сигнальная последовательность (гидрофобная, держится в мембране) отрезается протеазой, белок же оказывается в ЭПР, где претерпевает необходимый фолдинг.
Посттрансляционный транспорт в ЭПР Транспорт, при котором полностью синтезированный белок связывается в цитозоле с
шаперонами, а затем переносится в ЭПР через транслокатор при участии шаперонов семейства Hsp70. Этот вид транспорта является АТФ-зависимым. Для транспорта пептидов (длиной 8-16 аминокислот) из цитозоля в ЭПР для последующей их презентации в комплексе с молекулами MHC-I существует специальный транслокатор — TAP-белок.
Транспорт белов из ЭПР в АГ (аппарат Гольджи)
Белки поступают из ЭПР в АГ внутри окаймленных мембранных пузырьков, оболочка которых образуется из белка COP-II. Все правильно свернутые перемещаются в АГ. Однако белки со специальными сигнальными метками концентрируются в транспортных пузырьках. Отделившиеся от ЭПР пузырьки, сливаются в трубчато-везикулярные кластеры, которые с помощью моторных белков перемещаются по микротрубочкам к АГ. От этих кластеров отделяются пузырьки, одетые белком COP-I, обеспечивающие обратный транспорт белков в ЭПР. Возврат белков в ЭПР обеспечивается короткой сигнальной последовательностью на их С-конце, которая связывается либо непосредственно с COP-I (для мембранных белков), либо со специфическим рецептором, взаимодействующим с COP-I (для растворимых белков). Лишенные этих последовательностей белки преимущественно остаются в АГ.
Внутри пузырьков белки постепенно перемещаются из цис-Гольджи в транс-Гольджи. По мере перемещения белков внутри АГ ферменты гликозилтрансферазы осуществляют модификацию их олигосахаридных «меток».
Транспорт белков из АГ в лизосомы.
Мембранные белки и пищеварительные ферменты лизосом поступают из транс-Гольджи в составе окаймленных клатрином пузырьков в раннюю эндосому, а оттуда — в лизосомы. Для попадания лизосомальных ферментов в лизосомы на них должна присутствовать специальная метка
— остатки маннозо-6-фосфата на концах олигосахаридных цепей. Метка наносится на те белки, которые имеют специфические черты третичной структуры — «сигнальный бугорок». Затем маннозо-6-фосфаты опознаются специфическим мембранным рецептором, к которому присоединяются гидролазы. В эндосомах при понижении рН гидролазы отделяются от рецепторов, которые в составе специальных пузырьков доставляются обратно а АГ.
Транспорт в ядро (см. билет №9)
Транспорт в митохондрии
До наружной мембраны митохондрии пре-белки транспортируются в частично развёрнутом состоянии в ассоциации с белками-шаперонами (в частности — с hsp70). После переноса через наружную и внутреннюю мембраны, поступающие в митохондрию белки вновь связываются с шаперонами, но уже собственного митохондриального происхождения. Сам механизм немного похож на ядерный импорт, белки переносчики называются TOM (Translocase of Outer Membrane). Сигнал локализации удаляется митохондриальным Hsp70.
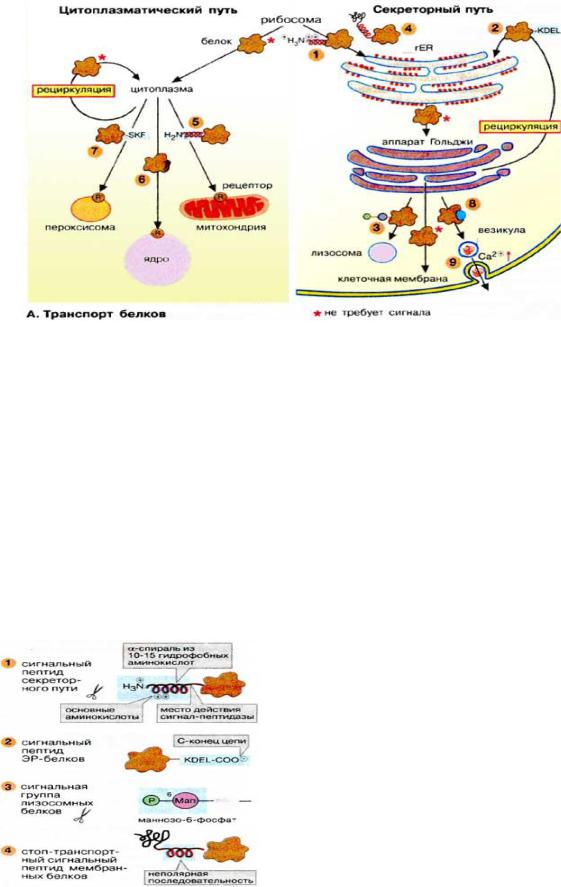
Билет 10 1. Сортинг белков в эукариотической клетке. Сигнальные пептиды. Везикулярный транспорт.
Биосинтез белков начинается на свободных рибосомах . Однако вскоре пути синтезируемых белков расходятся в соответствии с их функцией: белки, несущие на N-конце сигнальный пептид для ЭР , проходят через секреторный путь, а прочие белки, не имеющие этой сигнальной последовательности, следуют по цитоплазматическому пути .
Секреторный путь. Рибосомы, синтезирующие белок с сигнальной для ШЭР последовательностью, связаны с мембраной ЭПР. Растущая пептидная цепь направляется через мембрану в просвет ШЭР. Последующий путь растущей цепи определяется наличием соответствующего сигнального пептида или сигнального участка - разные вещи-
Белки, имеющие в растущей цепи специальную стоп-сигнальную последовательность (4), остаются в мембране ШЭР в качестве интегрального мембранного белка. По механизму везикулярного транспорта они могут быть перенесены из ШЭР на другие органеллы
Белки, попавшие в просвет ШЭР, транспортируются обычным путем в аппарат Гольджи и далее
вплазматическую мембрану. Белки, которые остаются в ШЭР, например ферменты модификации белков, возвращаются из аппарата Гольджи в ШЭР с помощью сигнала возврата (2)
Прочие белки из аппарата Гольджи попадают в лизосомы или в плазматическую мембрану (в качестве интегральных мембранных белков или продуктов конститутивного экзоцитоза), либо транспортируются секреторными везикулами (8) в межклеточное пространство (9; регулируемый экзоцитоз).
Цитоплазматический путь. Белки, не имеющие сигнального пептида для ШЭР, синтезируются
вцитоплазме на свободных рибосомах и остаются в этом отделе клетки. Для последующего
транспорта в митохондрии, ядро или пероксисомы белки
должны |
иметь |
специальные |
сигнальные |
последовательности.
Сигналы для сортировки белков Сигнальные пептиды — это короткие участки,
расположенные на N- и С-концах, реже — в центральной части полипептидной цепи. Эти фрагменты имеют характерные физико-химические свойства, такие, как гидрофобный характер, наличие положительного или отрицательного заряда, более важные в функциональном отношении, чем аминокислотная последовательность.
Сигнальные участки представляют собой трехмерные структуры на поверхности белка, составленные из
различных фрагментов одной и той же или нескольких