Материал: Bilet_1
Билет №1.
1. Шаперонины про- и эукариот.
Шаперонины – группа шаперонов, ролью которых является временное экранирование белка от окружающей среды. Эти белки представляют собой олигомерные комплексы (14-16 субъединиц), имеющие форму «бочонка» с центральной полостью, в которую активно (с затратой АТФ) заключается развернутый белок. Полость формируется двумя состыкованными кольцами из 7-8 субъединиц. Шаперонины разделяют на два класса: I и II, присутствующие в прокариотах (I) и эукариотах и архебактериях (II), причём они радикально отличаются по связыванию белковых субстратов.
К группе I шаперонинов относится хорошо изученный шаперонин GroEL из Escherichia coli, состоящий из 14 идентичных субъединиц, выстроенных в два состыкованных кольца по 7 мономеров в каждом. «Закрывание» этого шаперонина происходит с помощью «крышки» — кофакторагептамера GroES, присоединяющегося к GroEL после связывания последнего с АТФ.
Шаперонины группы II, обнаруженные в эукариотах и архебактериях, хотя и устроены схожим образом, существенно отличаются от бактериальных шаперонинов. Во-первых, они не являются гомоолигомерами — так, каждое из колец шаперонина TRiC (также известного под аббревиатурой CCT) состоит из восьми различающихся, хотя и родственных субъединиц. Во-вторых, у этих шаперонинов нет отдельной «крышки» — доступ во внутреннюю полость может перекрываться апикальными участками тех же молекул, что образуют сам шаперонин. Отличия в устройстве позволяют шаперонинам группы II взаимодействовать со многими исключительно эукариотическими белками — например, актином, который не может быть корректно свёрнут при участии бактериальных шаперонинов.
Два кольца шаперонина TRiC работают подобно двухтактному двигателю, — когда одно кольцо замыкается, открывается второе, «выпуская на волю» уже свернувшийся в недрах шаперонина белок. Время, в течение которого белок находится в полости, очень важно — ведь и слишком короткий, и слишком длительный срок приведёт к получению неработоспособного белка; однако механизмы, регулирующие эту длительность, пока совсем не изучены.
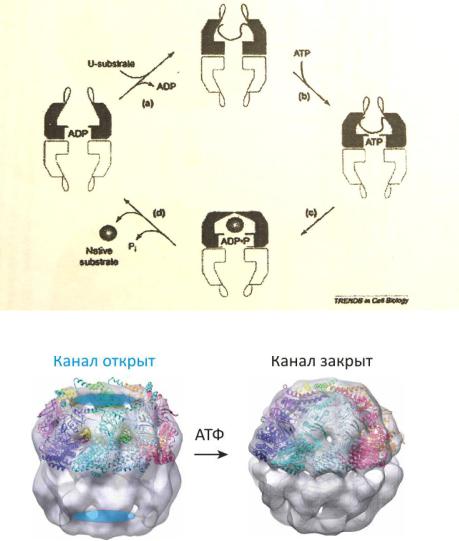
Устаревший механизм действия:
Модель, предложенная Джудит Фридман в 2008 году (на основе криомикроскопического анализа высокого разрешения):
Переход из открытой формы в закрытую связан с потреблением АТФ. Сворачиваемый белок, попадающий в результате этого на какое-то время в изолированное пространство внутри шаперонина, приобретает требуемую конформацию, после чего выходит из противоположных «ворот» шаперонина. Механизм открывания и закрывания канала эукариотического шаперонина напоминает действие диафрагмы фотоаппарата.
Компьютерная реконструкция работы шаперонина позволила выявить разные механизмы в эволюционно родственных белках — шаперонинах групп I и II. Однако многие детали работы шаперонинов так и остаются непонятыми.
2. Анализ аминокислотного состава белка. Определение N- и C-концевых аминокислот.
Для определения аминокислотной последовательности белка прежде всего разделяют его полипептидные цепи (если макромолекула состоит из нескольких цепей). Затем определяют аминокислотный состав цепей, N- и С-концевые аминокислотные остатки и аминокислотные последовательности. Полипептидные цепи подвергают специфическому расщеплению протеолитическими ферментами или хим. реагентами. Смесь образовавшихся фрагментов разделяют и для каждого из них определяют аминокислотный состав и аминокислотную последовательность. При необходимости крупные фрагменты дополнительно расщепляют на более мелкие. Порядок расположения фрагментов выясняют путем расщепления молекулы белка по др. связям и анализа образующихся при этом "перекрывающихся" фрагментов.
Анализ аминокислотного состава включает полный гидролиз исследуемого белка или пептида и количественное определение всех аминокислот в гидролизате. Для гидролиза обычно используют 5н водный р-р НСl, а при анализе содержания триптофана – 4н метансульфоновую к-ту, содержащую
0,2% 3-(2-аминоэтил) индола, или кипячение со щелочью. Количественное определение аминокислот в гидролизате проводят с помощью аминокислотного анализатора. В большинстве таких приборов смесь аминокислот разделяют на ионообменных колонках, детекцию осуществляют спектрофотометрически по реакции с нингидрином или флуориметрически с использованием флуорескамина или о-фталевого диальдегида. В последнем случае можно анализировать до 0,1-0,05 нмоль аминокислоты.
Наибольшее распространение для определения N-концевых остатков находит дансильный метод. Его первая стадия – присоединение дансилхлорида (1-диметиламинонафталин-5-сульфохлорида) к непротонированной α-аминогруппе с образованием дансилпептида (ДНС-пептида). Затем последний гидролизуют 5,7 н р-ром НСl при 105 °С, в результате чего освобождается N-концевая α-ДНС- аминокислота, которая обладает интенсивной флуоресценцией в УФ-области спектра; для ее идентификации достаточно 0,1-0,5 нмоль вещества.
Для определения С-концевых остатков чаще всего используют ферментативный гидролиз карбоксипептидазами, которые специфически расщепляют пептидные связи, образованные С- концевыми остатками. Поскольку после отщепления концевых остатков фермент атакует последующие пептидные связи, измерение скорости отщепления отдельных аминокислот позволяет анализировать также и С-концевую аминокислотную последовательность.
Важнейший этап в определении первичной структуры белка – расщепление макромолекулы на пептидные фрагменты. Среди ферментативных методов расщепления наиболее широко используется гидролиз трипсином. Трипсин обладает уникальной субстратной специфичностью: гидролизует исключительно связи, образованные карбоксильными группами основных аминокислот – лизина и аргинина. Введение заместителей в боковые цепи лизина или аргинина препятствует гидролизу по остаткам модифицированных аминокислот и позволяет гидролизовать макромолекулы избирательно только по остаткам аргинина или лизина. Особенно часто используется модификация остатков лизина с последующим гидролизом белков по остаткам аргинина. Модифицирующие агенты – ангидриды дикарбоновых кислот (янтарной, малеиновой и цитраконовой). Из других протеолитических ферментов широко применяется протеаза из Staphylococcus aureus (гидролизует связи, образованные карбоксильными группами остатков глутаминовой кислоты, а в некоторых случаях и остатков аспарагиновой кислоты), а также химотрипсин и термолизин. Последние ферменты обладают более широкой специфичностью. Химотрипсин катализирует гидролиз пептидных связей, образованных карбоксильными группами ароматических аминокислот: тирозина, фенилаланина и триптофана. С меньшей скоростью гидролизуются связи лейцина, метионина и гистидина. Термолизин преимущественно расщепляет связи, образованные аминогруппой остатков с
гидрофобной боковой цепью (изолейцин, лейцин, валин, фенилаланин, тирозин, триптофан).
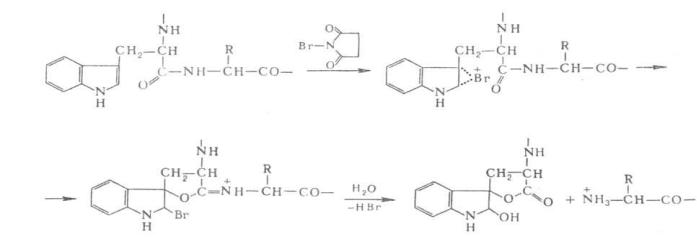
Для расщепления белков по карбонильной группе остатка триптофана используют N- бромсукцинимид или более селективный (BNPS-скатол):
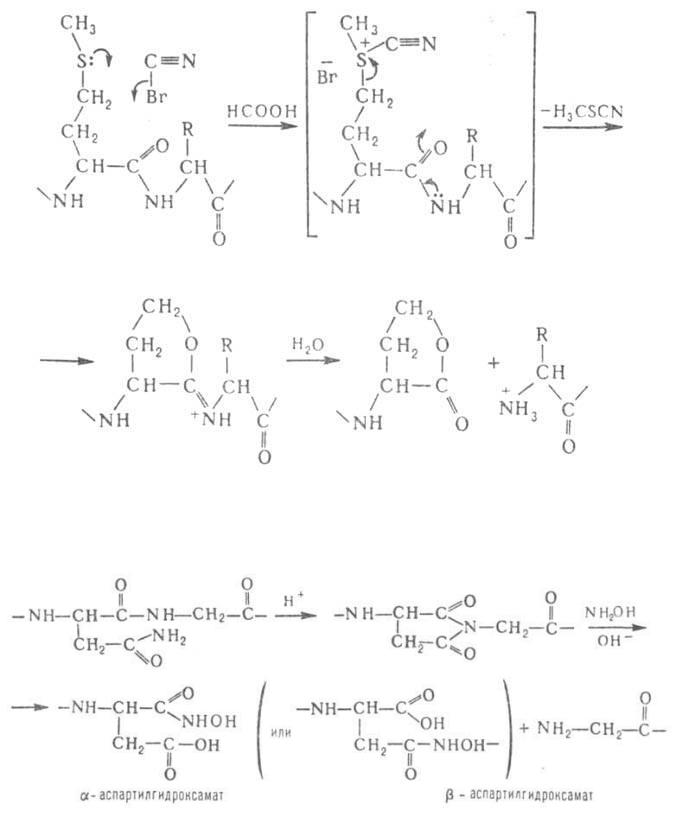
Из химических методов расщепления белков наиболее специфичный и чаще всего применяемый - бромциановое расщепление по остаткам метионина (выход 90-100%):
Гидроксиламин расщепляет пептидные связи между остатками аспарагина и глицина. При его взаимодействии с циклическим имидом ангидроаспартилглицина, спонтанно образующегося из аспарагинилглицина, в щелочной среде происходит расщепление пептидной цепи с образованием смеси α- и β-аспартилгидроксаматов:
В ряде случаев для расщепления белков используется метод частичного кислотного гидролиза. Наиболее чувствительны к действию кислот аспартильные пептидные связи и особенно связь аспартил - пропил.
При выборе методов разделения пептидов учитывают физ.-хим. свойства, кол-во и длину молекул разделяемых соединений. Для первичного фракционирования смесей коротких пептидов, содержащих до 15-20 аминокислотных остатков, в большинстве случаев используют ионообменную хроматографию на катионитах. Дальнейшее разделение и очистку проводят с помощью
хроматографии и электрофореза на бумаге или пластинках с тонким слоем целлюлозы или силикагеля.
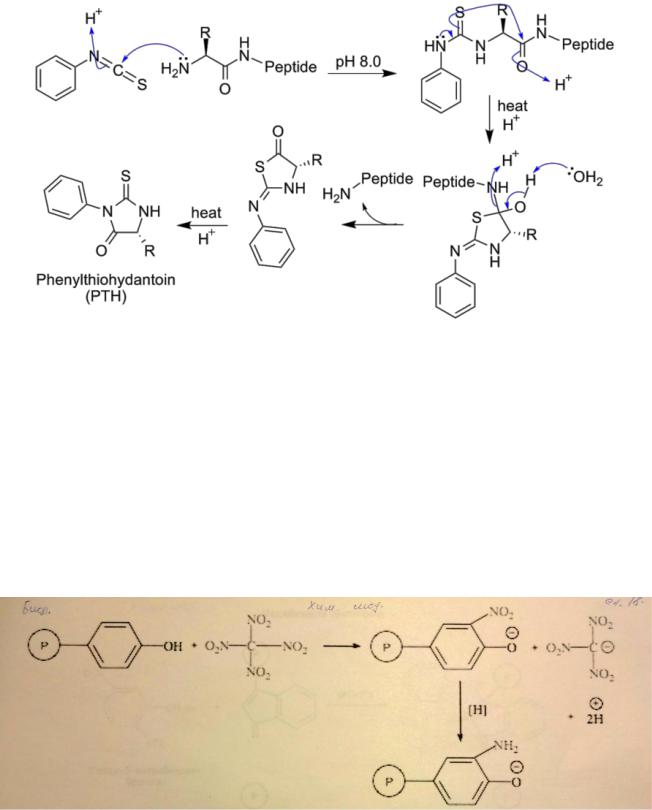
Осн. метод исследования аминокислотной последовательности пептидов и белков - хим. деградация с помощью фенилизотиоцианата. Этот метод позволяет последовательно отщеплять N-концевые аминокислотные остатки в виде фенилтиогидантоинов, к-рые абсорбируют свет в УФ-области с максимумом поглощения 265-270 нм. Для их идентификации наиб. часто используют тонкослойную хроматографию, жидкостную хроматографию высокого давления, а также масс-спектрометрию. Широкое применение нашел также метод, сочетающий последовательную деградацию пептида по Эдману с анализом N-концевых аминокислотных остатков в виде их дансильных производных. Достоинство метода -его высокая чувствительность.
Для непосредственного анализа первичной структуры белков обычно используют секвенатор - прибор, который с высокой эффективностью осуществляет последовательное автоматическое отщепление N-концевых аминокислотных остатков путем деградации белков по методу Эдмана.
3. Химическая модификация остатков тирозина и триптофана в белках.
Химические свойства тирозина определяются возможностями фенольной группы. Основные реакции химической модификации в данном случае – это реакции электрофильного замещения в ароматическом кольце.
Для модификации остатков тирозина в молекулах белков используют нитрование тетранитрометаном и иодирование ароматического кольца, ацетилирование гидроксигруппы, реакции с бромсукцинимидом, цианурфторидом и диазониевыми соединениями. В пептидном синтезе фенольный гидроксил остатка тирозина защищают бензильной, 2,6-дихлорбензильной или трет-бутильной группой.