Материал: Bilet_1

Частным случаем биоспецифической модификации является фотоаффинная модификация, основанная на использовании производного природного лиганда, содержащего фотореактивную группировку. При облучение происходит образование радикалов, способных реагировать с самыми различными группировками белковых молекул в местах наиболее тесного контакта с лигандом. В качестве предшественников активированных соединений обычно применяют разнообразные производные арилазидов и диазосоединений, генерирующие при фотолитическом разложении нитрены и карбены, соответственно:
Преимущество метода заключается в возможности проводить модификацию на любом этапе действия системы, однако выход целевых продуктов взаимодействия (радикалов с белком), как правило, низок из-за внутримолекулярных перегруппировок радикалов и других конкурирующих процессов. Таких проблем удаётся избежать при использовании радиоактивно меченных фотоаффинных реагентов.
В качестве примера можно рассмотреть локализацию в ДНК-зависимой РНК-полимеразе участков, контактирующих с 5'-концевой группой синтезируемой РНК. Были подобраны условия, при которых фермент способен синтезировать олигонуклеотиды определённой длины, содержащие 5'-концевую фотореактивную (γ-азидоанилидную) группу. После облучения транскрипционного комплекса светом в зависимости от длины синтезированного олигонуклеотида модифицировались различные субъединицы фермента. В частности, в случае динуклеотида модифицировалась β- субъединица, а в случае тетрануклеотида – β’-субъединица. Полученные результаты свидетельствовали о том, что центр связывания продукта изменяется в процессе синтеза РНК.
Билет 3 1. Импорт белка в эндоплазматический ретикулум.
Синтез основной массы белков протекает на полисомах в цитозоле. Особенность цитоплазматического синтеза белков заключается в том, что в зависимости от типа мРНК синтезируются различные белки, направляющиеся строго к своим внутриклеточным компонентам (связь мРНК-компартментализация). Это связано с тем, что разные по назначению белки имеют определенные сигнальные последовательности аминокислот, по которым разные молекулы распределяются в клетке.
В отличие от этих типов белков, белки экспортного назначения (пищеварительные ферменты, белки плазмы крови, гормоны и др.) и белки мембран (рецепторы) синтезируются на рибосомах, расположенных на мембранах эндоплазматического ретикулума и попадают внутрь вакуолей по мере синтеза полипептидной цепи, котрансляционно. Затем эти белки в составе или внутри вакуолей транспортируются по клетке.
За котрансляционный синтез растворимых внутривакуолярных белков и нерастворимых белков, входящих в состав мембран вакуолярной системы ответственен гранулярный эндоплазматический ретикулум (в народе называемый шероховатым). В нем же происходит первичная посттрансляционная модификация белков – их соединение с олигосахаридами (перв. гликозилирование). Дальнейшая судьба синтезированных продуктов определяется аппаратом Гольджи (вторичное гликозилирование, адресация по секреторному пути, по пути образования эндосом, экстрацеллюлярных рецепторов).
Гранулярным ЭПР был назван по наличию рибосом на мембране со стороны гиалоплазмы. Рибонуклеопротеиды расположены на мембране в виде полисом (множество рибосом, объединенных одной мРНК), имеющих вид плоских спиралей, розеток или гроздей. Это работающие, синтезирующие белок рибосомы, прикрепленные к мембранам своей большой субъединицей. Количество рибосом на ЭПР четко связано с его синтетической активностью. Так, на мембранах ЭПР в клетке несекретирующей молочной железы связывается до 25% клеточных рибосом, а после стимуляции лактации их кол-во там возрастает до 70%. Падение числа рибосом на мембранах ЭПР может происходить при дифференцировке клеток. Такое же уменьшение числа рибосом, связанных с ЭПР, наблюдается при различных патологических состояниях клеток.
Путь синтеза белков на рибосомах ЭПР таков: в гиалоплазме происходит связывание мРНК с рибосомой, начинается синтез полипептидной цепи, начинающийся с продукции сигнальной последовательности, богатой гидрофобными аминокислотами (16-30 остатков). Эта последовательность связывается с «узнающей сигнал частицей», находящейся в гиалоплазме (SRPчастица), состоящей из одной молекулы 7S РНК и 6 различных полипептидных цепей. Затем SRPчастица связывается с рибосомой, что приводит к полной остановке синтеза белка. На поверхности мембраны ЭПР, обращенной к гиалоплазме, расположены интегральные рецепторы, связывающиеся с SRP-частицами в комплексе с рибосомой. Такая «заякоренная» рибосома с SRP-частицей взаимодействует с большим белковым канальным комплексом – транслоконом. В результате связывания рибосомы с транслоконом происходит отделение SRP-частицы, и синтезированный первичный пептид входит в канал транслокона диаметром около 2 нм и продолжает синтезироваться. Сигнальная последовательность оказывается внутри ЭПР, где отщепляется с помощью сигнальной пептидазы. После окончания синтеза вся белковая молекула располагается в полости ЭПР, рибосома отделяется от транслокона и диссоциирует. Во время трансмембранного переноса растущей белковой цепи (т.е. котрансляционно) происходит её связь с олигосахаридами (гликозилирование): на белковую молекулу (на остатки аспарагина) переносится готовый блок олигосахаридов (2 молекулы N-ацетилглюкозамина, 9 молекул маннозы, 3 молекулы глюкозы), изначально связанный со специальным липидом на внутр. мембране ЭПР – долихолом. Перенос катализируется интегральным ферментом гликозилтрансферазой.
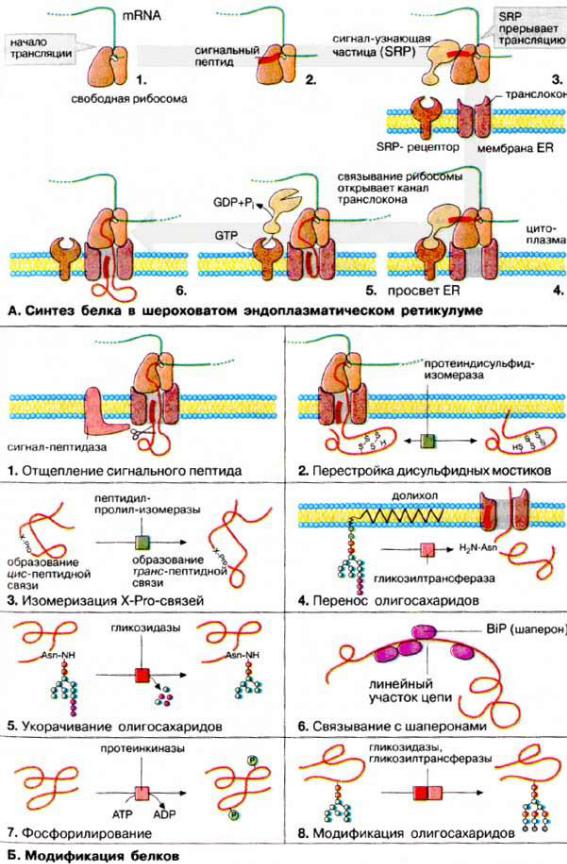
Попадая в полость цистерн ЭПР, белки претерпевают ряд дополнительных изменений: образуются дисульфидные связи, происходит правильное сворачивание и сборка четвертичной структуры белков.
2. Химический метод расщепления полипептидной цепи белка по остатку Met
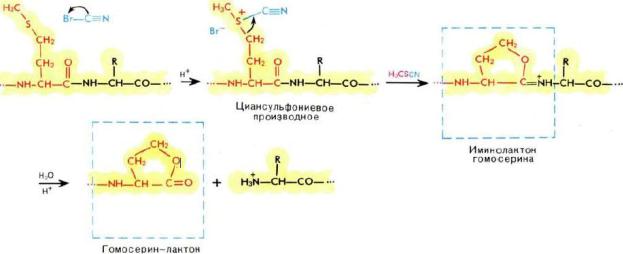
Среди химических методов фрагментации белков наиболее специфичным и чаще всего применяемым является расщепление бромцианом по остаткам метионина. Метод разработан в 1961 г. Э. Гроссом и Б. Виткопом и по избирательности действия не имеет себе равных. Реакция с бромцианом проходит с образованием промежуточного циансульфониевого производного метионина, спонтанно превращающегося в кислых условиях в иминолактон гомосерина, который, в свою очередь, быстро гидролизуется с разрывом иминной связи. Получающийся на С-конце пептидов лактон гомосерина далее частично гидролизуется до гомосерина (HSer), в результате чего каждый пептидный фрагмент, за исключением С-концевого, существует в двух формах — гомосериновой и гомосеринлактоновой.
Реакцию обычно проводят при комнатной температуре в течение 15—30 ч в сильнокислой среде (чаще всего в 70%-ной муравьиной кислоте) при 100-кратном избытке бромциана на каждый остаток метионина. В этих условиях связи, образованные остатками метионина, обычно расщепляются на 90—100%. Исключение составляют связи метионина с серином и треонином, расщепляющиеся лишь частично. В условиях обработки белка бромцианом может иметь место частичный гидролиз связи Asp—Pro, неустойчивой в кислой среде.
3. Кросс-сшивающие реагенты, классификация. Задачи, решаемые с помощью них
Говоря о кросс-сшивающих реагентах, имеют в виду создание конъюгатов молекул – соединений, сочетающих в себе свойства всех конъюгированных между собой веществ. Широко известным случаем применения конъюгации является «пришивание» фермента пероксидазы к молекуле антитела при получении конъюгата, применяемого в ИФА. Кроме того, конъюгацию применяют для мечения молекул флюоресцеирующим агентом или специфическим лигандом (биотинилирование, конъюгация со стрептавидином). Дизайн и синтез наночастиц: функционализация последних с помощью адресных агентов (антител, лигандов, рецепторов) или активных компонентов (ферментов, токсинов) – одна из основных задач нанобиотехнологии. А за
нанобиотехнологией – будущее, в том числе лечение рака, таблетка от бедности, нанороботы, путешествующие по кровотоку и поколачивающие вредных микробов, и другие незаменимые вещи.
Для каждой операции конъюгации необходимо подбирать наиболее подходящий реагент, опираясь на свойства «сшиваемых» молекул. В большинстве случаев это белки, т.е., задействуют следующие функциональные группы: α-COOH С-концевой аминокислоты; α-NH2 N-концевого аминокислотного остатка; ионизируемые боковые цепи остатков Asp, Glu, Lys, Arg, Cys, His, Tyr.
В депротонированном состоянии перечисленные группы являются потенциальными нуклеофилами, на что и ориентируется большинство реакций конъюгации. Также для конъюгации могут быть использованы олигосахаридные остатки гликопротеинов.
Системы, используемые для конъюгации биологических молекул, невероятно разнообразны. По результатам реакции и по химической структуре сшивающие реагенты делят на:
1. Конъюгирующие реагенты нулевой длины (связь образована изначальными соединениями).
2.Гомобифункциональные кросслинкеры (X-R-X).
3.Гетеробифункциональные кросслинкеры (X-R-Y).
4.Трифункциональные кросслинкеры (X-R(-Y)2).
5.Кросслинкеры, образующие расщепляемую связь (X-R≈R1-Y).
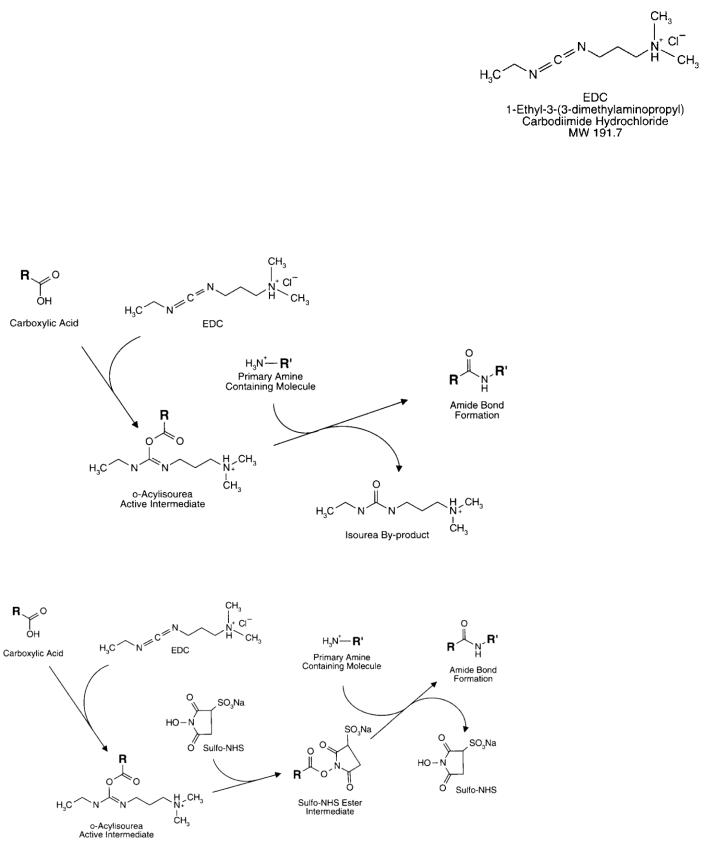
Кросслинкеры нулевой длины – вещества, таким образом активирующие группы, имеющиеся в субстратах, что они становятся способными к присоединению. Самыми популярными реагентами этого класса являются карбодиимиды, участвующие в реакции образования амидной связи (между карбоксильной группой и аминогруппой). Наиболее часто используемое вещество – EDC (1-этил-3- (3-диметиламинопропил)карбодиимид хлорид) хорошо растворяется в воде, что выгодно отличает его от родственных
соединений. В результате реакции EDC с карбоксильной группой образуется активное промежуточное соединение о- ацилизомочевина, имеющее реактивную эфирную связь. Такое соединение легко вступает в реакцию с молекулами, содержащими первичную аминогруппу. В качестве побочного продукта образуется изомочевина, что создаёт помехи при
дальнейшем использовании конъюгата. Избежать таких проблем можно либо постреакционной очисткой конъюгата, либо добавлением в реакционную смесь N-гидроксисульфосукцинимида (NHS), образующего более устойчивый эфир с карбоксильным агентом.
Реакция конъюгации с использованием карбодиимида:
В случае добавления сукцинимида: