Материал: Bilet_1
Если рибосомальная трансляция стандартным набором из 20 L-аминокислот,то нерибосомальные пептиды м. содержать необычные строительные блоки, включая D-аминокислоты, метилированные варианты стандартных аминокислот и непротеиногенные, гидроксилированные и гликозилированные остатки; сейчаст известно более 300 предшественников. Иногда пептидные продукты являются гетероцикличными, а пептидный остов м.б. разветвлен.
How are the peptides made? Нерибосомальные пептиды создаются на массивных линейных синтетазах. Эти энзимы являются модулярными, т.е. представлены серией функциональных единиц, которые м. связывать голые аминокислоты, активируя их как тиоэфир и присоединяя их к растущей пептидной цепочке. При линейных NRPSs, последовательности модулей действуют как матрицы, которые и предопределяют конечные последовательности пептидов. Но существуют также и повторяющиеся и нелинейные конфигурации NRPS, которые генерируют более сложные структуры.
Большинство NRP's модификаций являются преформированными во время синтеза или за счет сборки линейных компонентов, или внешними белками. Др. модификации м.б. добавлены после синтез. Некоторые синтетазы являются мультимерными комплексами, тогда как др. являются одиночными, массивными белками. Каждый модуль состоит примерно из 1,000-1,200 аминокислот, это делает энзимы ненормальными: одиночный в 15,281-остатков (1.7 MDa) белок, напр., синтезирует циклоспорин, иммуносупрессант в 11-остатков длиной.
Why is this important? NRPS продуцирует несколько фармакологически важных соединений, включая циклоспорин и антибиотики пенициллин и ванкомицин. Если исследователям удастся выяснить у пептидных синтетаз "генетическиий код," то они смогут манипулировать им, чтобы продуцировать новые соединения с лекарственными свойствами.
2. Химическая модификация остатков тирозина в белке, введение тиольной группы в остаток триптофана.
Гидроксильные группы тирозина в белках располагаются частично внутри, частично на поверхности белковой глобулы. В последнем случае для них характерен рКа>> 10, соответствующий
переходу:
-CH2-C6H4 –OH  -CH2-C6H4-O—
-CH2-C6H4-O—
Образующийся при этом фенолят-ион весьма активно вступает в реакции, свойственные также ε- аминогруппам лизина.
1)Ацилирование. Например присоединение ацетилимидазола.
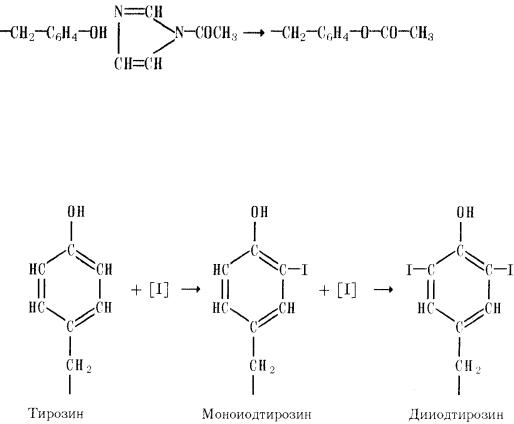
2)Иодирование. Эту реакцию часто применяют как способ внедрения реактивных изотопов иода в белковую молекулу. Источником атомов иода может служить комплекс иода и йодистого калия; в некоторых случаях используют иод, образующийся при окислении иодид-иона в присутствии фермента пероксидазы. Иодирование приводит к образованию как моно-, так и дийодтирозина, причем замещение идет в о-положение:
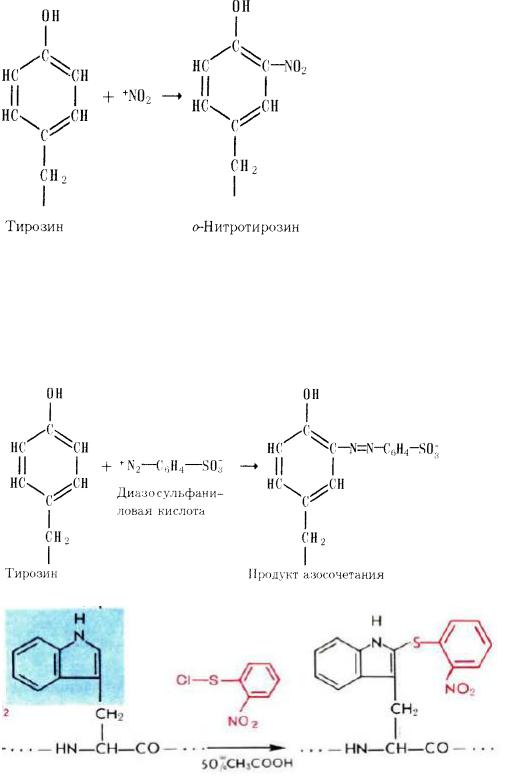
3) Нитрование. Нитрование достигается действием тетранитрометана С(NO2)4 , причем в роли активной частицы обычно выступает нитроний-катион NO2+
Введение второй нитрогруппы возможно в о-положение.
4) Азосочетание. Реакция остатков тирозина с ароматическими солями диазония, также, являющимися катионными реагентами, опять-таки приводит к образованию моно- и ди-о-замещенных продуктов с достаточно протяженной системой сопряженных двойных связей, сто придает им красно-оранжевое окрашивание в реакции Паули (р-р белка смешивают со свежеприготовл. р-ром n-диазобензолсульфокислотой в присут. Na2CO3.) Эта реакция приводит к усилению кислотных свойств гидроксильной группы тирозина.
Введение тиольной метки в триптофан:
После этого нужна только обработка меркаптаном и вот тиольная группа уже радует глаз!
3. Убиквитинирование как механизм специфической деградации белков в клетке.
Убиквитинирование — это посттрансляционное присоединение ферментами убиквитинлигазами одного или нескольких мономеров убиквитина с помощью ковалентной связи к боковым аминогруппам белка-мишени. биквитин (от англ. ubiquitous — вездесущий) — небольшой консервативный белок, который у эукариот присоединяется к белкам. Присоединение убиквитина влияет на внутриклеточную локализацию и функцию белков. Самым первым открытием стала деградация белков, помеченных мультиубиквитиновыми цепями, с помощью 26S- протеасомы.
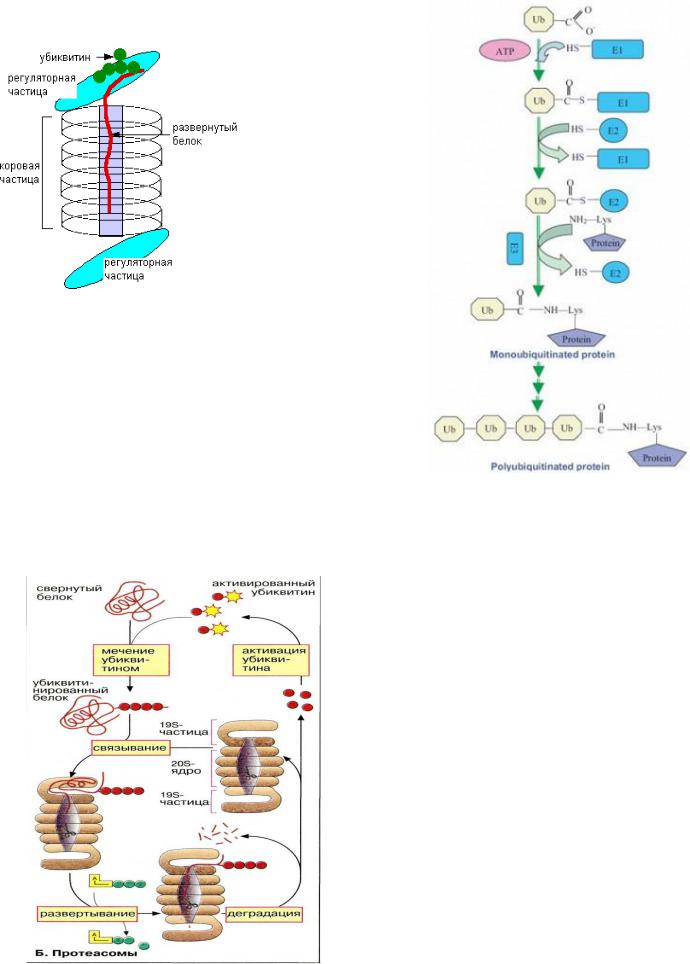
Протеасома построена из центрального кора, состоящего из 14 белковых димеров, по 7 в кольцевой структуре. Всего 4 кольца расположенных друг над другом; две регуляторные части с двух сторон от кора, 14 белков в каждой, 6 из которых ATP-
азы. Некоторые из субъединиц узнают убиквитин - белок, состоящий из 76 аминокислот. (рис.1).
рис.1 Схема протеасомы. Белок
подвергающийся протеолизу соединяется лизиновым остатком с С- концом убиквитина (рис.2),дополнительные молекулы убиквитина присоединяются формируя цепь, которая связываетя с регуляторной частью протеасомы. Степень убиквитинирования имеет
разные последствия для белка. Например, 48 остатков убиквитина присоединенные к белку служат сигналом протеасомного разрушения, тогда как 63 остатка служат посттрансляционным сигналом в различных клеточных процессах, таких как ДНК репарация, актвация транскрипционных факторов и др.
Рис.2 Схема присоединения убиквитина к белку и участие различных ферментов. Фермент Е1 активирует С-конец убиквитина, используя энергию АТФ, аденилированием и переносом тиоэфирной связи с цистеина на E1. Фермент Е1 переносит убиквитин к
транспортноми ферменту Е2, который при помощи Е3 лигазы присоединяет его к субстрату. Было обнаружено несколько генов кодирующих Е1, десятки генов Е2 и сотни Е3. Используя разные комбинации ферментов клетка регулирует какой белок должен быть разрушен и скорость распада. Развернутый белок перемещается в пространство коровой частицы, где специфически разрезается на короткие пептиды ~8 аминокислот, которые впоследствии могут быть разрушены пептидазами цитозоля.
Билет 15
1. Химическая модификация карбоксильных групп, остатков Tyr и Met в белках. Реакции карбоксильной группы:
1) Реакция с аминами в присутствии карбодиимидов (реакция Хоблина-Корано). Эту реакцию проводят в воде, используя водорастворимые карбодиимиды, например –этил-N-
триметиламинопропилкарбодиимид: С2H5 –N=C=N-CH2- CH2-+N(CH3)3I-
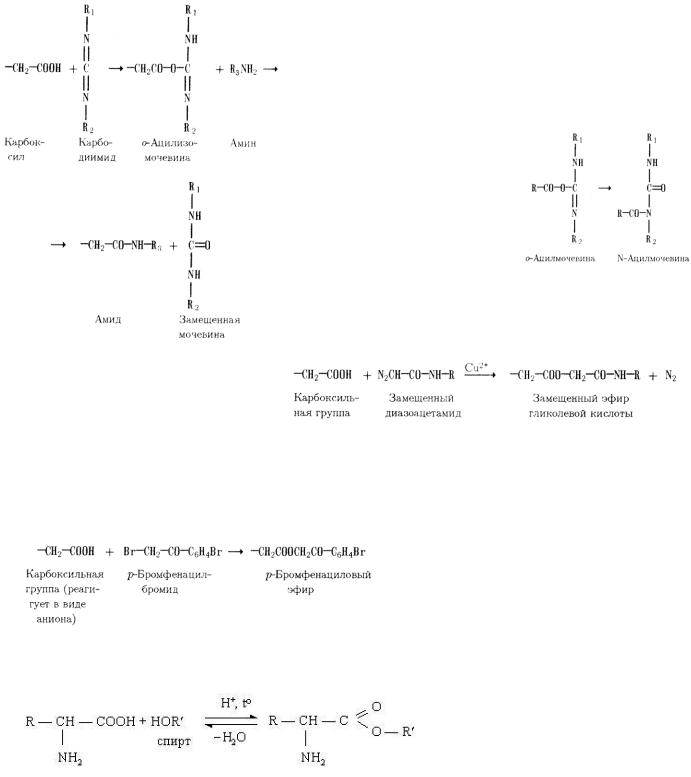
Реакция с этим или другими протекает по следующей схеме карбодиимид; R3-NH2-алифатический метиловый эфир глицина) – схема слева
Следует иметь в виду, что продукт активации карбоксильной группы- о- ацилизомочевинаможет не только вступать в реакцию с амином, но и стабилизироваться в результате
внутримолекулярного переноса ацильного остатка с атома кислорода на азот. Это приводит к образованию стабильной N-ацилмочевины:
2) Реакция с алифатическими диазосоединениями.
Стабильные |
алифатические |
|
диазосоединения, |
например |
|
производные |
диазоацетамида, |
в |
присутствии ионов меди реагируют с некоторыми карбоксильными группами, например с карбоксильной группой одного из остатков аспарагиновой кислоты :
3)Алкилирование карбоксильных групп. В качестве агентов, алкилирующих некоторые карбоксильные группы в белках, могут использоваться α-галоидкетоны, например р- бромфенацилбромид (Br-CH2CO-C6H4Br и его аналоги, а также галоидкислоты):
4)Гринкевич : можно восстановить карбоксильную группу до спиртовой с помощью B2H6.
5)Реакция этерификации. Эта реакция может использоваться для защиты карбоксильной группы при синтезе пептида.
6) Образование галогенангидридов с галогенидами фосфора (PCI5, РСl3) или тионилхлоридом (SOCI2). Реакция используется для активации карбоксильной группы при пептидном синтезе.