Материал: Bilet_1
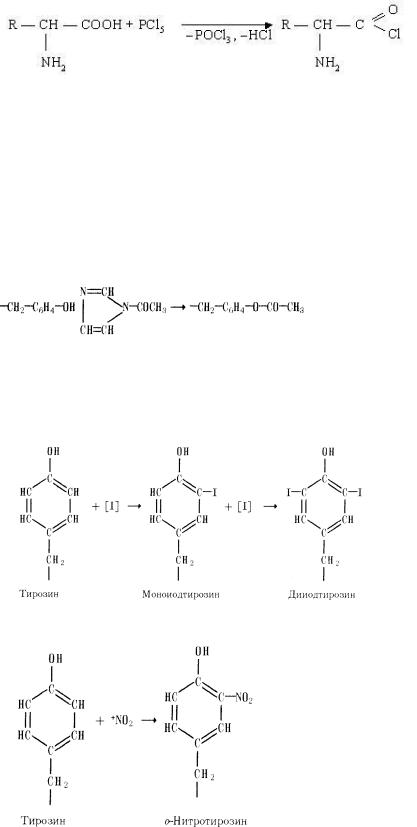
Химическая модификация остатков тирозина в белке
Гидроксильные группы тирозина в белках располагаются частично внутри, частично на поверхности белковой глобулы. В последнем случае для них характерен рКа>> 10, соответствующий переходу:
-CH2-C6H4-OH  -CH2-C6H4-O—
-CH2-C6H4-O—
Образующийся при этом фенолят-ион весьма активно вступает в реакции, свойственные также ε- аминогруппам лизина.
5)Ацилирование. Например присоединение ацетилимидазола.
6)Иодирование. Эту реакцию часто применяют как способ внедрения реактивных изотопов иода в белковую молекулу. Источником атомов иода может служить комплекс иода и йодистого калия; в некоторых случаях используют иод, образующийся при окислении иодид-иона в присутствии фермента пероксидазы. Иодирование приводит к образованию как моно-, так и дийодтирозина, причем замещение идет в о-положение:
7) Нитрование. Нитрование достигается действием тетранитрометана С(NO2)4 , причем в роли активной частицы обычно выступает нитроний-катион NO2+
Введение второй нитрогруппы возможно в о-положение.
8) Азосочетание. Реакция остатков тирозина с ароматическими солями диазония, также, являющимися катионными реагентами, опять-таки приводит к образованию моно- и ди-о- замещенных продуктов с достаточно протяженной системой сопряженных двойных связей, сто придает им красно-оранжевое окрашивание в реакции Паули (р-р белка смешивают со свежеприготовл. р-ром n-диазобензолсульфокислотой в присут. Na2CO3.) Эта реакция приводит к усилению кислотных свойств гидроксильной группы тирозина.
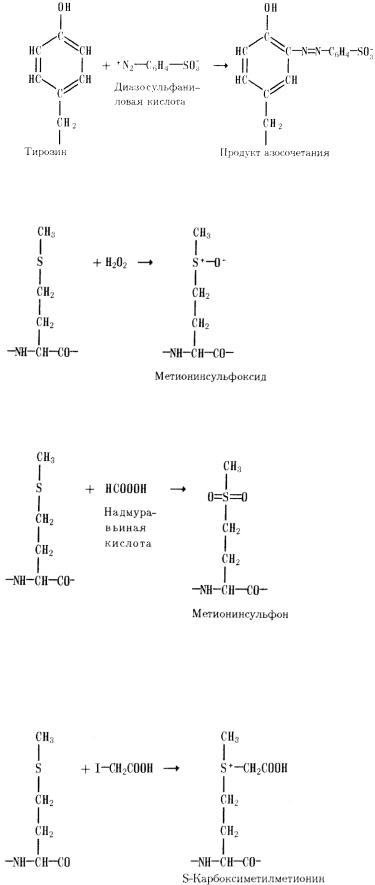
Химическая модификация остатков метионина:
1) Остатки метионина в белках и особенно в пептидах легко окисляются до метионинсульфоксида:
В ряде случаев эта реакция протекает даже под действием кислорода воздуха. В более жестких условиях, например при действии надмуравьиной кислоты, окисление проходит глубже и приводит к метионинсульфону:
2) Для модифицирования остатков метионина чаще, однако применяют алкилирующие агенты или галоидзамещенные кислоты, в частности иодуксусную кислоту или ее амд. При этом характерно, что сера метионина реагирует с такого рода соединениями даже в слабокислой среде, когда большинство других нуклеофильных групп белка, в частности имидазольные группы гистидина, в реакцию не вступают, будучи протонированы:
2. Проблемы, связанные с анализом посттрансляционно модифицированных аминокислотных остатков в белках.
Во-первых, функционально активные центры, как правило содержат ансамбли групп, функциональные группы в необычном окружении, что изменяет, делает нестандартными их свойства, в результате чего возникают проблемы при идентификации модифицированного остатка
аминокислоты. В то же время следует учитывать еще одну трудность, внутренне присущую трактовке результатов, полученных любым методом модифицирования. Получив данные о том, что присоединение к некой группе белка заместителя R вызывает характерное изменение его функциональных свойств, например утрату активности, нелегко определить произошло ли это вследствие блокирования данной функциональной группы или же в результате введения остатка R в данную точку белка, где его присутствие недопустимо ( например, из-за вызываемых этим заместителем стерических осложнений). Расчет на то, что применение реагентов с очень небольшими радикалами R снимет проблему, вряд ли оправдан, так как помехи вовсе не обязательно связаны размерами. Это делает результаты хим. Модифицирования не всегда однозначными. За последние 20 лет, масс-спектрометрический анализ стал важным инструментом для определения видов и участков белковых модификаций. Масс-спектрометрический анализ может быть выполнен как для очищенных белков, так и для смеси белков, например, клеточных лизатов .
Другой способ –фосфорилирование радиоактивно меченным фосфором.
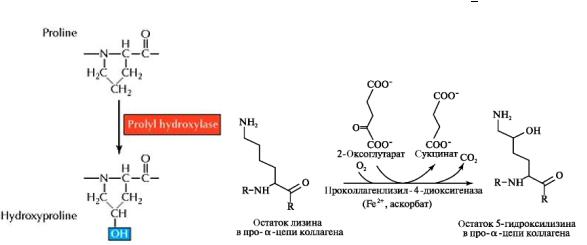
Гидроксилирование. Ярким примером является гидроксилирование Pro и Lys при образовании коллагена.
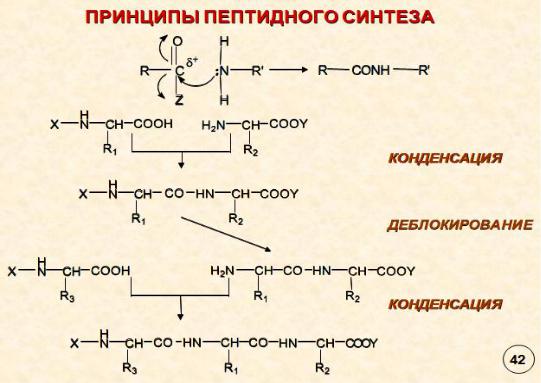
3. Пептидный синтез — это построение пептидной цепи путем соединения аминокислот с помощью химических методов. Обычно речь идет о получении пептидов, содержащих до 40 — 45 аминокислот, таким способом можно осуществить синтез и небольших белков.
Пептидный синтез служит надежным средством доказательства строения природных пептиднобелковых веществ. Синтетические пептиды широко используются для структурно-функциональных
исследований. С помощью химических методов удается получать аналоги биологически активных пептидов, в том числе циклические производные с заданными свойствами (например, с пролонги-
рованным, усиленным или избирательным действием), а также аналоги с остатками небелковых аминокислот. Синтетические пептидные фрагменты белков применяются для изучения их антигенных свойств и получения специфичных к отдельным участкам полипептидных цепей антител, используемых в структурно-функциональном анализе и в создании диагностикумов и вакцин. Методами пептидного синтеза получаются (в том числе и в промышленном масштабе) многие практически важные препараты для медицины и сельского хозяйства.
Защитные группы, используемые в пептидном синтезе
В пептидном синтезе существуют два типа защитных групп — постоянные и временные. Постоянными называют группировки, используемые для защиты боковых функциональных групп и удаляемые на заключительном этапе синтеза пептида.
Временными являются защитные группы для N-концевой аминогруппы и С-концевого карбоксила, снимаемые соответственно перед каждой стадией удлинения цепи или конденсации фрагментов.
Защитные группы, используемые в синтезе пептидов, должны удовлетворять следующим
условиям:
—полностью блокировать соответствующую группировку от участия в проводимых химических реакциях;
—быть устойчивыми в ходе удаления других защитных групп;
—не вызывать побочных реакций и рацемизации при введении, удалении и при образовании пептидных связей;
—защищенные производные должны быть устойчивыми идентифицируемыми соединениями;
—не вызывать осложнений с растворимостью и выделением пептидов из реакционных смесей.
Синтез на полимерном носителе. Пептидный синтез в классическом варианте сопряжен со значительными затратами труда и времени. С целью создания более эффективной методологии Р. Меррифилд в 1963 г. предложил твердофазный метод синтеза пептидов. Идея его состоит в закреплении растущей полипептидной цепи на полимерном нерастворимом носителе. При этом значительно упрощаются операции выделения промежуточных продуктов, которые сводятся к экстракции и фильтрованию полимера, полностью снимается проблема нерастворимости пептидов и создаются предпосылки для автоматизации процесса. Определяющим фактором в твердофазном синтезе является полнота протекания всех химических реакций, которая достигается за счет применения избытка конденсирующего агента и N-защищенной аминокислоты, отделяемых экстракцией. Естественно, выбор защитных группировок и методов конденсации должен обеспечить полное отсутствие рацемизации. Наилучшие результаты достигаются при использовании Вое-, Врос- и Fmoc-защитных групп, методов симметричных ангидридов и дициклогексилкарбодиимидного. Успешное проведение синтеза на твердом полимере требует применения высокоочищенных реагентов и растворителей на всех стадиях процесса. Первый твердофазный синтез гормона брадикинина был проведен Р. Меррифилдом с общим выходом 70%.
В качестве носителя наиболее широко используется микропористый хлорметилированный сополимер стирола и дивинилбензола, хорошо набухающий в органических растворителях и
обладающий химической и механической прочностью. Нагрузка полимера растущими пептидными цепями, как правило, невелика и составляет 0,1 — 0,3 ммоля пептида на 1 г полимера. Полнота реакции ацилирования оценивается на основании реакции с нингидрином или флуорескамином (см. с. 35 и 36) или физико-химическими методами.
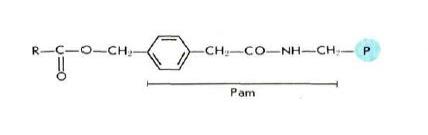
С целью повышения кислотоустойчивости якорных группировок, связывающих пептид с полимером, в настоящее время применяются полимерные смолы с фенилацетамидометильными группами (Рат-полимеры).
Отщепление пептида от смолы проводится с помощью жидкого HF в присутствии анизола, раствора HF в пиридине, трифторметансульфокислоты, реактива Плесса [(CF3COO)3B в CF3COOH], а также HBr/CF3COOH и других реагентов; иногда применяется аммонолиз, гидразинолиз, омыление и т. п.
Автоматический твердофазный синтез пептидов осуществляется на специальных приборах, называемых синтезаторами. В последние годы создан колоночный
вариант твердофазного синтеза пептидов. В качестве матрицы вначале использовалась полярная полиамидная смола. Этот желатинообразный полимер хорошо проницаем и сольватируется многими растворителями, включая воду и диметилформамид. Мягкие полимеры такого типа в колоночном варианте имели неудовлетворительные физико-химические и механические свойства. Р. Шеппард и сотр. Предложили использовать жесткий макропористый неорганический носитель — силикагель, в порах которого заполимеризован полидиметилакриламидный гель. Этот носитель, сочетающий в себе свойства жесткой матрицы и хорошо набухающего органического геля, нашел успешное применение в колоночном твердофазном синтезе. На его основе создан и синтезатор колоночного типа.