Материал: Bilet_1
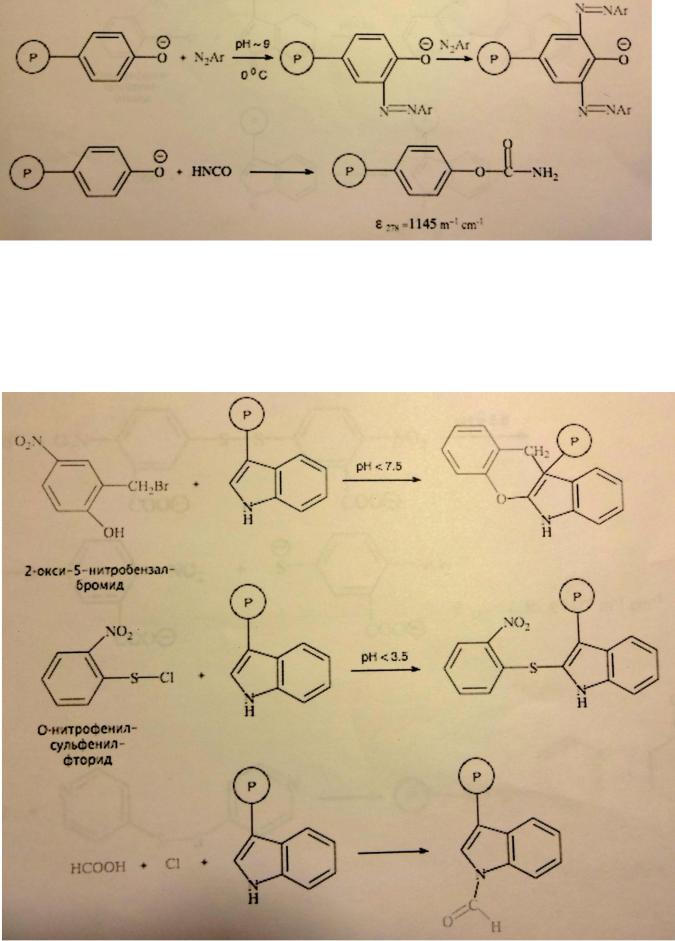
Основным реакционным центром триптофана в составе белка является индольное кольцо. π- Избыточный характер индола (а именно его пиррольного кольца) предопределяет его высокую реактивную способность по отношению к электрофильным реагентам.
Химическую модификацию остатков триптофана в молекулах белков проводят формилированием под действием муравьиной кислоты в соляной (последняя реакция на рисунке), сульфенированием с 2-нитрофенилсульфенилхлоридом (на фотографии фторид такой фторид) и конденсацией с 2-окси-5- нитробензалбромидом.
Билет №2.
1. Шаперон-зависимая автофагия как механизм специфической деградации белков в клетке.
Шапероны – класс белков, участвующих в формировании третичной и четвертичной структур белка и предохраняющих белки от агрегации. Белками теплового шока называют некоторые шапероны, экспрессия которых начинается в ответ на подъем температуры (а также другие повреждающие факторы), что содействует противостоянию неправильному сворачиванию белков. Также шапероны участвуют в транспорте белков (перенос субъединицы Rubisco из цитоплазмы в хлоропласт шапероном Hsp70), функционировании сигнальных путей (Hsp70 – часть антиапоптозного сигнального пути), регуляции действия молекул (Hsp90 блокирует стероидный рецептор в отсутствии его лиганда), и тому подобное и неподобное.
До сих пор не было известно иного способа утилизации белков, кроме убиквитинирования с последующей адресацией и разрушением в протеасоме. Однако, последние исследования британских учёных показали, что шапероны чуть менее, чем вездесущи: они могут принимать участие даже в деградации некоторых белков. Совсем недавно был выяснен механизм такой деградации, названной шаперон-зависимой автофагией, своей новизной вскружившей головы массе учёных. Процесс заключается в транслокации белка в лизосому, где он подвергается гидролизу под действием лизосомальных ферментов.
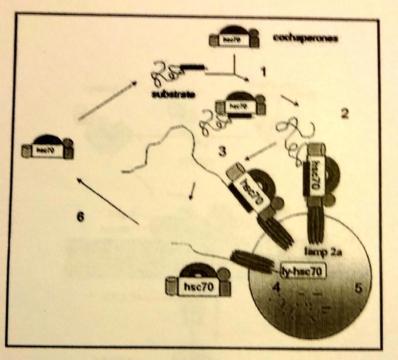
Этапы транспорта белка в лизосому:
hsc70 совместно с кошаперонами распознаёт пентапептид KFERQ в белке-мишени;
комплекс hsc70-мишень связывается с мультисубъединичным (вплоть до октамера) LAMP2A;
белок-мишень расплетается перед перемещением внутрь лизосомы;
для перемещения мишени в лизосому с ним связывается внутрилизосомальный шап. ly-hsc70;
белок-мишень расщепляется внутри лизосомы;
hsc70 отходит от мембраны лизосомы и готов взаимодействовать с новой мишенью.
Таким образом деградируется довольно широкий набор цитозольных белков, таких как рибонуклеаза А, некоторые гликолитические ферменты (альдолаза B, пируваткиназа, аспартатаминотрансфераза), некоторые транскрипционные факторы и ряд других белков.
2.Ферментативные методы гидролиза пептидных связей. Изменение специфичности действия трипсина с помощью химической модификации остатков K, R и С
гидролизуемого белка.
Реакции ферментативного гидролиза пептидных связей можно разделить на высокоспецифичные (Трипсин, протеаза из st. Aureus, лизин-специфическая протеаза, клострипаин, тромбин, протеаза из подчелюстной железы мышей, протеаза из почек ягненка) и низкоспецифичные (химотрипсин, термолизин, пепсин, папаин и эластаза).
Самым используемым в определении первичной структуры белка ферментом является трипсин – сериновая протеиназа, проявляющая наибольшую активность в диапазоне рН 7-9. Выделяется этот фермент из его предшественника, трипсиногена, получаемого из поджелудочной железы. В процессе выделения препарат загрязняется химотрипсином, низкоспецифичным ферментом, что создаёт серьёзные проблемы при оценке результатов трипсинолиза. Однако, есть способ избежать влияния такой контаминации: этого добиваются добавлением (1-тозиламидо-2-фенилэтил)-хлорметилкетона (ТФХК)– специфического ингибитора химотрипсина.
Трипсин уникален по своей субстратной специфичности, катализируя гидролиз связей, образованных карбокси-группами только основных аминокислот – лизина и аргинина. Выход такого гидролиза близок к 100%, однако может снижаться в случае локализации сайтов гидролиза на N- конце и соседстве с дикарбоновыми аминокислотами. Связи, образованные лизином или аргинином с пролином, обладают абсолютной устойчивостью к действию фермента. Также, несмотря на высокую избирательность фермента, после длительной инкубации наблюдается частичный гидролиз по связям, образованным ароматическими аминокислотами (тирозин, фенилаланин, триптофан).
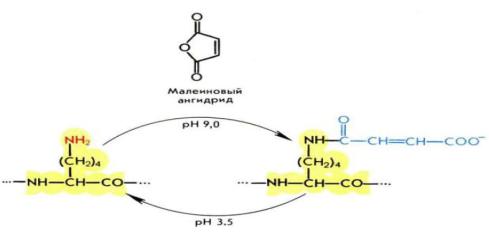
Введение заместителей в боковые цепи лизина и аргинина препятствуют гидролизу трипсином, позволяя выбирать между расщеплением связей, образованных одним из остатков. Модификацию лизина проводят с помощью ацилирования ангидридами дикарбоновых кислот. При этом происходит смена положительного заряда лизина на отрицательный заряд полуамида дикарбоновой кислоты:
В зависимости от природы используемого реагента модификация остатков лизина может быть как обратимой, так и необратимой. Для обратимой используется реакция с малеиновым или цитраконовым ангидридами. Регенерация остатков лизина в этом случае проводится путём понижения рН до 3,5 – в этих условиях полуамиды легко распадаются с деблокированием аминогруппы. Для необратимой модификации используется янтарный ангидрид.
Методы модификации остатков аргинина основаны на конденсации гуанидиновой группы с различными дикетонами и диальдегидами. Наиболее популярным блокирующим агентом является 1,2-циклогександион. Реакция протекает в мягких условиях в боратном буфере, при этом образуется устойчивый комплекс производного аргинина с боратом.
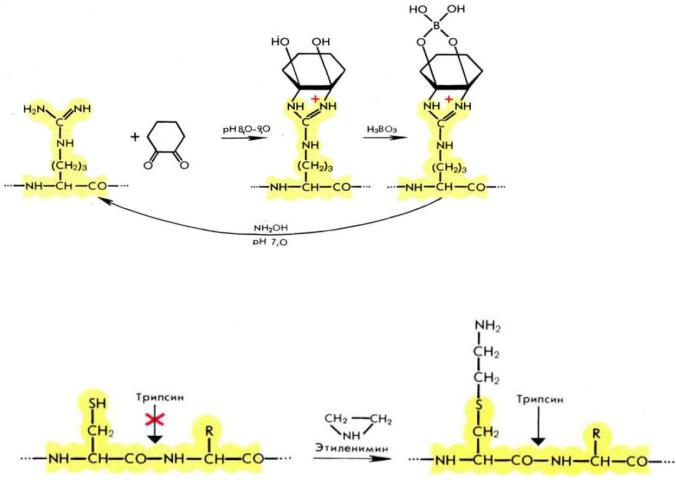
Модифицирующая группировка удаляется обработкой 0,5М гидроксиламином при рН 7,0, 37°С. С помощью хим. модификации можно также увеличить число гидролизуемых трипсином связей:
этого добиваются аминоэтилированием остатков цистеина этиленимином:
Пептидные связи, образованные карбокси-группой модифицированного цистеина, являющегося структурным аналогом лизина, способны расщепляться под действием трипсина, но с меньшей скоростью, чем каноничные пептидные связи.
Наряду с трипсином из поджелудочной железы выделяется химотрипсин – низкоспецифичная сериновая протеиназа, оптимум работы которой лежит в диапазоне рН 7,8-9,0. Фермент преимущественно катализирует гидролиз пептидных связей, образованных карбокси-группой ароматических аминокислот (тирозина, фенилаланина, триптофана). С меньшей скоростью гидролизуются пепт. связи лейцина, метионина, гистидина. Скорость расщепления может зависеть от природы соседствующего остатка.
Сериновая протеиназа, выделенная из St. aureus, имеет два оптимума работы: рН 4,0 и 7,8. Этот фермент расщепляет связи, образованные карбокси-группой глутаминовой кислоты. В ряде случаев гидролизу подвергаются и пепт. связи, образованные карбокси-группой аспарагиновой кислоты, особенно в случае соседства с гидрофобными остатками.
Уникальными свойствами обладает металлопротеиназа термолизин, содержащая цинк в качестве кофактора. Оптимум её работы лежит в диапазоне рН 7,0-9,0. Фермент невероятно устойчив: сохраняет свою активность в 8 М мочевине, при шестидесяти градусах и в 20%-ном растворе этанола. В отличие от большинства протеолитических ферментов, специфичность термолизина относится к остатку, которому принадлежит аминогруппа в пептидной связи. Таким образом, термолизин расщепляет пепт. связи, образованные аминогруппой гидрофобных аминокислот (изолейцин, лейцин, валин, фенилаланин, тирозин, триптофан). С меньшей скоростью гидролизуются связи с участием аланина и метионина.
Для избирательного расщепления белковой молекулы по остаткам лизина и аргинина широко используются новые ферменты. Один из них, лизин-специфическая протеиназа (из грибов Armilaria mellea), катализирует расщепление пепт. связи, образованной аминогруппой лизина. Клострипаин (Clostridium histolyticum) гидролизует связи, образованные карбокси-группой остатков аргинина.
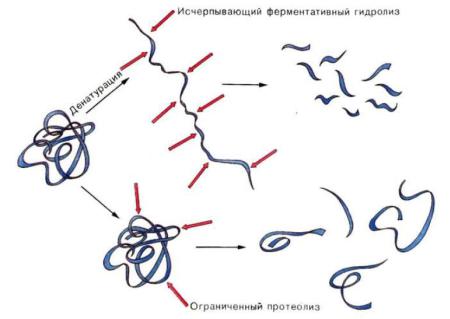
В арсенале современных исследователей также имеются менее специфичные ферменты (пепсин, папаин, эластаза, субтилизин, проназа и др.), которые используются для дополнительной фрагментации пептидов. Их субстратная специфичность определяется природой не только образующих пепт. связь остатков, но и более удаленных аминокислот.
Для исчерпывающего гидролиза необходимо денатурированное состояние белковой глобулы. В нативной конформации лишь часть сайтов могут быть задействованы в ферментативном гидролизе – проходит ограниченный протеолиз. Такие реакции повсеместны для организма – путём ограниченного протеолиза идёт активация многих проферментов.
3. Биоспецифическая модификация белков.
Модификации белков обычно проводятся с целью изучения взаимосвязи между структурой и функцией биополимерной молекулы. С этой целью могут предприниматься попытки химической модификации отдельных аминокислот, модификации с помощью бифункциональных реагентов, а также направленной биоспецифической модификации. Последняя модификация выделяется среди перечисленных своей точной адресацией (поэтому такой метод ещё называют аффинным мечением). Широко известно, например, использование субстратоподобных агентов для химического исследования природы и локализации активного центра ферментов и иных систем. Как биоспецифическую модификацию можно рассматривать и процессы посттрансляционной модификации белков в клетке (фосфорилирование, ацетилирование, гликозилирование, метилирование).
Реакционноспособные аналоги субстратов или других биоспецифических лигандов (гормонов, медиаторов, и др.) могут преимущественно или даже исключительно взаимодействовать с аминокислотными остатками, расположенными в активном центре фермента или белка-рецептора. В общем случае такие реагенты называются субстратоподобными. Так, например, этиловый эфир N- тозил-L-фенилаланина являетя субстратом химотрипсина. Аналог этого соединения – N-тозил-L- фенилаланилхлорметан является специфическим ингибитором – он селективно алкилирует остаток гистидина-57, расположенного в активном центре химотрипсина. Для изучения активности химотрипсина также использовался фенилметилсульфонилфторид, который избирательно реагирует с остатком серина-195. Так двумя путями уничтожалась возможность образования водородной связи между His57 и Ser195.
Реагенты для биоспецифической модификации белков часто содержат эпоксидную и диазогруппы. Так, для модификации химотрипсина применяется феноксиметилэтиленоксид, специфично взаимодействующий с остатком метионина-192.