Материал: Bilet_1
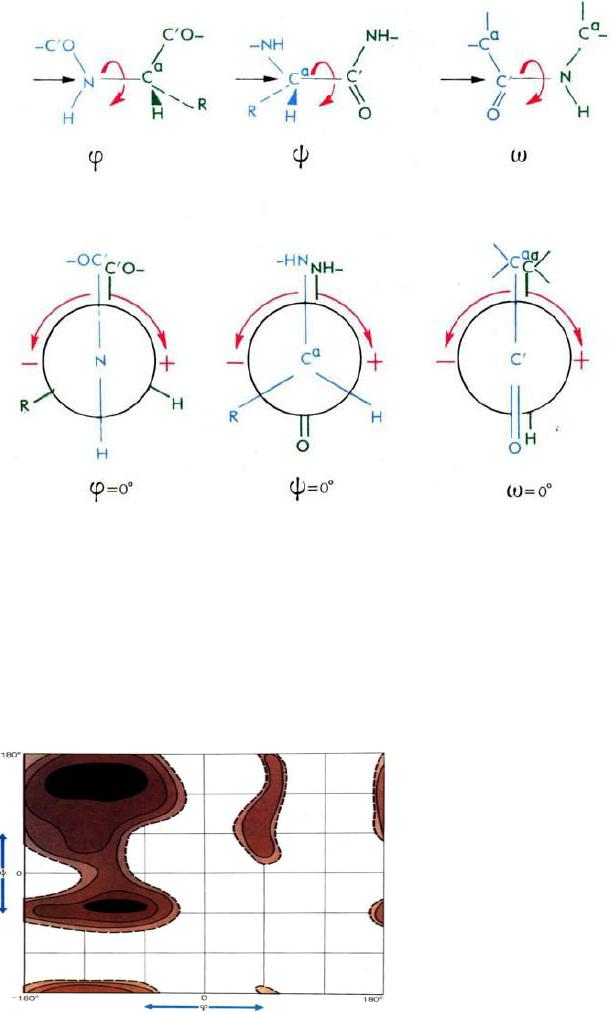
Рис. 35. Конформации пептидной цепи, отвечающие нулевым значениям углов φ, ψ и ω (черные стрелки указывают направление взгляда наблюдателя).
Знание таких значений для всех пептидных звеньев эквивалентно полной информации о пространственном строении основной цепи белка и пептида.
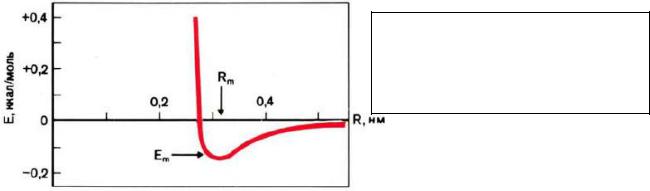
Графически конформационные параметры полипептидной цепи удобно изображать с помощью карт, предложенных Г. Рамачандраном в 1963 г. и отражающих зависимость энергии остатка от параметров φ и ψ (рис. 36). Значения углов откладываются по осям координат от —180° до +180°. В силу взаимодействия между заместителями в пептидной цепи углы не могут принимать любые значения — для них разрешенными оказываются лишь некоторые дискретные области (выделенные на карте темным цветом), которые соответствуют энергетически выгодным конформациям пептидной цепи, т. е., по существу, являются областями минимума энергии. Их достаточно компактная локализация свидетельствует о том, что углы взаимосвязаны, изменение одного из них влечет изменение второго.
Невалентные взаимодействия в пептидной цепи. Пространственная структура белков и пептидов в основном определяется невалентными взаимодействиями между различными атомами. К их числу относятся ван-дер-ваальсовы, электростатические, или ионные, ион-дипольные и дипольдипольные, гидрофобные, торсионные взаимодействия и водородные связи.
Водородные связи, как правило, образуются между подвижным атомом водорода (—ОН,— NH,—SH) и гетероатомом, чаще всего атомом кислорода. Водородная связь имеет донорноакцепторную природу, т. е. она образуется с участием неподеленной электронной пары гетероатома (донор электронов); акцептором электронов является атом водорода. Наибольшее значение для формирования пространственной структуры белков имеют водородные связи между СО- и NHгруппами пептидного остова. Помимо указанных, возможны и водородные связи с участием функциональных групп боковых цепей.
Гидрофобные взаимодействия, имеющие энтропийную природу, связаны с тем, что неполярные заместители выталкиваются из воды и стремятся ограничить свой контакт с водой; напротив, вода стремится восстановить свое структурированное состояние и как бы принудительно группирует заместители в кластеры, обладающие минимумом энергии. В такого родавзаимодействия вступают в основном неполярные боковые группы аминокислотных остатков.
Ван-дер-ваальсовы взаимодействия, описываемые потенциалом Ленард-Джонса (рис. 37), складываются из дисперсионных сил притяжения атомов и сил взаимного отталкивания их электронных оболочек. Как видно из рисунка 37, наиболее выгодным является расстояние Rm, равное или близкое сумме эффективных радиусов взаимодействующих атомов. Энергетический вклад каждого контакта невелик, но ввиду их большого числа ван-дер-ваальсовы взаимодействия дают основной вклад в суммарную энергию внутримолекулярных невалентных взаимодействий.
Рис. 37. Потенциал ЛенардДжонса (минимум: расстояние Rm и энергия притяжения Еm).
Ионные, или электростатические, взаимодействия представляют собой взаимодействия заряженных групп. При этом одноименно заряженные отталкиваются, а разноименно заряженные притягиваются. К ним относятся взаимодействия ионогенных групп, образующих солевые связи.
Торсионные взаимодействия характеризуют «скрученность» ординарной связи. В частности, поворот какой-либо группировки вокруг ординарной связи может нарушать электронную структуру этой связи и вызывать своего рода «тормозную» реакцию.
Торсионные силы относительно слабы, но при анализе поворотов вокруг связей С—С, С—N в боковых цепях аминокислотных остатков их нельзя не учитывать.
Реализуемая в данных условиях конформация белка и пептида определяется суммой всех взаимодействий и является энергетически наиболее выгодной, что и отражается «попаданием» соответствующих углов в разрешенные области конформационных «карт Рамачандрана».
Вторичная структура.
Пространственно упорядоченные участки, стабилизированные водородными связями между пептидными СО- и NH-группами, называются элементами вторичной структуры. То есть это конформационное расположение главной цепи, независимо от конформации боковых цепей или отношения к другим сегментам.
Исторически первой описанной пространственной конфигурацией полипептидной цепи была β-структура (исследования β-кератина). β-структура, или «складчатый лист»— полипептидная цепь в растянутом состоянии, ее NH и CO группы связаны водородными связями с аналогичными группами соседней, параллельно ориентированной полипептидной цепи. «Складчатый», т.к. α-атомы остатков расположены попеременно по обе стороны центральной плоскости слоя!
Примером белков природного происхождения с β-структурой является фиброин шелка. По существу, предельная вытянутость β-структуры и определяет большую прочность шелковой нити, ее
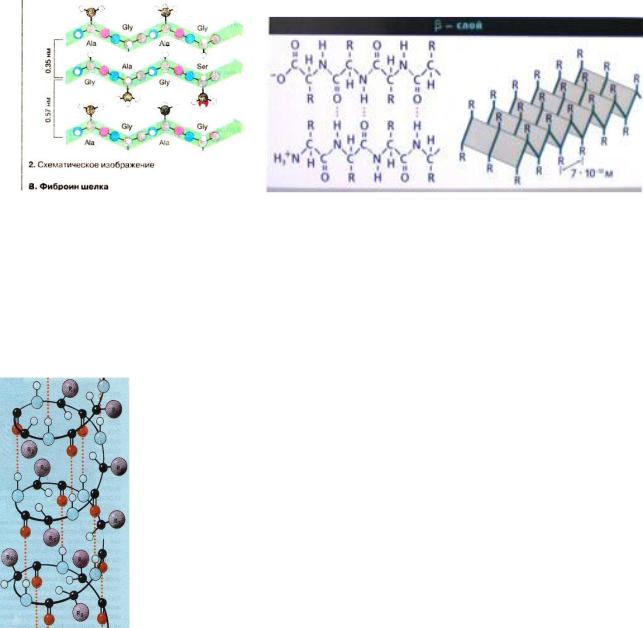
малую растяжимость. С другой стороны, так как отдельные «слои» ее связаны друг с другом лишь за счет ван-дер-ваальсовых взаимодействий, шелк чрезвычайно эластичен.
В фиброине шелка полипептидные цепи расположены антипараллельно, а в β-кератине стягиваются дополнительно липопротеином серицином.
Края антипараллельных β-структур образованы особым видом вторичной структуры, который называется β-изгибом (реверсивным поворотом). β-изгибы образуются четырьмя последовательно расположенными аминокислотными остатками, как правило, образующими водородную связь 4 — >1. Фрагмент β-структуры из двух антипараллельных цепей с β-изгибом часто называют «β- шпилькой».
Одна из главных канонических форм полипептидной цепи - α-спираль. Спираль стабилизирована почти линейными водородными связями между NH и CO группой четвертого по счету аминокислотного остатка. Каждый аминокислотный остаток, таким образом, формирует две водородные связи. Структура неустойчива, пока не произойдет формирование вод. связей с выделением свободной энергии, ван-дер-ваальсовы радиусы таковы, что внутри спирали нет
свободного пространства, отсюда устойчивость.
Зеркально симметричная левая α-спираль встречается в природе кране редко, хотя энергетически возможна.
А вот в коллагене присутствует принципиально другая левозакрученная. Вот здесь образование водородных мостиков невозможно!
Радикалы аминокислотных остатков оказываются на периферии образованного спиралью цилиндра и могут обеспечивать гидрофобную или гидрофильную природу этой цилиндрической поверхности. Один виток α- спирали образуют 3,6 аминокислотных остатка.
Наряду с α-спиралью возможно существование и других спиралей, имеющих иные параметры, — содержащих меньшее (например, так называемая 310-спираль) или большее (π-спирали, в белках практически не встречаются) число остатков на виток. Спираль 310, хотя и является напряженной, тем не менее существует в природе, в частности найдена в
миоглобине и лизоциме.
Сверхвторичная структура. Следующий за вторичной структурой уровень организации полипептидной цепи связан с наличием ансамблей взаимодействующих между собой вторичных структур. В частности, имеются примеры агрегации α-спиралей с образованием суперспирализованных систем. α-кератин шерсти: три α-спиральные цепи кератина скручены в протофибриллы, которые, в свою очередь, объединены в микрофибриллу, образующую волос. Поэтому шерсть эластична, легко растягивается и после снятия усилия постепенно восстанавливает свою длину. В силу того, что межмолекулярные связи слабы, шерсть непрочна. Короткие участки суперспирализованных антипараллельных α-спиралей присутствуют и в некоторых глобулярных белках. Весьма компактную левую тройную спираль образуют параллельные спирали типа полипролина в коллагене. Другая распространенная группа супервторичных структур — различные варианты так называемой βαβ-структуры (α-спираль взаимодействует с β-складчатым листом).
Третичная структура белков
Полипептидная цепь, содержащая определенное число участков вторичной структуры, обычно укладывается в пространстве в относительно компактную систему, в которой элементы вторичной структуры взаимодействуют между собой и с участками неупорядоченной структуры, образуя глобулу (глобулярные белки) или достаточно вытянутое волокно (фибриллярные белки). Для многих
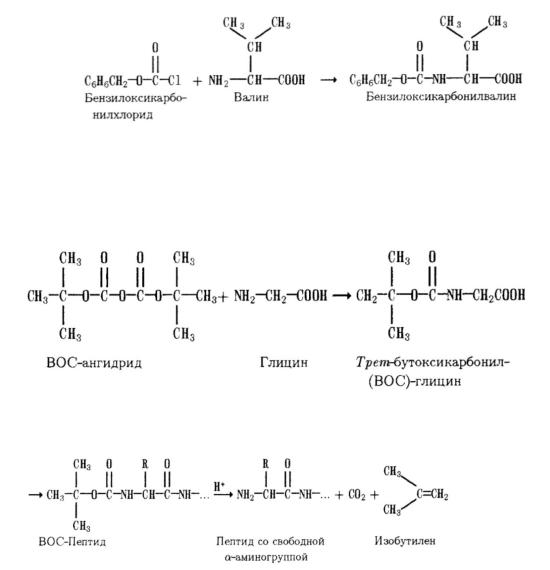
белков третичная структура эквивалентна полной пространственной структуре. Главным методом, с помощью которого в настоящее время определяется третичная структура белка, является рентгеноструктурный анализ кристаллических образцов.
2. Понятие о защите и активации α-NH2-группы. Специфическая модификация α- и ε- аминогрупп в белках: гуанидилирование, взаимодействие с иминоэфирами.
В пептидном синтезе существуют два типа защитных групп —постоянные и временные. Постоянными называют группировки, используемые для защиты боковых функциональных групп и удаляемые на заключительном этапе синтеза пептида. Временными являются защитные группы для Nα-концевой аминогруппы и С-концевого карбоксила, снимаемые соответственно перед каждой стадией удлинения цепи или конденсации фрагментов.
Защитные группы, используемые в синтезе пептидов, должны удовлетворять следующим условиям:
—полностью блокировать группировку от участия в проводимых химических реакциях;
—быть устойчивыми в ходе удаления других защитных групп;
—не вызывать побочных реакций при введении, удалении и при образовании пептидных связей;
—защищенные производные должны быть устойчивыми идентифицируемыми соединениями;
—не вызывать осложнений с растворимостью и выделением пептидов из реакционных смесей.
NH2-защитные группировки.
α-NH2 ацилирующей аминокислоты или пептида защищают так, чтобы блок после образования
пептидной связи можно было снять в условиях, которые гарантировали бы целостность пептида.
1.) Защита:
Одной из первых была предложена (сохранившая значение до сих пор) бензилоксикарбонильная группа (Z, устар. карбобензоксигруппа). Вводят, ацилируя пептид бензилоксикарбонилхлоридом
Активация: бензилоксикарбонильную группу отщепляют гидрированием в присутствии палладиевого катализатора или действием бромистого водорода в ледяной уксусной кислоте
2.) Защита:
Широко применяют ВОС-группу. Вводят, ацилируя аминогруппу ангидридом моно-трет- бутилового эфира угольной кислоты (ВОС-ангидридом):
Активация: мягким действием кислотных агентов — ТФУ или хлористого водорода в органических растворителях
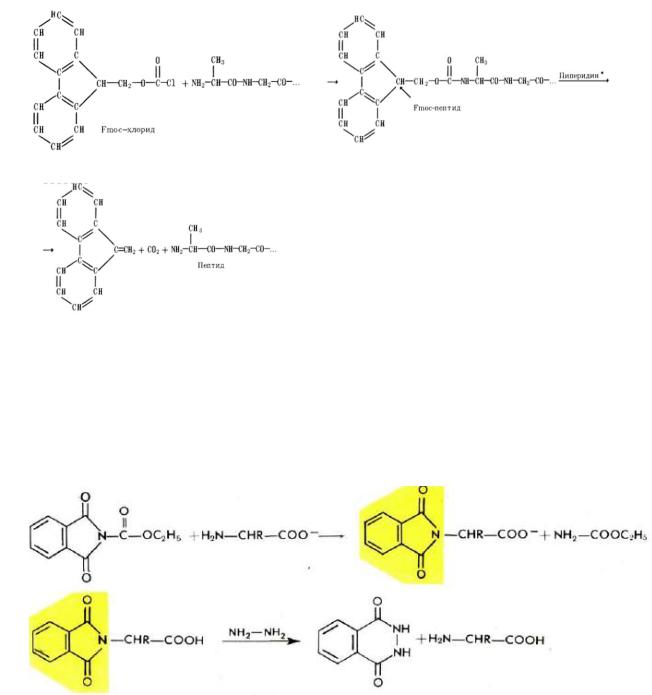
3.) Защита:
Среди уретановых группировок несомненный интерес представляют устойчивые к ацидолизу, но удаляемые мягким щелочным гидролизом 9-флуоренилметилоксикарбонильная (Fmoc) и метилсульфонилэтилоксикарбонильная (Msc). Fmoc-группа широко применяется, в частности, в твердофазном синтезе пептидов.
Для тех, кто не помнит: уретаны (карбаматы) — соединения общей формулы R'R''NCOOR, где R' и R'' — H, Alk, Ar; R — Alk, Ar. Эфиры неустойчивой карбаминовой кислоты H2NCOOH и её N-замещённых производных. Группы уретанового типа вводятся с помощью соответствующих хлоридов, азидов или карбонатов. Удаляют каталитическим гидрогенолизом (при серосодержащих пептидах — гидрированием в жидком аммиаке) или «переносным гидрированием» с донорами: 1,4- циклогександиен, циклогексен, муравьиная кислота или формиат аммония. Часто применяется и ацидолиз в различных условиях (HBr/СНзСООН, CF3COOH, 2н. HCl в диоксане, HF и т. п.).
Вот Fmocон уретановый! Устойчив к ацидолизу. Ацидолиз - обменная реакция между сложным эфиром или ацеталем и карбоновой к-той в присутствии каталитич. количества минер. к-ты, напр.: RCOOR' + R"COOH -> R"COOR' + RCOOH Все Тлен. Боже, Храни Начальника тюрьмы.
Ее вводят, действуя на аминокислоту или пептид соответствующим хлорангидридом:
Известно множество других защитных групп, обладающих теми или иными преимуществами и недостатками и применяемых в различных схемах синтеза. Их нужно много, потому как деблокирование α-аминогрупп мы проводим перед каждой новой стадией, а специфику в боковых группах – только в конце, иначе все сломается.
Защитные группы ацильного типа не используются в качестве временных защитных группировок из-за невозможности их удаления без расщепления пептидных связей (например, бензоильная или ацетильная группы) и легко происходящей рацемизации при получении активированных производных. Формильная и трифторацетильная группы (1 — 2) находят применение для защиты Nε-групп лизина. Фталильную (3) и тозильную (4) группы используют редко из-за жесткости условий их удаления (гидразинолизом и обработкой Na в жидком аммиаке соответственно). Для получения фталиламинокислот свободные аминокислоты ацилируют в воднощелочном растворе при 20 °С карбэтоксифталимидом: