Материал: Bilet_1
3.Посттрансляционные модификации α-COOH группы
Включающие расщепление пептидной связи 1) Удаление N-концевого остатка метионина
Как известно, в белках прокариот, в митохондриях и хлоропластах остаток, метионин инициирующий трансляцию, формилирован. N-Формильная группа удаляется ферментом формилазой. У эукариот трансляция инициируется метионином. После того как длина пептидной цепочки, еще связанной с рибосомой, достигнет примерно 20 аминокислотных остатков, инициирующий метионин может отщепляться специальной аминопептидазой. (не у всех)
Аминопептидаза предпочтительно отщепляющей N-концевой метионин, если за ним следует аминокислота с небольшой боковой цепью. Объемистый радикал, - метионин не отщепляется.
Природа N-концевой аминокислоты связана с устойчивостью белка к внутриклеточному протеолизу.
2) Ограниченный протеолиз
Присоединение небольших химических групп
1) N-ацилирование
Замещение атомов водорода в органических соединениях остатком карбоновой кислоты — ациьной группой [RCO]. Заключается, например, в присоединении к белкам жирных карбоновых кислот (см. также Миристилирование).
В организме реакции ацилирования протекают с участием особого вещества — кофермента ацилирования КоА (KoA-SH). Кислота вначале активируется путем соединения с сульфгидрильной группой KoA-SH (образуется ацил-S-KoA). Эта реакция протекает с использованием энергии макроэргической связи аденозинтрифосфорной кислоты (АТФ). Остаток кислоты затем переносится
сацил-S-KoA на ацилируемое вещество.
2)N-аргинилирование
Присоединение гидрофобных групп для локализации в мембране
1) N-миристоилирование
Перенос остатка миристиновой кислоты — СН3(СН2)12СО— от миристоилкоэнзима А на α- аминогруппу N-концевого остатка глицина белка. Гидрофобный миристоильный остаток участвует в удерживании белка в липидном слое мембраны или, возможно, связывается специальным белкомрецептором. Последний формируется на аминном конце полипептидной цепи после отщепления от нее сигнального пептида, обеспечивающего перенос полипептидной цепи белка через мембрану. В таких белках аминоконцевое положение неизменно занимает остаток цистеина. К его сульфгидрильной группе тиоэфирной связью присоединяется остаток диацилглицерина, затем еще один остаток жирной кислоты ацилируют α-аминогруппу цистеина, что приводит к следующей структуре:
Также, если есть остаток аргининадезаминирование, циклизация.
Билет 7.
1. Шапероны семейства Hsp100 и Hsp70
ЧТО ВООБЩЕ ТАКОЕ ШАПЕРОНЫ?
Белки за счет альтернативных гидрофобно-гидрофильных взаимодействий могут принимать неверную структуру. Есть белки, способные к самосборке ( in vitro –рибозимы)
Катализаторы фолдинга- ускоряют фолдинг. Шапероны фолдинга- принимают участие в изменении формы белка.
Можно выделить четыре типа молекул:
1)Молекулы, обеспечивающие правильный фолдинг.
2)Молекулы, удерживающие частично свернутый белок в определенном состоянии. Это для того, чтобы система смогла закончить фолдинг. Например, во время синтеза белка.
3)Молекулы, разворачивающие неправильно свернутые молекулырефолдинг.
Например, стероидный рецептор в цитоплазме связан с Hsp 90, лиганд, попадающий в цитоплазму, связывается с рецептором, вытесняет шаперон. Лигандрецептор могут теперь связываться с ДНК
4) Молекулы, сопровождающие белки при транспорте через клеточную мембрану. Например, рубиско в хлоропласт при участии Hsp 70.
Трансмембранный переносконтроль фолдинга белка. Белок поддерживается в несвернутом состоянии до тех пор, пока не пройдет через мембрану.
Многие шапероны - сахара или пептиды. Относительно неспецифичны. Иногда комлекс существует долго, иногда шаперон катализирует изменение одной стабильной конформации в другуюкомплекс распадается. Энергозависимы. Связываются с гидрофобными участками белка.
Основные семейства шаперонов по характеру экспрессии и присутствию в клетках Hsp90, Hsp70, Hsp60, Hsp100 и их кошапероны (оптимизирующие процесс).
Роль шаперонов состоит в защите белков от агрегации и обеспечении концентрационнонезависимого фолдинга. Если белок обладает способностью к самосборке in vitro-не значит, что обладает in vivo (разница в условиях протекания реакции, например, наличие других белков ).
HSP 70
Система Hsp70 состоит из нескольких отдельных белков. Обнаружена в цитоплазме, ЭПР, митохондриях, хлоропластах. Узнает только что синтезированные белки, белки, прошедшие через мембрану, белки, денатурированные во время стресса. В основном система контролирует взаимодействия между экспонированными наружу частями белка.
Компоненты системы:
Hsp70 (DnaK)-АТФаза
Hsp40 (DnaJ)- активатор АТФазы Grp E- фактор нуклеотидного обмена
Цикл функционирования системы шаперонов Hsp70:
Hsp70 и Hsp40 связываются с белком субстратом обособленно, работают совместно с фактором обмена (NEF) восстанавливающим АТФ из АДФ
1.Hsp40 первым связывается с синтезирующимся белком (в момент выхода его N конца за пределы рибосомы).
2.Регион Hsp40 - J доменсвязывается с Hsp70. Hsp70 одновременно связывается и с J и с полипептидом. В результате с субстратным белком оказались связанными два взаимодействующих между собой шаперона.
3.АДФ связанная форма такого комплекса остается ассоциированной пока GrpE не вытеснит АДФ. (GrpE обнаружен в прокариотах, митохондриях, хлоропластах. В других случаях реакции диссоциации сложнее).
4.После этого Hsp70 и Hsp40 диссоциируют.
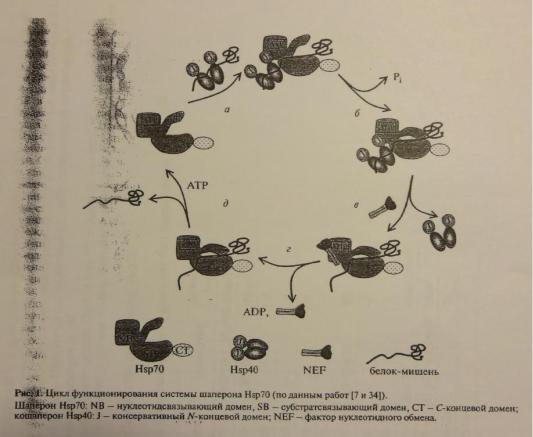
5.Hsp70 находит новую молекулу АТФ, цикл повторяется.
Сворачивание белка многократным повтором цикла ассоциации - диссоциации.
Как Hsp70 узнает мишень?
Hsp70 связывается с гидрофобной последовательностью, поскольку в зрелом белке такие участки запрятаны внутрь гидрофобного ядра, их экспозиция на поверхность свидетельствует о том, что белок только что синтезирован или денатурирован.
BiP (binding immunoglobulin protein) локализован в ЭПР, относится к Hsp70. Содействует олигомеризации, фолдингу только что поступивших в белков, удаляет белки с неправильной структурой.
Ответ на тепловой шок при участии Hsp70 и HSF (фактор теплового шока)
Вклетках, не подвергающихся стрессу Hsp70 связан с HSF (в мономерной форме, нет ДНКсвязывающей активности). В ответ на стресс Hsp70 отсоединяется от HSF и начинает укладывать денатурированные белки. HSF собирается в тримеры, у него появляется ДНК связывающая активность, он аккумулируется в ядре и связывается с промоторомтранскрипция шаперонов возрастает. Стресс проходит, Hsp70 снова связан с HSF.
HSP100 И ДЕЗАГРЕГАЦИЯ БЕЛКОВ
Участвуют в разрушении белковых агрегатов, образовавшихся в результате нарушения пространственной структуры белков. В бактериальных клетках функционирует Hsp100-шаперон ClpB, (растения и дрожжи содержат ортологи ClpB - Hsp101 и Hsp104)
Восновном дезагрегация белков осуществляется кооперативной работой системы Hsp70–
Hsp100.
Шапероны Hsp100 принадлежат к суперсемейству ААА+-белков (АТР-аз, ассоциированных с различными клеточными активностями).
Субъединицы Hsp100-шаперона ClpB и его ортологов содержат N-концевые экстрадомены и по два соединенных вариабельными линкерами ААА+-модуля (ААА+-1 и ААА+-2), важных как для олигомеризации, так и для проявления шапероновой функции.
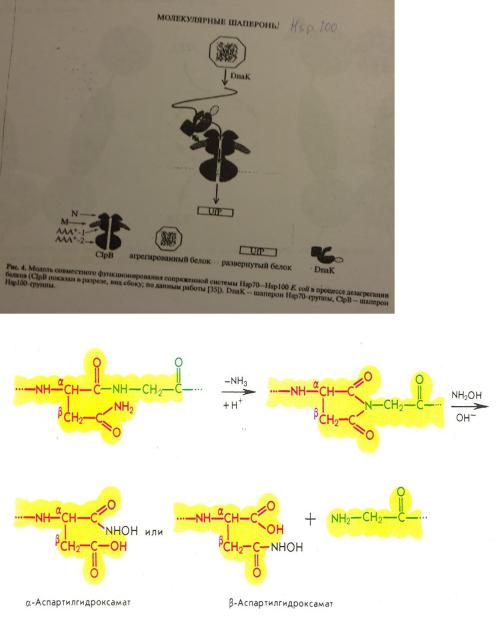
Согласно результатам рентгеноструктурного анализа, ClpB имеет классическую бочкоподобную
ААА+-упаковку и формирует двухъярусное гексамерное кольцо с центральным каналом d ≈ 16 Ǻ. Кольцо верхнего яруса, образованное ААА+-1-модулями, подвергается конформационным
изменениям, сопряженным с гидролизом АТР. Это же кольцо включает в себя уникальный пропеллерообразный домен (middle domain, М-домен), сформированный четырьмя α-спиралями. Он проявляет регуляторные функции, контролируя как АТФазную активность шаперона ClpB, так и DnaK-зависимое связывание агрегированных белков с аксиальным каналом ClpB
Считается, что система Hsp70-шаперона DnaK способствует изменению физических свойств агрегатов, инициирует высвобождение отдельного полипептида из белкового агрегата и перемещает его к ClpB. При этом N- концевой экстрадомен, расположенный на вершине ААА+-1-кольца, обеспечивает дополнительное взаимодействие шаперона с агрегатами.
В процессе транслокации полипептида сквозь центральный канал ClpB, промотируемой гидролизом АТР, происходит его разворачивание. Высвобожденный в среду развернутый полипептид (UfP) подвергается рефолдированию (либо спонтанному, либо с участием других шаперонов!). М домен как бы посредник между DnaK и ClpB.
Наличие характерного М-домена отличает шапероны, вовлеченные в процессы дезагрегации, от других членов суперсемейства ААА+-белков.
2. Расщепление полипептидной цепи по связям Asn-Gly
Выход данной реакции 40%.

3.Посттрансляционные модификации α-COOH группы
1.Амидирование (у гормональных пептидов)
2.Липопротеины с С-концевым гликолипидом Обнаружено около 30 белков, которые встраиваются в мембраны животных клеток за счет
гидрофобных, взаимодействий между липидами мембраны и своеобразно организованной С- концевой частью белка, представляющей собой гликолипид (так называемые «PIG-tailed»-белки — «белки со свиными хвостиками», от англ. Phospho-Inositol-Glycan).
Присоединение гликозилфосфатидилинозитола (GPI)
Это гликолипид, который может присоединяться к C-концу белка в процессе посттрансляционной модификации. Он состоит из фосфатидилинозитольной группы, соединенный углеводным связующим звеном (глюкозамин и манноза, гликозидно связанным с остатком инозитола) с C-концевой аминокислотой зрелого белка. Две жирные кислоты, составляющие фосфатидил-инозитоловую группу, заякоривают белок в клеточной мембране.
Белки, принимающие ГФИ, содержат сигнальную последовательность на C-конце, направляющую их в эндоплазматическую сеть. Эта последовательность состоит из гидрофобных аминокислот и погружается в мембрану ЭС и впоследствии отщепляется, замещаясь ГФИ-якорем.
Белок по секреторному пути проходит аппарат Гольджи и выделяется в межклеточное пространство, где с помощью якоря удерживается на внешнем слое плазмалеммы. Поскольку такие белки держатся на мембране исключительно при помощи ГФИ-якоря, его отщепление при помощи фосфолипаз приводит к высвобождению белка, причем процесс этот контролируемый. Такое отщепление используется в исследованиях.