Материал: Bilet_1
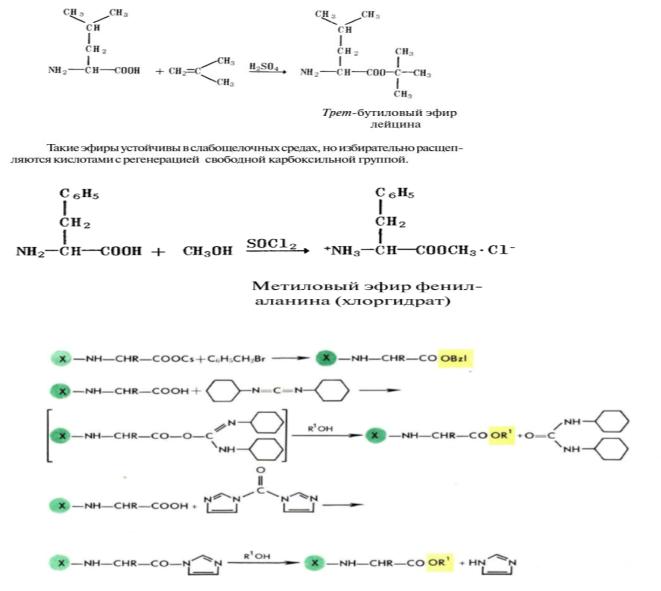
Билет 8 1. Защита и активация α-СООН. Химическая модификация карбоксильных групп белка.
Наиболее широко применяются превращение карбоксильной группы в метиловый, третбутиловый, бензиловый эфиры. Бензиловые эфиры и их производные получаются прямой этерификацией аминокислот в присутствии кислотных катализаторов или обработкой защищенных производных аминокислот бензилбромидом в щелочной среде.
В тех случаях, когда этерификация не может быть использована, применяются специальные реагенты, обычно рекомендуемые для образования сложноэфирных связей, а именно: N, N'- дициклогексилкарбодиимид (часто в присутствии катализатора 4-диметил - аминопиридина) и N,N'- карбонилдиимидазол.
В ряде случаев не требуется специально защищать карбоксильную группу. При проведении синтеза пептида в щелочной среде карбоксильная группа аминокислоты практически полностью диссоциирована и участие ее в образовании пептидной связи исключено, тогда как аминогруппа свободна.
Для отщепления метилового эфира прибегают к его омылению щелочью, которое не всегда протекает гладко и создает опасность рацемизации С-концевого остатка. Трeт-бутиловые эфиры удобно расщеплять мягкой обработкой кислотными агентами, например, трифторуксусной кислотой.

ω-Карбоксильные группы аспарагиновой и глутаминовой кислот, как правило, весьма многочисленны и в большинстве своем размещены поверхностном слое белка. Наиболее часто применяют следующие методы модификации этих групп
1.

2. Деградация пептидов по методу Эдмана, дансильный метод Эдмана.
Деградация по методу Эдмана смотри 9.2 Метод дансилирования:
ДНС-аминокислоты идентифицируют с помощью ВЭТСХ
3. Протеогликаны
Гликопротеины – белки, содержащие ковалентно связанный углеводный компонент. Делят на 2 класса по количеству связанных олигосахаридных цепочек: протеогликаны – количество олигосахаридных цепочек многократно превышает пептидную часть; собственно гликопротеины – сладенького понемножку.
Протеогликаны состоят из сердцевинных белков с которыми ковалентно связаны несколько гликозаминогликановых цепей. Сердцевинные белки синтезируются на шероховатом ЭПР и транспортируются в АГ, где происходит гликозилирование. На первой стадии происходит «наращивание» на сериновом остатке сердцевинного белка связующего тетрасахарида - ксилоза- галактоза-галактоза-глюкуроновая кислота (Xyl-Gal-Gal-GlcA), после чего соответствующими гликозилтрансферазами осуществяется наращивание специфичной гликозиламиногликановой цепи. Гликозаминогликановые цепи зачастую сульфированы.
Протегликаны – основной компонент внеклеточного матрикса (основа соединительной ткани). Обеспечивают необходимые физико-химические свойства стенок кровеносных сосудов, сухожилий, хрящей, стекловидного тела глаза. Нарушения биосинтеза протеогликанов приводят к тяжёлым заболеваниям.
Билет 9.
1. Импорт белков в ядро клетки.
Ядерный поровый комплекс – супрамолекулярная структура с молекулярной массой более 125 мДа (у позвоночных), состоящая из более 1000 белков.
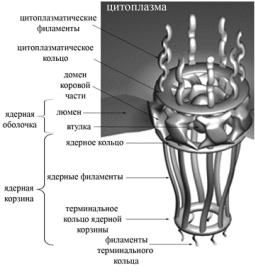
Строение ядерной поры:
Ядерные поры —сложно устроенные, многофункциональные регулируемые структуры, организованные приблизительно 30 белками — нуклеопоринами.Коровая часть-заякорена в ядерной оболочке, состоит из восьми доменов, ограничена цитоплазматическим и ядерным кольцами.
Пассивный транспорт
Разные молекулы-разная скорость.
Через ядерную оболочку беспрепятственно в обе стороны происходит пассивный транспорт высокомолекулярных соединений, имеющих массу не более 5 кДа (в Википедии проходят до 50, 60-70 уже активно)
Активный транспорт
Путём активного транспорта через ядерные поры могут проходить гораздо более крупные молекулы и целые надмолекулярные комплексы (рибосомные субчастицы, например). Причем одни белки должны поступать в ядро конститутивно (например, гистоны), а другие в ответ на определенные стимулы (например, транскрипционные факторы).
Белки должны обладать сигнальными последовательностями. Самая распространеннаяNLS- один или два участка положительно заряженных аминокислот, аргинина и лизина.
Впервые аминокислотные последовательности ядерной локализации (NLS) были обнаружены на С-конце субъединиц нуклеоплазмина (ядерный белок, принимающий участие в структуризации хроматина). Если удалить примерно 50 аминокислот с С-конца, то ни весь нуклеоплазмин, ни его мономеры в ядро не попадают.
Транслокация белков в ядро, в отличие от транслокации в митохондрии и ЭПР, не сопровождается отщеплением этой сигнальной последовательности и разворачиванием полипептидной цепи!
Белок с NLS проходит в ядро в несколько этапов:
1)Связывание NLS с рецептором, импортинами (α и β) и закрепление на цитоплазматических филаментах порового комплекса;
2)Постепенный проход этого комплекса через пору (импортины якобы разрыхляют пространство внутри поры);
3)Импортин β связывается с белком RAN (малая ГТФаза, гидролиз ГТФ делает этот процесс необратимым), происходит распад комплекса (NLS не отщепляется). Импортины возвращаются в цитоплазму (β-импортин в составе с RAN).