Материал: 2_MIKROBIOLOGIYa_temy_5-9_FIZIOLOGIYa_I_IZMENChIVOST_MIKROORGANIZMOV
Группа |
Потребность в О2 |
Возможные |
Примеры |
микроорганиз |
для жизнедеятельности |
типы |
микроорганизмов |
мов |
|
энергетическог |
|
|
|
о метаболизма |
|
|
течение нескольких минут. |
|
|
- умеренные |
Концентрация О2 не должна превышать 3%, |
|
С.tetani, |
|
выдерживают воздействие О2 воздуха в течение |
|
С.botulinum, |
|
20-30 мин. |
|
бифидобактерии, |
|
|
|
бактериоды, |
|
|
|
пептострептококки |
3. |
Растут и в присутствии О2, и в бескислородных |
Аэробное |
Большинство м/о: |
Факультативн |
условиях |
дыхание, |
энтеробактерии, |
ые анаэробы |
|
анаэробное |
стафилококки, вибрионы |
|
|
дыхание, |
|
|
|
брожение |
|
16
17
2. Изучение методов создания анаэробных условий
Существует несколько методов создания анаэробных условий
физические:
эвакуационно-заместительный (откачивание воздуха с помощью вакуумного насоса из герметически замкнутой емкости, например, анаэростата или анаэробного бокса, с последующей заменой на бескислородную газовую смесь);
посевы специальными методами - «уколом» в столбик агара, который затем заливают вазелиновым маслом; по методам Перетца, Бурри, Вейон-Виньялю и др. (схема 2);
химические: использование автономных анаэростатов - герметичных сосудов из прозрачного пластика с плотно закрывающейся крышкой в комплекте с газогенирирующими пакетами, которые содержат химические соединения, связывающие молекулярный кислород; используются для создания анаэробных или микроаэрофильных условий;
биологические:
посев по методу Фортнера – совместное выращивание микроорганизмов с разным типом дыхания: на один сектор агара засевают культуру аэробов, на другой – анаэробов, края чашки парафинируют. Аэробы при росте поглощают кислород и создают условия для развития анаэробов;
заражение восприимчивых лабораторных животных (например, культивирование лептоспир в организме морских свинок);
смешанные (использование одновременно нескольких методов).
1
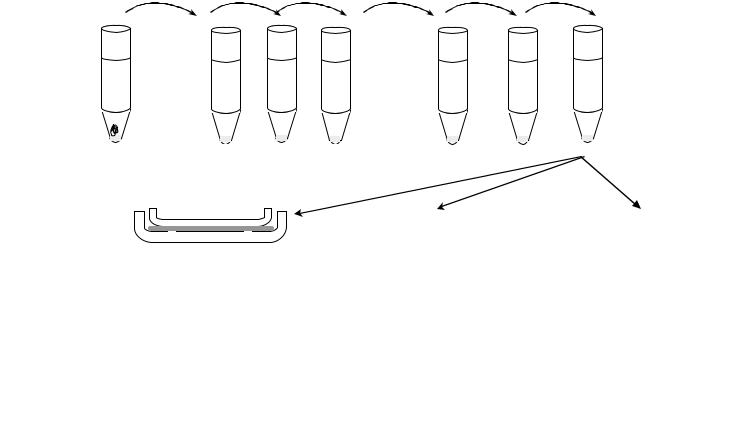
Схема 2
Методы выделения чистых культур анаэробных бактерий
(метод разведений пастеровской пипеткой по Вейнбергу, метод Перетца, Бурри, Вейон-Виньяля)
исследуемая |
физиологический |
полужидкий сахарный МПА |
культура в среде |
раствор |
|
Китт-Тароцци |
|
|
Метод Перетца
одно из разведений Вейнберга помещают между дном и крышкой чашки Петри
|
Метод Бурри |
|
Метод Вейон-Виньяля |
одно из разведений Вейн- |
одно из разведений Вейнберга |
||
берга |
набирают |
в |
набирают в пастеровскую |
стеклянную трубку; кон- |
пипетку; оттянутый конец пипет- |
||
цы трубки парафинируют |
ки запаивают, другой - пара- |
||
|
2 |
|
финируют |
Разведения по методу Вейнберга производят с помощью пастеровской пипетки с запаянным концом, которой последовательно переносят культуру анаэробов, выросших в среде Китт-Тароцци, в 3 пробирки со стерильными физ.растворами и три пробирки с расплавленными и остуженными до 45-500С полужидкими агарами с 1% глюкозой.
3. Выделение и идентификация чистых культур микроорганизмов
Выполняется 2-ой этап исследования чистых культур факультативно-анаэробных и облигатно-анаэробной культуры в соответствии с Приложениями 1 и 2.
При описании двух типов колоний факультативно-анаэробных бактерий учитывают отсутствие или наличие пигмента, придающего культуре определенный цвет и оптическую плотность.
Пигменты бактерий могут иметь различный состав (табл.14) и растворимость.
|
|
Таблица 14 |
|
Классификация пигментов бактерий по химическому составу |
|||
|
|
|
|
Название химической |
Цвет |
Примеры м/о, |
|
группы пигментов |
|
синтезирующих |
|
|
|
пигменты |
|
каротиноидные |
желтый, |
S.flava, S.aureus, |
|
|
оранжевый, |
M.marinum |
|
|
красный |
|
|
меланиновые |
коричневый, |
B.niger |
|
|
черный |
|
|
пирроловые |
ярко-красный |
S.marcescens |
|
фенозиновые |
сине-зеленый и |
P.aeruginosa |
|
|
др. |
|
|
По растворимости пигменты подразделяются на: - жирорастворимые (каротиноидные)
3