Материал: 2_MIKROBIOLOGIYa_temy_5-9_FIZIOLOGIYa_I_IZMENChIVOST_MIKROORGANIZMOV
3.дробная |
|
|
|
стерилизация |
|
|
|
текучим паром |
1000С – 40-60 мин. |
Питательные среды, |
|
|
дробно 3 дня |
содержащие углеводы, |
|
тиндализация |
подряд |
молоко, желатин и др. |
|
56-580С – 60 мин. |
Сыворотки, витамины, |
||
|
|||
|
дробно 5-6 дней |
некоторые лекарственные |
|
|
подряд |
вещества |
|
4. прокаливание в |
|
Бактериологические |
|
пламени |
|
петли, иглы, пинцеты |
Химическая стерилизация
используется ограниченно, поскольку существует ряд нежелательных эффектов при использовании данного вида обработки:
1)необходимость отмывания простерилизованного объекта от остатков стерилизанта (возможна повторная контаминация объекта);
2)длительность;
3)возможность побочного действия химического вещества на человека.
Химическая стерилизация используется в случаях, когда по каким-либо причинам невозможно использовать другие способы (обработка крупногабаритных приборов, приборов с дорогостоящими деталями, требующими «щадящих» режимов, например, эндоскопов и т. д.).
Основные способы и режимы химической стерилизации представлены в табл. 20 Таблица 20
Химическая стерилизация
|
Газовая |
|
Погружная |
|
|
||
|
(предметы помещают в |
(предметы погружают в раствор) |
|
|
герметические контейнеры) |
|
|
|
1. пары формальдегида 1 |
1. |
формалинэтил-алкоголь,24 ч. |
|
г/мл, влажность 80-90%, t0 > |
2. |
формалин-изопропанол,24 ч. |
|
20 0С, 24 ч. |
3. |
раствор первомура |
|
2. окись этилена с |
4. |
раствор анолита |
|
добавлением СО2, 500-200 |
|
|
|
мг/мл, влажность 60-90%, t0 > |
|
|
|
20 0С, 6-24 ч. |
|
|
Для оценки эффективности стерилизации контролируют критические параметры (табл.21)
Таблица 21
Критические параметры, контролируемые для оценки эффективности стерилизации
|
Вид стерилизации |
Контролируемые критические параметры |
1) |
суховоздушная |
Время экспозиции, температура |
2) |
паровая |
Время экспозиции, температура, |
|
|
насыщенный пар |
3) |
химическая (этилен |
Время экспозиции, температура, |
оксидная) |
концентрация газа, относительная |
|
|
|
влажность |
Для контроля качества термической и химической стерилизации используют различные индикаторы (табл.22)
Таблица 22 Классификация индикаторов контроля качества стерилизации по принципу работы
Группа |
|
Принцип работы |
|
Преимущества метода |
|||||
индикаторов |
|
|
|
|
|
|
|
|
|
1) биологические |
Содержат |
|
тестовые |
Является |
«золотым |
||||
индикаторы (БИ) |
микробные споры (B.subtilis |
стандартом», |
|
т.к. |
|||||
|
или |
B.stearothermophilus), |
только БИ определяют |
||||||
|
которые после стерилизации |
реальный факт гибели |
|||||||
|
инкубируют в |
питательной |
спор |
бактерий |
внутри |
||||
|
среде 24-48 час. |
|
стерилизатора |
|
|||||
2) химические |
Используют |
реакции |
-дает ответ сразу после |
||||||
индикаторы |
химических |
веществ |
на |
завершения |
|
работы |
|||
|
воздействие |
факторов |
стерилизатора |
|
|||||
|
стерилизации |
(изменение |
-не |
требует |
|
наличия |
|||
|
цвета |
или |
оплавление |
при |
бак.лаборатории |
||||
|
достижении |
критического |
-прост |
|
в |
||||
|
значения |
не |
менее |
двух |
интерпритации |
||||
|
стерилизационных |
|
|
|
|
|
|||
|
параметров). |
|
|
|
|
|
|
||
Классификация индикаторов контроля качества стерилизации по способу применения:
наружные (размещаемые на поверхности упаковки стерилизуемого объекта);
внутренние (размещаемые внутри упаковки).
2.Классификации антибиотиков и принципы рациональной антибактериальной терапии.
Термин химиотерапия, впервые предложенный П.Эрлихом, подразумевает использование лекарственных средств для уничтожения возбудителей инфекций в организме человека и животных без вреда для последних.
Классификация химиотерапевтических средств
В настоящее время средства, применяемые для химиотерапии, по происхождению принято делить на:
1)антибиотики;
2)синтетические антибактериальные средства разных химических групп.
Антибиотики - лекарственные средства биологического происхождения, способные избирательно подавлять возбудителей заболеваний в организме хозяина. К группе антибиотиков также относят их производные и синтезированные аналоги.
Существует несколько принципов классификации антибиотиков (табл. 23, 24, 25).
Таблица 23
Классификация антибиотиков по происхождению
№ |
Продуценты |
Примеры антибиотиков |
п/п |
|
|
1. |
Грибы родов: |
Группа пенициллинов: |
|
|
|
- Penicillum |
-бензилпенициллин (природный) |
||
|
|
- метициллин, оксациллин, |
|
|
|
|
ампициллин (полусинтетический) |
||
|
|
|
|
|
|
- Cephalosporium |
Группа цефалоспоринов: |
|
|
|
|
-ценорин |
|
|
|
|
-кефзол и др. |
|
|
2. |
Актиномицеты рода |
Полиеновые |
(нистатин, |
леворин, |
|
Streptomyces |
амфотерицин, пимафуцин) |
|
|
|
|
|
|
|
|
|
Группа стрептомицина |
|
|
|
|
|
|
|
|
|
Аминогликозиды |
(неомицин, |
|
|
|
мономицин, |
|
|
|
|
канамицин, гентамицин) |
|
|
|
|
Тетрациклины: тетрациклин |
|
|
|
|
|
|
|
|
|
Линкомицин |
|
|
|
|
|
|
|
|
|
Левомицетин |
|
|
|
|
|
|
|
|
|
Макролиды |
(эритромицин, |
|
|
|
азитромицин) |
|
|
|
|
Рифамицины |
|
|
|
|
|
|
|
3. |
Бактерии: |
Группа полимиксина: |
|
|
|
- Bacillus polymyxa |
-полимиксин М, В |
|
|
|
|
|
|
|
|
- Bacillus brevis |
грамицидин С |
|
|
|
|
|
|
|
4. |
Животного |
Лизоцим |
|
|
|
происхождения |
|
|
|
5. |
Растительного |
Фитонциды |
|
|
|
происхождения |
|
|
|
Таблица 24 Классификация природных антибиотиков в зависимости от химической структуры
№ |
Название группы |
Некоторые |
п/п |
|
представители |
1. |
β- лактамы: |
Бензилпенициллин, |
|
1. пенициллины |
оксациллин, |
|
2. цефалоспорины |
цефотаксим |
|
3. монобактамы |
|
|
4. карбопенемы |
|
2. |
Макролиды |
Олеандомицин, |
|
|
эритромицин |
3. |
Линкозамиды |
Линкомицин, |
|
|
клиндамицин |
4. |
Аминогликозиды |
Стрептомицин, |
|
|
амикацин, Гентамицин |
5. |
Тетрациклины |
Доксициклин |
6. |
Полимиксины |
Бацитрацин, |
|
|
полимиксин В, М |
7. |
Полиеновые антибиотики |
Нистатин, |
|
|
Амфотерицин В |
8. |
Рифампицины |
Рифампицин |
9. |
Производные |
Левомицетин |
|
диоксиаминофенилпропана |
|
10. |
Фузидин |
Грицеофульвин |
11. |
Гликопептиды |
Ванкомицин, |
|
|
тейкопланин |
12. |
Ристомицин |
Ристомицин |
Таблица 25 Классификация антибиотиков по механизму действия на микробную клетку
Механизм действия |
Примеры |
|
|
|
антибиотиков |
1.Нарушение синтеза клеточной |
бетталактамные, |
|
стенки или ее компонентов |
гликопептидные |
|
|
|
|
2.Нарушение |
морфофункциональной |
полимиксины, полиены |
организации |
цитоплазматической |
|
мембраны |
|
|
3.Ингибирование синтеза белка на |
рифампицины |
|
уровне РНК-полимеразы |
|
|
4.Ингибирование синтеза белка на |
тетрациклины, |
|
уровне рибосом |
левомицетин, |
|
|
|
макролиды |
По спектру действия антибиотики классифицируются на:
-антибактериальные,
-противогрибковые,
-антипротозойные,
-противовирусные,
-противоопухолевые.
Синтетические химиотерапевтические средства (ХТС) - это группа веществ разного химического строения и механизма действия на микроорганизмы, которые используются для антимикробной терапии (табл.26)
Таблица 26
Основные группы синтетических химиотерапевтических средств
№ |
Группа ХТС |
Примеры препаратов |
|
п/п |
|
|
|
1. |
Сульфаниламиды |
Сульфадиметоксин, фталазол, ко- |
|
|
|
тримаксозол (комбинированный с |
|
|
|
триметопримом) |
|
2. |
Производные |
Ципрофлоксацин, |
норфлоксацин, |
|
хинолонкарбоновой |
дифлоксацин |
|
|
кислоты 3-го поколения - |
|
|
|
фторхинолоны |
|
|
3. |
нитрофураны |
Фурадонин, |
фурагин, |
|
|
энтерофурил |
|
4. |
8-оксихинолоны |
Энтеросептол, нитроксолин |
|
5. |
нитроимидазолы |
метранидазол |
|
6. |
производные хиноксалина |
диоксидин |
|
3. Определение чувствительности бактерий к антибиотикам
Различают эмпирическую противомикробную терапию и противомикробную терапию при установленной чувствительности возбудителя к антибиотикам. Эмпирическое лечение начинают в соответствии с протоколами еще до выделения возбудителей инфекции из организма больного и постановки антибиотикограммы – определения их чувствительности к антибактериальным препаратам.
Эмпирическая антибиотикотерапия может иметь нежелательные последствия:
-если до лечения не взят материал для бактериологического и других видов исследования, то диагноз остается неясным и осложняется дальнейший выбор лекарственного препарата;
-если штамм бактерий, являющийся причиной инфекции, оказывается малоили нечувствительным к выбранным препаратам, то неоправданным являются расходы на лечение и возможные токсические эффекты антимикробной терапии;
-при использовании антибиотиков широкого спектра действия, как правило, происходит селекция резистентных штаммов, ведущая к клинической неэффективности лечения.
Антибиотикограмма выполняется с чистой культурой выделенных от пациента бактерий. Для обеспечения этого требования необходимо соблюдать следующие правила взятия материала на исследование:
1)материал должен быть получен до начала антибактериальной терапии или через срок, равный периоду полувыведения антибактериального препарата из организма;
2)материал для посева следует брать непосредственно из очага инфекции с соблюдением правил асептики (стерильными инструментами в стерильную посуду); если взятие материала непосредственно из очага инфекции невозможно, но он сообщается с внешней средой, можно провести исследование соответствующего отделяемого (моча, мокрота и др.);
3)материал высевают на соответствующий набор питательных сред, используемых для выделения чистых культур различных видов микроорганизмов;
4)если патологический процесс вызван микробной ассоциацией, раздельно исследуют чувствительность к антибиотикам всех членов ассоциации, выделенных в чистой культуре.
Способы определения чувствительности микроорганизмов к антибиотикам
Исследование чувствительности микроорганизмов к антибиотикам и химиотерапевтическим препаратам проводят стандартными унифицированными методами, регламентированными официальными инструкциями.
Существует несколько способов, которые можно разделить на следующие группы
(рис.8)
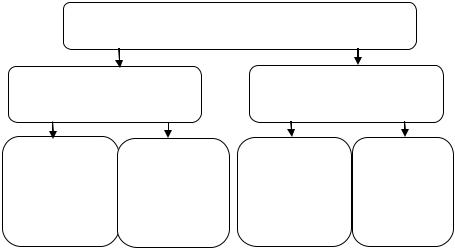
Способы определения чувствительности микроорганизмов к антибиотикам
Регламентрованные |
Нерегламентрованные |
|
(описанные в нормативных |
|
|
документах) |
|
|
Диффузионные |
Серийных |
АвтоматизиУскоренные |
1. диско- |
разведенй |
рованные |
диффузионный |
1. в бульоне |
(в баканализа- |
2. Е-тест |
2. в агаре |
торах) |
(эпсилон-тест) |
|
|