Материал: 2_MIKROBIOLOGIYa_temy_5-9_FIZIOLOGIYa_I_IZMENChIVOST_MIKROORGANIZMOV
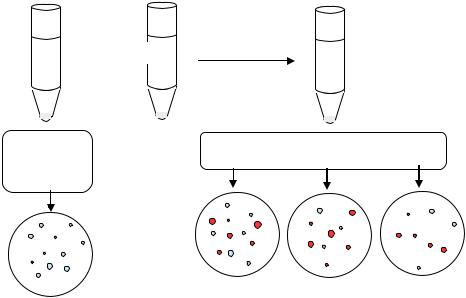
Схема опыта трансдукции
(формирование у лактозонегативного штамма E.coli способности разлагать лактозу)
Реципиент |
Донор фаг λ |
Зараженная трансдуцирующим |
E.coli lac- |
dgal, 1 мл |
фагом λ dgal культура E.coli lac- |
1 мл |
|
|
|
|
|
соединение
Высев на |
Высевы на среду Эндо по 0,1 мл |
среду |
из разведения смеси 10-6 |
Эндо 1 мл |
|
Условные обозначения:  - лактозонегативные колонии
- лактозонегативные колонии  - лактозопозитивные колонии
- лактозопозитивные колонии
Пример расчета: |
|
|
|
|
частота трансдукции = |
(5+1)х10х106 |
= |
6 |
= 1,3х10-2 |
|
(138+170+160)х10х106 |
468 |
||
4. Области использования учения о генетике и изменчивости микроорганизмов
I. Применение в промышленности генетически модифицированных микроорганизмов с заданными свойствами для получения коммерчески ценных продуктов
илекарств
1)производство вакцин:
-живых вакцин путем аттенуации (ослабления вирулентности) микробов под действием физических, химических и биологических факторов с сохранением иммуногенности;
-штаммов бактерий с высокой продукцией экзотоксинов для производства анатоксинов;
-генно-инженерных вакцин.
2)производство антибиотиков (получение штаммов бактерий и грибов с высокой продукцией антибиотиков);
3)производство биологически активных веществ (гормонов, например, инсулина, витаминов группы В,С, цитокинов и др.);
4)получение химических веществ: ацетона, спиртов, органических кислот, ингибиторов ферментов и др.
II. Генная диагностика с использованием молекулярно-генетических методов (ПЦР,
методов гибридизации и амплификации ДНК, секвенирование ДНК и др.):
1)экспресс-диагностика инфекционных заболеваний;
2)диагностика неинфекционных заболеваний (наследственных, онкологических, различных видов иммунопатологии и др.);
3)идентификация ДНК, белков в судебной медицине
III. Генная терапия - лечение соматических заболеваний путем переноса в дефектные клетки организма человека необходимых генов; для переноса используют векторы на основе вирусов.
5. Молекулярно-генетические методы исследований, используемые при диагностике инфекционных заболеваний
Наиболее часто используется полимеразная цепная реакция.
Полимеразная цепная реакция (ПЦР)
ПЦР разработана американским исследователем K.B.Mullis в 1985 году, является прямым, высокочувствительным и специфичным методом диагностики. Она основана на репродукции в пробирке уникальных участков генов вирусов или бактерий и образовании миллионов и миллиардов копий-амплификаций за 2-3 часа в присутствии фермента термостабильной ДНК-полимеразы (tag – полимеразы). Чувствительность ПЦР может достигать математически возможного предела (детекции 1 копии ДНК-матрицы).
ПЦР и методика ее постановки
При выполнении исследования ПЦР в реакторе (амплификаторе, или термоциклере) повторяются определенные циклы:
1.Денатурация - исследуемый биологический материал помещают в реактор (амплификатор, или термоциклер), где происходит нагревание материала и расщепление ДНК на две отдельные цепочки.
2.Отжиг - присоединение праймеров к противоположным концам полученных цепочек ДНК-мишени; праймеры («затравки») — это искусственно синтезированные олигонуклеотиды, комплементарные искомому фрагменту ДНК, они выделяют и ограничивают нужный участок.
3.Элонгация – после отжига праймеров фермент Taq-полимераза (по названию бактерии – Thermus aquaticus) начинает достраивание второй цепи ДНК с 3'-конца
праймера и формируется вторичная копия ДНК. Температурный цикл амплификации многократно повторяют (30-40 раз) по типу «цепной реакции». На каждом цикле количество синтезированных копий фрагмента ДНК — ампликонов - удваивается.
1.Идентификация копий ДНК, которую возможно проводить тремя методами:
а) электрофоретическим (в агарозном или полиакриламидном геле) — только качественный анализ, не автоматизированный, требует затрат времени, высокая степень опасности получения ложноположительного результата из-за переноса через предметы и реагенты как самой ДНК-матрицы, так и ампликонов, получаемых в больших количествах в течение ежедневной работы, сложность и субъективность трактовки результато в;
б) гибридизационно–ферментным; в) гибридизационно–флуоресцентным - используются праймеры, меченые
флюоресцентной меткой и детекторы флюоресценции для учета результатов; регистрацией продукта может проводиться после полного окончания реакции амплификации («анализ по конечной точке») или детекцией продукта в режиме «реального времени».
2.Компьютерный анализ и сравнение результатов с данными базы различных видов
ДНК.
Для предотвращения контаминации необходимо постоянно использовать собственные лабораторные контроли и периодически применять зашифрованные отрицательные и положительные образцы для оценки специфичности и чувствительности ПЦРгенодиагностических исследований.
Основные варианты ПЦР
1.Стандартная ПЦР - проводится на основе многократной амплификации (удвоения) конкретного фрагмента ДНК при использовании особых ферментов-праймеров; в результате многократного копирования (30-40 циклов) получается количество материала, достаточное для исследования.
2.ОТ-ПЦР (режим обратной транскрипции) - используется для идентификации вирусной РНК; используемый в этом варианте ПЦР фермент обратная транскриптаза позволяет на базе РНК выстроить комплементарную цепь ДНК, их которой восстанавливают вторую цепь ДНК и далее выполняют стандартную методику.
3.ПЦР с анализом результатов «по конечной точке» (End-point PCR) – это модификация метода ПЦР, которая позволяет учитывать результаты реакции по наличию флуоресценции после амплификации, не открывая пробирки; таким образом, решается одна из основных проблем ПЦР – проблема контаминации ампликонами.
4.ПЦР в реальном времени Real-time - количественный вариант, позволяющий не только идентифицировать, но и определить концентрацию ДНК, поскольку выявление заданного фрагмента ДНК запускается после прохождения каждого цикла амплификации, а не после осуществления всей цепочки; идентификация проводится без использования электрофореза и позволяет учитывать результаты реакции, не открывая пробирки; высокая степень автоматизации и специфичность, сокращение времени исследования и площади, занимаемой ПЦР-лабораторией.
5.ПЦР в CMD формате «Мультипрайм» (позволяет выявить в одной пробе несколько патогенов).
Область применения ПЦР
Выявление генов наследственных болезней.
Диагностика инфекционных болезней, особенно вызванных трудноили некультивируемыми на питательных средах микроорганизмами (микоплазмами, хламидиями, вирусами, риккетсиями и др.), а также медленнорастущими микроорганизмами (возбудителем туберкулеза).
Контроль вирусной безопасности крови доноров в качестве подтверждающего теста при ее серонегативности.
Оценка эффективности противовирусной терапии у больных ВИЧ-инфекцией и вирусными гепатитами.
Обнаружение маркеров лекарственной устойчивости у микроорганизмов для повышения эффективности антибактериальной терапии и др.
Судебно-медицинская экспертиза при наличии для исследования крайне малого количества ДНК.
ДНК – идентификация личности.
Установление родства людей.
Фармакогеномика.
Санитарная эпидемиология.
При диагностике инфекционных заболеваний необходимо иметь ввиду, что ни один из методов не имеет 100% гарантии чувствительности и специфичности, поэтому результаты ПЦР должны учитываться в комплексе с результатами других лабораторных методов исследования.
Тема: Действие химических и физических факторов на микроорганизмы. Антимикробные мероприятия. Антибиотики. Методы определения чувствительности микроорганизмов а антибиотикам (1 этап).
1. Основные группы антимикробных мероприятий, используемых для профилактики и лечения инфекционных заболеваний.
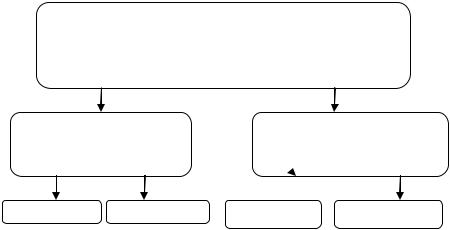
Существует множество мероприятий, направленных на создание безмикробной зоны в ЛПУ. Они могут быть разделены на прямые, косвенные и комплексные (рис. 6):
1)прямые - микробная деконтаминация - полное или частичное удаление микроорганизмов с объектов внешней среды и биотопов человека с помощью факторов прямого повреждающего действия
2)косвенные:
разграничительные меры (разобщение потоков людей, помещений, транспорта и т.д., тормозящее миграцию возбудителей);
меры воздействия на иммунную систему индивидуума (иммунопрофилактика, иммунотерапия, иммунокоррекция);
физические и механические методы воздействия, снижение численности микробной популяции (хирургическая, ультразвуковая, лазерная обработка ран, их дренирование и др.).
3)комплексные (сочетание прямых и косвенных методов) - асептика
Асептика - комплекс прямых и разграничительных антимикробных мероприятий, целью которых является создание безмикробной зоны в местах нахождения больных, проведения лечебно-диагностических манипуляций и лабораторных исследований для предупреждения развития и распространения инфекционных болезней.
МИКРОБНАЯ ДЕКОНТАМИНАЦИЯ - полное или частичное удаление микроорганизмов с
объектов внешней среды и биотопов человека с помощью факторов прямого повреждающего
МИКРОБНАЯ |
МИКРОБНАЯ |
ДЕКОНТАМИНАЦИЯ |
ДЕКОНТАМИНАЦИЯ |
объектов внешней среды |
биотопов человека |
Дезинфекция Стерилизация |
Антисептика Химиотерапия |
Рис. 6. Группы антимикробных мероприятий прямого повреждающего действия
Основные группы факторов, оказывающих прямое бактериостатическое и/или бактерицидное действие на микроорганизмы
физические (табл.16);
химические (табл.17);
биологические (антибиотики, бактериоцины, бактериофаги и др.).