Материал: Ткачёв С.В. Введение в органическую химию
5.3. АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ (АЛКИНЫ)
Ацетиленовые углеводороды — это углеводороды, в молекулах которых два атома углерода связаны друг с другом тройной связью. Длина связи С С в алкинах равна 0,120 нм. Общая формула алкинов CnH2n–2. Простейшее соединение с тройной связью — это ацетилен НС СН.
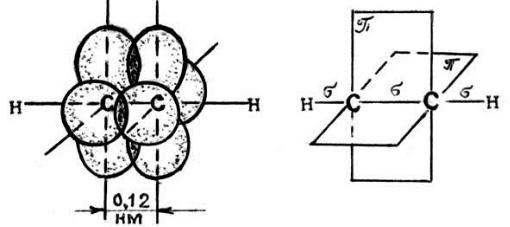
В молекуле ацетилена атомы водорода и углерода расположены на одной прямой, поэтому молекула имеет линейное строение. Атомы углерода соединены между собой одной -связью и двумя -связями (рис. 8). В молекуле ацетилена каждый атомом углерода соединен -связями только с одним атом углерода и с одним атомом водорода, поэтому в гибридизации здесь участвуют одна s-орбиталь и одна р-орбиталь каждого атома углерода (sp-гибридизация). В результате sp-гибридизации в ацетилене у каждого атома углерода образуются по две гибридных sр-орбитали. Эти две гибридные орбитали (от каждого атома по одному) взаимно перекрываются и между атомами углерода образуется -связь. Остальные две гибридные орбитали перекрываются с s-орбиталями водорода и между ними и атомами углерода тоже образуются -связи. Четыре (от каждого атома углерода по два) негибридных р-орбитали расположены взаимно перпендикулярно и перпендикулярно направлениям -связей.
В этих плоскостях р-орбитали взаимно перекрываются и образуются две -связи, которые в химических реакциях легко разрываются.
а |
б |
Рис. 8. Схема образования -связей в молекуле ацетилена:
а — попарно боковое перекрывание облаков р-электронов; б — две взаимно перпендикулярные плоскости, в которых происходит образование -связей
Изомерия и номенклатура. Названия углеводородов ряда ацетилена образуются в результате замены суффикса -ан в предельных углеводородах на -ин (этин, пропин, бутин и т. д.). У алкинов имеется структурная изомерия, которая определяется разветвлением углеродной цепи или по-
30
ложением тройной связи. Например, пентин С5Н8 образует следующие изомеры:
HC C – CH2 – CH2 – CH3 – пентин-1,
НС C – CН – CH3 – 3-метилбутин-1,
CH3
СН3 – С С – СН2 – СН3 – пентин-2.
Алкины и алкадиены имеют одну общую формулу. Поэтому они являются изомерами по отношению друг другу. Например, 2-метил- бутадиен-1,3, пентин-1, пентин-2 и 3-метил-бутин-1 являются изомерами. Они имеют общую формулу С5Н8. Изомерия между соединениями различных классов называется межклассовой изомерией.
Получение. В лаборатории и промышленности ацетилен получают при взаимодействии карбида кальция с водой и из метана.
СаС2 + 2Н2О НС СН + Са(ОН)2 2СН4 t НС СН + 3Н2
Физические свойства. В гомологическом ряду алкинов первые четыре члена — газы, алкины С5–С15 — жидкости, от С16 — твердые вещества.
Химические свойства 1. Реакции присоединения:
а) Гидрирование (присоединение)
HC CH |
H2 |
CH2 = CH2 |
H2 |
CH3 |
– CH3 |
|
(Ni, Pt) |
(Ni, Pt) |
|||||
|
|
|
|
б) Галогенирование
HC CH |
Br2 |
HC |
|
= CH |
|
|
|
||||
|
|
|
|
||
|
|
||||
|
|
|
|
|
|
|
|
Br Br |
|||
Br2 |
CHBr2 |
– CHBr2 |
|
Бромная вода обесцвечивается. Эта реакция является качественной на алкины, как и на все ненасыщенные углеводороды.
в) Присоединение галогеноводородов
HC CH |
HCl |
CH2 = CHCl HCl |
CH3 – CHCl2 |
|
|
|
|
|
|
|
винилхлорид |
1,1-дихлорэтан |
||
|
|
|||
г) Гидратация ацетилена (реакция М. Г. Кучерова). Присоединение воды к ацетилену происходит в присутствии катализатора — солей ртути (II) — Hg(NO3)2, HgSO4. Образуется уксусный альдегид.
HC CH + HOH CH3CHO
31
2. Реакции окисления а) Горение (полное окисление)
2C2H2 + 5O2 t 4CO2 + 2H2O
б) Неполное окисление под действием сильных окислителей (KMnO4, K2Cr2O7)
CH3 – C C – CH3 + 3[O] + H2O 2CH3 – COOH
Раствор KMnO4 обесцвечивается. Реакция с KMnO4 — качественная реакция на алкины.
3. Реакции полимеризации
Алкины могут образовывать линейные димеры, тримеры и полимеры, циклические тримеры.
HC CH + HC CH |
CuCl, H+ |
|
|
||||
|
CH2 = CH – C CH (винилацетилен) |
||||||
|
|
NH4Cl |
|
|
|||
3HC CH |
CuCl, H+ |
CH2 |
= CH – C C – СH = СН2 (дивинилацетилен) |
||||
NH4Cl |
|||||||
|
|
|
|
|
|
||
|
3HC CH |
уголь |
С6Н6 |
(бензол) |
|||
|
|
|
|||||
|
|
|
|||||
4. Кислотные свойства
В отличие от этана и этилена ацетилен проявляет свойства очень слабых кислот, атомы водорода в нем замещаются атомами металла. Например, при пропускании ацетилена через аммиачные растворы солей серебра и меди выпадают осадки ацетиленидов.
HC CH + 2AgOH Ag – C C – Ag + 2H2O
HC CH + 2CuOH Cu – C C – Cu + 2H2O
Применение ацетилена. Ацетилен является исходным продуктом для получения ряда химических соединений: этанола, уксусной кислоты, синтетического каучука и других соединений.
ВОПРОСЫ И УПРАЖНЕНИЯ
1.Какие углеводороды называются алкинами? Какова общая формула гомологического ряда алкинов?
2.Напишите структурную формулу вещества, изомерного бутину, но принадлежащего к другому классу углеводородов.
3.Какие типы изомерии характерны для алкинов? Напишите структурные формулы изомеров пентина и назовите их по международной номенклатуре.
4.Напишите структурные формулы веществ:
а) 3,3-диметилбутина-1; |
в) 3-метилбутина-1; |
б) 4-метилпентина-2; |
г) 1,4-дихлорбутина-2. |
32
5. Дайте название по международной номенклатуре следующим веществам:
а) СН3 – С С – СН – СН3 |
б) СН3 – СН2 – СН – С СН |
||||||
|
|
|
|
|
|
|
|
|
СН3 |
|
СН3 |
СН3 |
|||
|
|
|
|
|
|
||
|
|
||||||
|
|
|
|||||
в) СН2 = СН – СН – СН = СН – СН3 |
г) НС С – С – СН3 |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СН3 |
|
|
|
|
|
||
|
|
|
СН3 |
||||
6.Из каких веществ можно получить ацетилен? Напишите уравнения реакций.
7.Напишите уравнения реакций присоединения, характерных для бутина-1.
8.Напишите уравнения качественных реакций для алкинов.
9.Как получить хлорэтан из ацетилена? Напишите уравнения реак-
ций.
10.Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
метан ацетилен винилхлорид полихлорвинил.
ЗАДАЧИ
1.Какой объем ацетилена (н.у.) может быть получен из 1 кг технического карбида кальция, содержащего 30 % примесей? (Ответ: 245 л)
2.Из 100 г карбоната кальция получен карбид кальция. Какой объем ацетилена получится при действии воды на образовавшийся карбид кальция? Сколько уксусного альдегида образуется из ацетилена? (Ответ: 22,4 л; 44 г СН3СНО)
3.Объем смеси ацетилена и водорода равен 56 литрам. После пропускания смеси над катализатором ее объем уменьшился до 44,8 л (ацетилен прореагировал полностью). Определите состав полученной смеси газов в объемных процентах. (Ответ: 12,5 % этана; 87,5 % водорода)
4.При пропускании смеси этана и ацетилена через раствор бромной воды масса раствора увеличилась на 1,3 г. При полном сгорании такого же количества смеси углеводородов выделилось 14 л углекислого газа. Какой объем исходной смеси газов? (Ответ: 7 л)
5.Какой объем (в литрах, н.у.) винилхлорида образуется при присоединении хлористого водорода к ацетилену, полученному из 2 м3 (н.у.) природного газа с содержанием метана 98 % по объему? Выход винилхлорида равен 86 %, а выход ацетилена — 78 % от теоретического. (Ответ: 657 л)
33
ТЕСТОВЫЙ САМОКОНТРОЛЬ ПО ТЕМЕ «АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ»
1.Какие углеводороды имеют общую формулу CnH2n–2: а) этиленовые; б) диеновые; в) ацетиленовые; г) предельные?
2.Длина углерод – углеродной связи в ряду этан – этен – этин: а) увеличивается; б) уменьшается;
в) практически не изменяется.
3.Какие типы гибридизации электронных облаков атомов углерода
можно использовать |
для |
объяснения |
строения соединения: |
СН3 – С С – СН3 |
|
|
|
а) sp, sp2; |
б) sp, sp3; |
в) sp2, sp3; |
г) sp, sp? |
4. Укажите число |
возможных алкинов с |
молекулярной формулой |
|
С5Н8: |
|
|
|
а) один; |
б) три; |
в) четыре; |
г) два. |
5.Укажите, какие из формул соответствуют названию 2-хлор- гексадиен-1,3-ин-5:
а) CH3 – CHCl – CH = CH – CH = CH2; б) CH2 = CCl – CH = CH – C CH;
в) CH2 = CCl – CH2 – C C – CH3; г) HC C – CH = CH – CCl = CH2.
6.Укажите изомеры пентина-1:
а) 3-метилбутин-1; |
в) 2-метилбутадиен-1,3; |
б) циклопентан; |
г) пентин-2. |
7.Охарактеризуйте химическое строение молекулы ацетилена: а) три и две -связи; б) три -связи;
в) -связи образованы при перекрывании р-орбиталей атомов угле-
рода;
г) sр-гибридизация атомов углерода.
8.Укажите способы получения ацетилена: а) дегидрирование метана;
б) взаимодействие карбида кальция с водой; в) горение метана; г) взаимодействие гидрида кальция с водой.
34