Материал: Ткачёв С.В. Введение в органическую химию
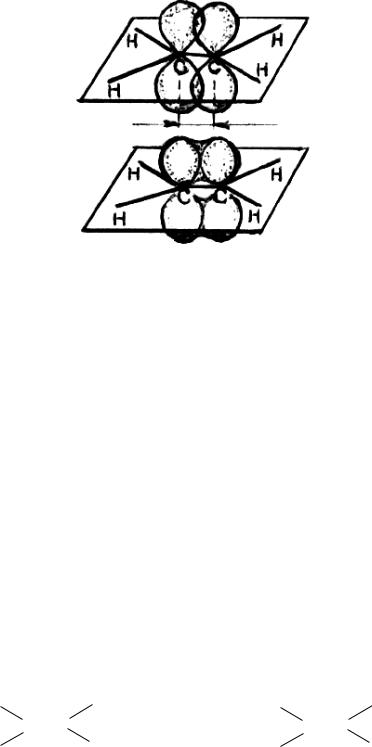
а
б
Рис. 7. Схема образования -связи в молекуле этилена:
а — боковое перекрывание облаков р-электронов; б — распределение общего облака-связи над плоскостью и под плоскостью атомных ядер
Таким образом, углерод — углеродная двойная связь в молекулах этиленовых углеводородов состоит из одной σ- и одной π-связи.
Расстояние между центрами атомов углерода в молекуле этилена равно 0,134 нм, а в молекуле этана оно равно 0,154 нм. π-Связь в этиленовых углеводородах более слабая, чем σ-связь.
Изомерия и номенклатура. Названия этиленовых углеводородов образуются от названия алканов, изменяя окончание -ан на -ен (этен, пропен, бутен и т. д.). Часто применяют старое окончание -илен (этилен, пропилен, амилен вместо пентилена). Выбирают самую длинную углеродную цепь и нумеруют ее с конца, к которому ближе расположена двойная связь.
1 |
2 |
3 |
4 |
CH2 |
= C – CH3 |
||
C H2 C H C H |
2 C H3 |
||||||
|
|
|
|||||
|
бутен-1 |
|
|
CH3 |
|||
|
|
|
|
2-метил-пропен-1 |
|||
CH3 |
|
CH3 |
|
H |
|
CH3 |
|
|
С = С |
|
|
|
С = С |
||
Н |
|
Н |
|
СН3 |
|
Н |
|
цис-бутен-2 |
|
|
транс-бутен-2 |
||||
Уалкенов, начиная с бутена, наблюдается структурная изомерия
ипространственная изомерия (цис- и транс-). Структурная изомерия характеризуется разветвлением углеродной цепи или положением двойной связи; пространственная изомерия — отсутствием свободного вращения вокруг двойной связи. Например: изомерия 2-метил-пропена-1 объясняет-
20

ся разветвлением углеродной цепи; бутена-2 — изменением положения двойной связи.
Если в молекулах есть заместители и двойная связь, то нумерацию начинают с того конца цепи, к которому ближе двойная связь, например:
5 |
4 |
3 |
2 |
1 |
C H3 |
C H C H C H C H3 |
|||
CH3 CH3
3,4 диметилпентен-2 Цис- и транс-бутены являются пространственными изомерами (сте-
реоизомерами).
Получение алкенов. Чаще всего алкены получают в результате реакций отщепления и при крекинге нефтяных продуктов.
1. Отщепление воды от спиртов (дегидратация):
(Al2O3, H2SO4(конц.), ZnCl2)
СН3 – СН – СН2 – СН3  СН3 – СН = СН – СН3 + H2O 350–450 °C
СН3 – СН = СН – СН3 + H2O 350–450 °C
ОН
2. Отщепление водорода от алканов (дегидрирование, дегидрогенизация) при температуре 450–650 °С в присутствии катализатора (Cr2O3, Al2O3 + KOH):
СН3 – СН2 – СН2 – СН3 СН3 – СН = СН – СН3 + Н2 3. Отщепление галогенов от дигалогенопроизводных:
СН3 – СН – СН2 + Zn |
|
СН3 – СН = СН2 + ZnBr2 |
|
Br Br
4. Отщепление галогеноводорода от галогенопроизводного в присутствии спиртового раствора щелочи:
СН3 – СН2 – СН – CH3 |
|
СН3 – СН = СН – CH3 + HBr |
|
Br
5. Крекинг нефтяных продуктов:
СН3 – СН2 – СН2 – СН3 Н2С = СН2 + СН3 – СН3 Образуется смесь алканов и алкенов, которую разделить на алкены
и алканы очень трудно.
Получение этилена.
1. Этилен в лаборатории получают при нагревании смеси этилового спирта с концентрированной серной кислотой:
H2SO4(конц.)
C2H5OH  H2C = CH2 + H2O t > 140 °C
H2C = CH2 + H2O t > 140 °C
21

2. В промышленности этилен получают дегидрированием этана или частичным гидрированием ацетилена:
СН3 –СН3 Н2С = СН2 + Н2 НС СН + Н2 Н2С = СН2
Физические свойства. Низшие алкены-газы, алкены от С5 до С14 — жидкости, высшие алкены — твердые вещества. Температуры кипения и плотности алкенов увеличиваются с увеличением длины углеродной цепи. В алкенах электронная плотность повышена у двойной связи. Все алкены практически нерастворимы в воде, мало растворимы в спиртах.
Химические свойства. π-Связь легко разрушается под влиянием различных реагентов. Это объясняется меньшей прочностью π-связи, так как электронные облака перекрываются в этом случае вне плоскости молекулы (см. рис. 6). Поэтому алкены легче вступают в химические реакции, чем алканы. Для алкенов характерны реакции присоединения по двойной связи.
1. Присоединение водорода (гидрирование):
|
Pt |
|
CH3 – CH = CH2 + H2 |
|
CH3 – CH2 – CH3 |
|
||
|
t |
|
2. Присоединение галогенов (галогенирование):
CH2 = CH2 + Cl2 CH2Cl – CH2Cl
CH3 – CH = CH2 + Br2 (бромная вода) CH3 – CHBr – CH2Br
3. Присоединение галогеноводородов:
H2C = CH2 + HBr CH3 – CH2Br
H2C = CH2 + HCl CH3 – CH2Cl
Пропилен и другие алкены реагируют с галогеноводородами по правилу В.В. Марковникова: водород присоединяется к наиболее, а атом галогена — к наименее гидрированному атому углерода:
CH2 = CH – CH3 + HBr CH3 – CHBr – CH3
4. Присоединение воды (гидратация):
CH2 = CH2 + HOH кат.t CH3CH2OH
СН3 – СН = СН2 + НОН СН3 – СНОН – СН3 Присоединение воды к алкенам идет по правилу В. В. Марковникова. 5. Окисление. Алкены легко окисляются. Водный раствор перманга-
ната калия KMnO4 окисляет этилен в этиленгликоль:
3CH2 = CH2 + 2KMnO4 + 4H2O 3CH2OH – CH2OH + 2MnO2 + 2KOH
Эту реакцию, как и реакцию с бромной водой применяют для качественного обнаружения алкенов. В кислороде, в воздухе алкены горят светящимся пламенем:
С2Н4 + 3О2 2СО2 + 2Н2О
22
6. Полимеризация. Полимеризация — это процесс, при котором небольшие молекулы (мономеры) соединяются друг с другом с образованием высокомолекулярного соединения (ВМС). При полимеризации молекулы алкена соединяются по месту разрыва двойной связи:
СН2 = СН2 + СН2 = СН2 + … -СН2 – СН2 – СН2 – СН2- …..
или: n CH2 = CH2 (–CH2–CH2–)n, где n — степень полимеризации (число молекул мономера). Известны полимеры: полиэтилен, полипропилен, полибутилен и другие.
Применение алкенов. Алкены применяются для получения алкилгалогенидов, спиртов, полимеров и других соединений. Этилен ускоряет созревание цитрусовых и обладает анестезирующими свойствами. Алкены токсичны для человека.
ВОПРОСЫ И УПРАЖНЕНИЯ
1.Какие углеводороды называются непредельными?
2.Какие непредельные углеводороды называются алкенами? Напишите общую формулу алкенов.
3.Укажите тип гибридизации орбиталей атомов углерода, связанных двойной связью в молекулах алкенов.
4.В чем различие между σ- и π-связью в молекуле этилена? Какая из связей менее прочная? Объясните почему.
5.Какие виды изомерии наблюдаются у предельных и непредельных углеводородов? Приведите примеры.
6.Составьте структурные формулы изомерных углеводородов, имеющих молекулярную массу 56. Назовите изомеры.
7.Почему число изомеров у углеводородов ряда этилена больше, чем
упредельных углеводородов? Для доказательства приведите изомеры углеводородов с молекулярными формулами С4Н10 и С4Н8.
8.Укажите изомеры из числа тех веществ, формулы которых приведены ниже:
а) СН2 = С – СН3 |
б) СН2 – |
СН – СН3 |
в) СН2 = СН – СН= СН2 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СН3 |
СН2 |
|
СН2 |
|
|||
|
|
|||||||||
г) СН2 – СН2 |
д) СН3 – СН = СН– СН2– СН3 е) СН3 – СН = СН – СН3 |
|||||||||
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
СН2 |
|
СН2 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
||||
9. Дайте названия по международной номенклатуре следующим углеводородам:
а) СН2 = С – СН2–СН3 |
б) СН3 – СН = С – СН – СН2 – СН3 |
||||
|
|
|
|
|
|
СН3 |
СН3 |
С2Н5 |
|||
|
|
23 |
|
|
|
|
СН3 |
|
|
|
|
в) СН2 =СН – С – СН3 |
г) СН3 – СН – С = СН2 |
||||
|
СН3 |
СН3 |
СН3 |
||
а) СН2 = С – СН2–СН3 |
3 |
|
2 |
3 |
||
СН3 |
СН3 |
|
С2Н5 |
|
||
СН3 |
|
|
|
|
|
|
|
|
г) СН3 – |
СН – |
С = СН2 |
|
|
в) СН2 =СН – С – СН3 |
|
|||||
|
|
|
|
|
|
|
СН3 |
СН3 |
СН3 |
|
|||
10. Среди веществ, формулы которых приведены ниже, укажите изомеры и гомологи пентена:
а) СН3 – СН = СН2 – СН3
б) СН3 – С = СН – СН3 |
|
в) СН3 – СН2 – СН2 – СН = СН2 |
|||||
|
|
|
|
|
|
|
|
|
СН3 |
|
|
|
|||
г) |
СН = СН |
д) СН3 – СН2 – СН2 – СН2 – СН3 |
|||||
|
|
||||||
|
|
|
|
|
|
||
СН3 СН3 |
|
|
|
||||
|
|
|
Н2С |
|
СН2 |
||
|
|||||||
|
|
|
е) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Н2С |
|
СН2 |
||
СН2
11.Составьте структурные формулы следующих углеводородов: а) 3-этил-гептена-2; б) 3,3 диметилпентена-1;
в) 3-метил-4-этилгексена-2.
12.У каких из приведенных ниже соединений возможна цис-транс- изомерия:
а) бутена-1; |
в) 2-метилбутена-2; |
б) пентена 2; |
г) 2-метилпропена? |
Приведите формулы изомеров.
13.Как получают этилен и углеводороды ряда этилена? Напишите уравнения соответствующих реакций.
14.Какие реакции являются качественными реакциями на алкены? Напишите уравнения этих реакций.
15.Сформулируйте правило Марковникова. Напишите уравнение реакции взаимодействия пропена и бутена-1 с бромистым водородом.
16.Что называется полимеризацией? Напишите уравнение реакции полимеризации пропилена и тетрафторэтилена.
17.Где применяются этилен и его производные?
18.Определите молекулярную формулу этиленового углеводорода, молекулярная масса которого:
а) 98; б) 126.
24