Материал: Ткачёв С.В. Введение в органическую химию
4.Напишите уравнения реакций получения: а) динитрата целлюлозы; б) диацетата целлюлозы.
5.Напишите уравнения реакций для превращений:
крахмал глюкоза этанол оксид углерода (IV) гидрокарбонат натрия
ЗАДАЧИ
1.Одна тонна картофеля содержит 20% крахмала. При брожении из одной тонны картофеля получено 100 л спирта ( = 0,8 г/мл). Определите выход этанола. (Ответ: 70,43 %)
2.После кислотного гидролиза 10 г целлюлозы получили 5,2 г глюкозы. Сколько процентов это составляет от теоретически рассчитанного количества? (Ответ: 46,85 %)
3.3 тонны древесины содержит 55 % целлюлозы по массе. Определите, какую массу триацетата целлюлозы можно получить из этой древесины, если выход продукта составляет 60 % от теоретически возможного. (Ответ: 1,76 т)
ТЕСТОВЫЙ САМОКОНТРОЛЬ ПО ТЕМЕ «УГЛЕВОДЫ. ПОЛИСАХАРИДЫ»
1. |
Укажите вещества, которые относятся к углеводам: |
|
|
а) крахмал; |
в) сахароза; |
|
б) целлюлоза; |
г) спирты. |
2. |
Крахмал можно получить: |
|
|
а) из картофеля; |
в) кукурузы; |
|
б) древесины; |
г) из риса. |
3. |
Укажите углеводы, которые построены только из остатков молекул |
|
глюкозы: |
|
|
|
а) целлюлоза; |
в) мальтоза; |
|
б) крахмал; |
г) сахароза. |
4.Охарактеризуйте строение целлюлозы: а) природный полисахарид; б) имеет линейное строение;
в) состоит из остатков β-глюкозы; г) имеет разветвленное строение.
5.Укажите общее химическое свойство дисахаридов и полисахаридов:
а) брожение; |
в) гидрирование; |
б) гидролиз; |
г) окисление. |
90
6. |
Укажите конечный продукт гидролиза крахмала: |
|
|
а) декстрины; |
в) глюкоза; |
|
б) мальтоза; |
г) сахароза. |
7. |
При взаимодействии целлюлозы с азотной кислотой образуется: |
|
|
а) сложный эфир; |
в) простой эфир; |
|
б) нитросоединение; |
г) аминосоединение. |
8. |
Какие соединения образуют красный осадок при нагревании с гид- |
|
роксидом меди (II): |
|
|
|
а) сахароза; |
в) глюкоза; |
|
б) целлюлоза; |
г) этаналь? |
9. |
Какие вещества вступают в реакцию этерификации: |
|
|
а) целлюлоза; |
в) пропаналь; |
|
б) фруктоза; |
г) крахмал? |
10. Определите число структурных звеньев в макромолекуле целлюлозы, если ее относительная молекулярная масса равна 2,5 миллионов:
а) 1540; б) 13900; в) 15432; г) 30864.
14. АМИНЫ
Амины — это производные аммиака (NH3), в молекуле которого один, два или три атома водорода замещены углеводородными радикалами. Например: метиламин (1), диметиламин (2), триметиламин (3)
|
H |
CH3 |
CH3 |
|
||
|
|
|
|
|
||
CH3–N |
(1) |
N–H (2) |
CH3 |
|
N |
(3) |
|
||||||
|
H |
CH3 |
CH3 |
|
||
|
|
|
|
|||
По числу атомов водорода в аммиаке, замещенных на углеводородный радикал, различают первичные (1), вторичные (2) и третичные (3) амины. В зависимости от природы углеводородного радикала различают алифатические, алициклические, ароматические и гетероциклические амины.
Номенклатура и изомерия. Названия аминов образуются от названий радикалов и слова амин, например, метиламин CH3NH2, триметиламин (CH3)3N, метилэтиламин C2H5NHCH3. Названия более сложных аминов образуются от названий соответствующих алканов: например, H3C–CH(NH2)–CH3 называется 2-аминопропан.
Изомерия аминов характеризуется изомерией углеводородного радикала (изомерия цепи) и положением аминогруппы в молекуле (изомерия положения), например, 1-аминобутан CH3–CH2–CH2–CH2–NH2 и 2-амино-
бутан CH3–CH(NH2)CH2–CH3.
91

Физические свойства. Метиламин, диметиламин и триметиламин — газообразные вещества, все остальные амины — жидкости или бесцветные кристаллические вещества. Низшие амины растворимы в воде и имеют запах аммиака. С увеличением молекулярной массы растворимость аминов в воде уменьшается.
Химические свойства. В молекулах аминов, как и в молекуле аммиака, атом азота имеет одну неподеленную пару электронов. В водном растворе и в присутствии кислот эта электронная пара взаимодействует с положительно заряженным ионом водорода и присоединяет его:
H
H – N + HOH
+ HOH
H
H
H3С–N + HOH
+ HOH 
H
H
H – N + H++Cl– H
+ H++Cl– H
H
H3С–N + H++Cl–
+ H++Cl–
H
[NH4]+ + OH– , где [NH4]+ – ион аммония
[Н3C–NH3]+ + OH– , где [H3C– NH3]+ – ион метиламмония

 [NH4]+ Cl– (хлорид аммония)
[NH4]+ Cl– (хлорид аммония)
[Н3C–NH3]+ Cl– (хлорид метиламмония)
Поэтому растворы аминов в воде имеют щелочную реакцию. Они изменяют цвет индикаторов: фенолфталеина — в малиновый, лакмуса — в синий.
Однако, по сравнению с аммиаком амины — более сильные основания. Это объясняется тем, что в молекуле метиламина СH3–NH2 к атому азота сдвинуты электронные облака от атомов водорода метильной группы и от двух атомов водорода непосредственно:
H H H
H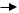 N
N H
H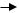 C
C 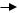 N
N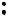
H
H H
В результате атом азота в молекуле метиламина приобретает больший по значению отрицательный заряд, чем атом азота в молекуле амми-
92
ака. Благодаря избыточному отрицательному заряду атом азота в молекулах аминов сильнее притягивает к себе протоны, чем в молекуле аммиака.
Органические амины горят на воздухе.
4CH3–NH2 + 9O2 4CO2 + 10H2O + 2N2
14.1. АНИЛИН
Анилин — простейший представитель первичных ароматических аминов:
NH2
C6H5–NH2 или
Получение. Анилин и другие первичные ароматические амины получают восстановлением нитросоединений
катализатг ор, t0
C6H5NO2 + 6H C6H5NH2 + 2H2O
Эта реакция известна как реакция Зинина.
Физические свойства. Анилин — бесцветная маслянистая жидкость
схарактерным запахом, мало растворим в воде и сильно ядовит. На воздухе быстро окисляется.
Химические свойства. Анилин реагирует с кислотами с образованием солей, но цвет лакмуса не изменяет. Это объясняется тем, что бензольное ядро оттягивает свободную электронную пару от атома азота аминогруппы. Поэтому электронная плотность на атоме азота в молекуле анилина уменьшается, и он слабее притягивает к себе протоны. В этом случае основные свойства анилина проявляются слабее по сравнению
спредельным алифатическим амином метиламином CH3–NH2.
C6H5 :NH2 + H2O  [C6H5NH3]+OH–
[C6H5NH3]+OH–
гидроксид фениламмония
C6H5 :NH2 + HCl [C6H5NH3]+Cl– или C6H5NH2 HCl
хлорид фениламмония (или солянокислый анилин)
[C6H5NH3]Cl– хорошо растворим в воде. При действии на него щелочи анилин выделяется в свободном виде.
[C6H5 NH3 ]Cl + NaOH C6H5NH2 + NaCl + H2O
Атомы водорода бензольного ядра анилина легко замещаются галогенами. При действии бромной воды на водный раствор анилина выделяется белый осадок 2,4,6 триброманилина.
93

|
NH2 |
|
|
|
NH2 |
|
||||||
|
|
|
|
|
|
|
|
|
||||
6 |
|
|
1 |
2 |
|
|
Br |
|
|
1 Br |
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|||||
|
|
|
+ 3Br2 |
|
6 |
|
|
|
2 |
+ 3HBr |
||
5 |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|||||
3 |
|
|
|
|
|
|
||||||
|
|
5 |
3 |
|
||||||||
|
|
|
|
|
|
|
|
|||||
|
4 |
|
|
|
|
4 |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Br |
|
|||
Применение. Анилин применяется для получения анилиновых красителей, лекарств, взрывчатых веществ, анилиноформальдегидных смол.
ВОПРОСЫ И УПРАЖНЕНИЯ
1.Что такое амины?
2.Напишите формулы всех изомеров аминопропана.
3.Напишите структурные формулы аминов: а) 3-аминопентан; б) 1,5 диаминогексан; в) 2,3 диаминобутан;
г) 3-амино-4метилгексан.
4.Объясните, почему у диметиламина основные свойства сильнее, чем у метиламина.
5.Напишите уравнения реакций для превращений:
CH4 CH3NO2 CH3NH2 [CH3NH3]Cl CH3NH2 N2
6.Объясните, почему ароматические амины имеют более слабые основные свойства, чем предельные алифатические амины.
7.Какое соединение — дифениламин (C6H5)2NH или фениламин C6H5NH2 имеет более сильные основные свойства?
8.Как получить анилин из карбида кальция? Напишите уравнения ре-
акций.
9.Укажите химические способы разделения смеси бензола и анилина.
ЗАДАЧИ
1.26,8 г раствора соляной кислоты с массовой долей хлористого водорода потребовалось для нейтрализации 10 г технического водного раствора диметиламина. Определите массовую долю амина в техническом растворе. (Ответ: 33 %)
2.Полученная соль первичного амина при взаимодействии с хлороводородом содержит 43,48 % хлора. Определите молекулярную формулу амина. Какой объем (н.у.) азота образуется при сжигании 9 г этого амина? (Ответ: С2H5NH2, 2,24 л)
94