Материал: Ткачёв С.В. Введение в органическую химию

этанола ( = 0,8 г/мл). Вычислите массу этого раствора глюкозы. (Ответ: 1095,6 г)
13.5. ДИСАХАРИДЫ
Дисахариды образуются при отщеплении воды от двух молекул гексоз. Наиболее важными из дисахаридов являются сахароза, мальтоза
илактоза. Все они имеют одну и ту же эмпирическую формулу С12Н22О11
иявляются изомерами.
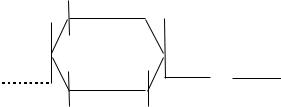
Сахароза Строение. Молекула сахарозы состоит из остатков глюкозы и фрук-
тозы, соединенных между собой атомом кислорода:
|
CH2OH |
|
|
|
|
|
|
|
|
|
O |
|
|
H |
||
H |
|
O |
H |
НОН2С |
|
|
||||||||||
|
|
|
|
|
||||||||||||
|
|
|
|
|
H |
|
OH |
|
||||||||
|
|
|
H |
|
|
|
|
|
|
|||||||
|
OH |
|
|
|
|
|
|
|||||||||
|
|
|
O |
|
|
|
|
|
|
|
CH2OH |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
OH |
|
H |
||||||
|
H |
OH |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
В молекуле сахарозы нет ни альдегидной группы, ни полуацетального гидроксила, но имеются гидроксильные группы.
Получение. Сахароза содержится во многих растениях, но особенно ее много в сахарной свекле и в сахарном тростнике. Из этих растений сахарозу и получают.
Физические свойства. Сахароза — это обычный сахар. Это кристаллическое белое вещество сладкого вкуса, очень хорошо растворяется в воде. Температура плавления сахарозы 160 °С. При охлаждении расплавленной сахарозы она превращается в аморфную прозрачную массукарамель.
Химические свойства. В присутствии разбавленных минеральных кислот и при нагревании происходит гидролиз сахарозы. В результате гидролиза образуются глюкоза и фруктоза.
С12Н22О11 + Н2О С6Н12О6 + С6Н12О6
Сахароза легко взаимодействует с гидроксидами металлов, образуя растворы сахаратов. В отличие от глюкозы сахароза не дает реакции «серебряного зеркала», не восстанавливается другими восстановителями.
Изомеры сахарозы — мальтоза и лактоза. Мальтоза состоит из двух остатков глюкозы; лактоза — из остатков глюкозы и галактозы.
Применение. Сахароза применяется в основном в пищевой промышленности.
85
ВОПРОСЫ И УПРАЖНЕНИЯ
1.Как отличить растворы глюкозы и сахарозы, находящиеся в разных пробирках?
2.Напишите уравнения реакций, при помощи которых сахарозу можно превратить в этанол.
3.Сколько глюкозы и фруктозы: а) в молях; б) в граммах можно получить при гидролизе 5 моль сахарозы?
ЗАДАЧА
Какая масса сахарозы потребуется для гидролиза, чтобы из образовавшейся глюкозы получить 54 г молочной кислоты при выходе ее 60 %? (Ответ: 171 г)
ТЕСТОВЫЙ САМОКОНТРОЛЬ ПО ТЕМЕ «УГЛЕВОДЫ. МОНОСАХАРИДЫ. ДИСАХАРИДЫ»
1. Укажите общую формулу углеводов:
а) CnH2n+1OH; |
в) CnH2n+1CHO; |
б) Cn(H2O)m; |
г) CnH2n+1COOH. |
2.Охарактеризуйте химическое строение глюкозы: а) гексоза; б) альдегидоспирт;
в) в циклической форме присутствует полуацетальный гидроксил; г) в растворе устанавливается равновесие между - и -формами.
3.Какие вещества являются изомерами по отношению друг к другу:
а) глюкоза и мальтоза; |
в) сахароза и мальтоза; |
б) глюкоза и фруктоза; |
г) сахароза и лактоза? |
4. Укажите процессы, ведущие к образованию глюкозы:
а) гидролиз крахмала; |
в) фотосинтез; |
б) гидролиз сахарозы; |
г) гидролиз целлюлозы. |
5.Какие продукты образуются при окислении глюкозы аммиачным раствором оксида серебра:
а) глюконовая кислота и вода; б) глюконовая кислота и металлическое серебро; в) многоатомный спирт и вода; г) фруктоза и вода?
6.Укажите группы веществ, которые дают реакцию «серебряного зеркала»:
а) глюкоза, глицерин, этиленгликоль; б) глицерин, глюкоза, сахароза;
в) глюкоза, формальдегид, метановая кислота; г) глюкоза, молочная кислота, фруктоза.
86
7. |
Укажите вещество, которое можно использовать для обнаружения |
|
глицерина, ацетальдегида, уксусной кислоты и глюкозы: |
||
|
а) гидроксид меди (II); |
в) водород; |
|
б) оксид серебра; |
г) гидроксид натрия. |
8. |
При действии ферментов глюкоза подвергается: |
|
|
а) гидролизу; |
в) брожению; |
|
б) гидрированию; |
г) дегидратации. |
9.Охарактеризуйте химическое строение фруктозы: а) пентоза; б) имеется карбонильная группа в молекуле;
в) кетоноспирт; г) имеются гидроксильные группы.
10.Охарактеризуйте свойства сахарозы:
а) сладкий вкус; б) растворима в воде;
в) в воде распадается на ионы; г) при нагревании в присутствии кислот идет гидролиз.
13.6. ПОЛИСАХАРИДЫ
Молекулы полисахаридов состоят из большого числа остатков гексоз (мономеров). Остатки гексоз связаны между собой в длинные цепи различной длины. Эти цепи имеют разную молекулярную массу. Полисахариды имеют общую молекулярную формулу (С6Н10О5)n, где n — число гексоз. При гидролизе полисахаридов образуются дисахариды или моносахариды. Важнейшие полисахариды — крахмал, целлюлоза (клетчатка).
Крахмал
Строение. Макромолекулы крахмала состоят из остатков молекул циклической -глюкозы.
Макромолекулы крахмала различаются по строению: наряду с линейными молекулами с молекулярной массой в несколько сотен тысяч (амилоза) имеются молекулы разветвленного строения, молекулярная масса которых достигает нескольких миллионов (амилопектин).
CH2OH
H H H
OH H
O
H OH
87
Получение. Получают крахмал чаще всего из картофеля, риса и кукурузы.
Физические свойства. Крахмал — белый аморфный порошок. Практически нерастворим в холодной воде, но получены водорастворимые формы крахмала. В горячей воде крахмал образует коллоидный раствор, который при охлаждении превращается в клейстер.
Химические свойства.
1.Нагревание. Крахмал не имеет определенной температуры плавления и при нагревании разлагается на декстрин и другие продукты.
2.Взаимодействие с йодом. Крахмал дает характерное синее окрашивание с йодом. Это позволяет обнаруживать крахмал в пищевых продуктах.
3.Гидролиз. При нагревании с водой в присутствии кислоты или при действии ферментов крахмал легко подвергается гидролизу.
(C6H10O5)n (C6H10O5)m xC12H22O11 nC6H12O6
крахмал декстрины мальтоза глюкоза
Применение. Крахмал применяется в производстве антибиотиков, витаминов, колбас, кондитерских изделий, в фармации и медицине, для накрахмаливания белья. В промышленности крахмал перерабатывают
вэтиловый спирт, глюкозу, декстрины и другие вещества.
Ворганизме крахмал гидролизуется до глюкозы.
Целлюлоза
Строение. Макромолекулы целлюлозы состоят из остатков молекул β-глюкозы и имеют только линейное строение. Макромолекулы целлюлозы располагаются в одном направлении и образуют волокна (лен, хлопок, конопля). В каждом остатке молекулы глюкозы содержатся три гидроксильные группы, что выражается формулой [C6H7O2(OH)3]n. Общее число остатков глюкозы в макромолекуле целлюлозы равно примерно 6000–12000, что соответствует относительной молекулярной массе 1–2 миллиона.
Получение. Целлюлоза — основная составная часть оболочки растительных клеток. До 98 % целлюлозы содержится в хлопке, в древесине — около 50 %. Вата — это почти чистая целлюлоза и представляет собой очищенный хлопок. Основную массу целлюлозы получают из древесины.
Физические свойства. Целлюлоза — белое волокнистое вещество, нерастворимое в воде и органических растворителях. Не имеет ни вкуса, ни запаха.
Химические свойства
1. Гидролиз. При нагревании с разбавленной серной кислотой под давлением целлюлоза превращается в глюкозу.
88
H SO
(C6H10O5)n + nH2O 2 4 nC6H12O6
2. Реакция этерификации. При взаимодействии целлюлозы с азотной кислотой в присутствии концентрированной серной кислоты образуются сложные эфиры -моно-, ди- и тринитратцеллюлозы:
[C6H7O2(ONO2)(OH)2]n;
[C6H7O2(ONO2)2(OH)]n;
[C6H7O2(ONO2)3]n
Нитраты целлюлозы — горючие вещества. Тринитрат целлюлозы (пироксилин) — сильно взрывчатое вещество.
Взаимодействует целлюлоза и с органическими кислотами:
H SO
[C6H7O2 (OH)3]n + 3nCH3COOH 2 4 [C6H7O2(OCOCH3)3]n + 3nH2O
Обычно образуется смесь моно-, ди- и триацетатов целлюлозы:
[C6H7O2(OCOCH3)(OH)2]n;
[C6H7O2(OCOCH3)2(OH)]n;
[C6H7O2(OCOCH3)3]n
Диацетат и триацетатцеллюлоза используются для получения искусственного ацетатного волокна.
3. Горение (полное окисление)
(C6H10O5)n + 6nO2 t 6nCO2 + 5nH2O
4. Термическое разложение целлюлозы без доступа воздуха. В зависимости от температуры разложения образуются древесный уголь, вода, метан, метанол, уксусная кислота, ацетон и другие продукты.
Применение. Целлюлоза в виде древесины используется в строительстве, в быту. Большое количество целлюлозы перерабатывается на бумагу, этанол, вату, простые и сложные эфиры. Простые и сложные эфиры целлюлозы применяются в различных отраслях промышленности и в медицине.
ВОПРОСЫ И УПРАЖНЕНИЯ
1.Что такое полисахариды? Напишите общую молекулярную формулу полисахаридов.
2.В чем отличие крахмала от целлюлозы?
3.Сколько звеньев С6Н10О5 содержится в макромолекуле целлюлозы: а) льняного волокна (Mr = 5900000);
б) хлопкового волокна (Mr = 1750000)?
89