Материал: Ткачёв С.В. Введение в органическую химию

Свободные углеводородные радикалы взаимодействуют с молекулами хлора и образуют свободные радикалы хлора:
CH3 + Cl : Cl CH3Cl + Cl
В. Обрыв цепи. Радикалы соединяются с друг другом:
Cl + Cl Cl2
CH3 + CH3 CH3 – CH3
CH3 + Cl CH3Cl
2. Все предельные углеводороды горят с образованием оксида углерода (IV) и воды:
CH4 + 2O2 CO2 + 2H2O
3. При сильном нагревании без доступа воздуха предельные углево-
дороды разлагаются:
CH4 1000 C C + 2H2
2CH4 1500 C H – C C – H + 3H2
CH3 – CH3 500 C, Ni H2C = CH2 + H2
4. В присутствии катализаторов и при нагревании углеводородов нормального строения происходит реакция изомеризации и образование углеводородов разветвленного строения.
t, AlCl
CH3 – CH2 – CH2 – CH2 – CH3 3 CH3 – CH – CH2 – CH3
CH3
Реакция изомеризации не происходит, если углеводород содержит в молекуле меньше четырех атомов углерода.
ВОПРОСЫ И УПРАЖНЕНИЯ
1.Какие элементы входят в состав углеводородов?
2.Как делятся углеводороды в зависимости от характера связей между атомами в углеродной цепи?
3.Напишите общую формулу предельных углеводородов. Приведите примеры предельных углеводородов.
4.Что называется гомологическим рядом? Что такое гомологи?
5. Назовите первые десять членов гомологического ряда алканов
исоответствующие им радикалы.
6.Какую геометрическую форму имеет молекула метана? Укажите значение угла между связями С – Н в этой молекуле.
7.Что такое гибридизация? Какой тип гибридизации характерен для метана и его гомологов?
15
8.Какой тип изомерии существует в ряду алканов? Какие алканы не имеют изомеров?
9.Составьте структурные формы всех изомеров н-гексана. Назовите их по международной номенклатуре.
10.Составьте структурные формулы:
а) 3-этилгептана; |
в) 2-метил-3-этилгептана; |
б) 2,4-диметилгексана; |
г) 3-метил-5-этилгептана. |
11.Какие реакции наиболее характерны для алканов?
12.Бром реагирует с метаном подобно хлору. Напишите уравнения реакций замещения.
ЗАДАЧИ
1.Какой объем водорода (н.у.) образуется при полном термическом разложении 2 моль метана? (Ответ: 89,6 л).
2.Какой объем воздуха (н.у.) потребуется для полного сжигания смеси 3 моль метана и 20 л этана, если воздух содержит 20,94 % кислорода по объему? (Ответ: 880,61).
3.4,3 г органического вещества сожгли в кислороде. Образовалось 6,72 л углекислого газа и 6,3 г воды. Плотность вещества по водороду равна 43. Определить формулу органического вещества. (Ответ: С6Н14).
4.При сгорании 0,56 л (н.у.) н-бутана получили углекислый газа. Этот газ пропустили через 26,7 мл раствора гидроксида калия с массовой долей его 32 % (плотность раствора 1,31 г/мл). Определите массовую долю соли в растворе после пропускания углекислого газа. (Ответ: 35,1 %).
5.На сжигание 6 л смеси пропана и бутана израсходовали 37,2 л кислорода. Объемы газов измерены при нормальных условиях. Определите состав газовой смеси в объемных долях (%). (Ответ: 20 % пропана).
ТЕСТОВЫЙ САМОКОНТРОЛЬ ПО ТЕМЕ «ПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ»
1. |
Укажите формулу предельного углеводорода: |
|||
|
а) С7Н14; |
б) С8Н18; |
в) С6Н6; |
г) С6Н12. |
2. |
Укажите название предельного углеводорода, который имеет отно- |
|||
сительную плотность по водороду 36: |
|
|||
|
а) гексан; |
б) пентан; |
в) пропан; |
г) бутан. |
3. |
Укажите формулу предельного углеводорода, который содержит |
|||
20 атомов водорода: |
|
|
|
|
|
а) С8Н20; |
б) С9Н20; |
в) С10Н20; |
г) С7Н20. |
4. |
Укажите геометрическую форму молекулы хлороформа: |
|||
|
а) линейная; |
|
в) плоскостная; |
|
|
б) пирамидальная; |
г) тетраэдрическая. |
||
16

5. Укажите соединение, которое является изомером н-пентана:
|
а) CH3 – CH – CH3 |
|
|
|
б) CH3 – CH – CH2 – СН3 |
||||||
|
|
CH3 |
|
|
|
|
|
CH3 |
|
|
|
|
в) CH3 – CH2 – CH2 – |
|
СН2 |
г) |
|
CH2 – CH2 – |
|
СН2 |
|||
|
|
|
|
||||||||
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
CH3 |
CH3 |
||||||
6. |
Укажите число изомеров для соединения формулы С2Н4Br2: |
||||||||||
|
а) 3; |
б) 4; |
в) 2; |
г) 1. |
|
|
|
||||
7. |
Укажите соединение с максимальной температурой кипения: |
||||||||||
|
а) н-пентан; |
в) 2,2–диметилпропан; |
|
|
|
||||||
|
б) изопентан; |
г) изобутан. |
|
|
|
||||||
8. |
Укажите число изомеров для алкана с молекулярной массой 86: |
||||||||||
|
а) 5; |
б) 4; |
в) 2; |
г) 3. |
|
|
|
||||
9. |
Какая реакция характерна для предельных углеводородов: |
||||||||||
|
а) обмена; |
в) соединения; |
|
|
|
||||||
|
б) замещения; |
г) присоединения? |
|
|
|
||||||
10. Укажите, какое из веществ является твердым при комнатной температуре:
а) СН4; б) С6Н14; в) С5Н12; г) С20Н42.
11.Алканы растворяются:
а) в дистиллированной воде; б) бензоле; в) метаноле;
г) в водопроводной воде.
12.Укажите, какое вещество будет реагировать с н-бутаном: а) перманганат калия в щелочной среде; б) перманганат калия в кислой среде;
в) холодный разбавленный раствор азотной кислоты; г) бром при освещении светом.
13.Охарактеризуйте гомологи метана: а) отличаются на группу –СН2 ;
б) имеются газообразные, жидкие и твердые вещества;
в) все предельные углеводороды горят с образованием оксида углерода (IV) и воды;
г) названия углеводородов имеют окончание -ан.
17

СН3
14. Охарактеризуйте соединение: СН3 – С – СН3
СН3
а) алкан; б) углеводород разветвленного строения;
в) имеет более высокую температуру кипения, чем н-пентан; г) изомер пентана.
15.Какие вещества образуются при хлорировании метана: а) хлористый водород; б) дихлорэтан; в) дихлорметан; г) хлороформ?
16.Какие пары соединений являются гомологами относительно друг
друга:
а) пропан и циклопропан; б) пропан и н-пентан;
в) 1-хлорпропан и 1-хлорбутан; г) н-бутан и 2-метилпропан?
17.Охарактеризуйте свободные радикалы:
а) образуются при гомолитическом расщеплении ковалентной
связи;
б) имеют неспаренные электроны; в) реагируют с углеводородами с образованием углеводородных
радикалов; г) соединяются друг с другом.
18. |
Какие углеводороды не вступают в реакции изомеризации: |
|||
|
а) метан; |
б) этан; |
в) пропан; |
г) бутан? |
19. |
Укажите название алкана, в молекуле которого содержится 16 |
|||
связей -типа: |
|
|
|
|
|
а) пропан; |
б) бутан; |
в) пентан; |
г) этан. |
20. Какие факторы сместят вправо равновесие процесса
2CO(г) + 5Н2(г)  С2Н6(г) + 2Н2О(г):
С2Н6(г) + 2Н2О(г):
а) понижение давления; б) повышение давления;
в) поглощения паров воды концентрированной серной кислотой; г) применение катализатора?
18
5. НЕПРЕДЕЛЬНЫЕ АЛИФАТИЧЕСКИЕ УГЛЕВОДОРОДЫ
Непредельными или ненасыщенными углеводородами называются углеводороды, в молекулах которых атомы углерода связаны между собой кратными (двойными или тройными) связями. Наиболее важными из непредельных алифатических углеводородов являются этиленовые, диеновые и ацетиленовые углеводороды.
5.1. ЭТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ (ОЛЕФИНЫ, АЛКЕНЫ)
Этиленовые углеводороды имеют одну двойную связь и общую формулу CnH2n. Простейшее соединение с двойной связью — это этилен СН2 = СН2. В молекуле этилена появляются связи и -, и -типа. Согласно экспериментальным данным, все шесть атомов располагаются в одной плоскости и углы между связями очень близки к 120° (рис. 6). Плоское строение молекулы и угол между связями 120° позволяют считать, что для образования -связей каждый атом углерода соединяется с тремя другими атомами (одним атомом углерода и двумя атомами водорода). В этом случае в гибридизации участвуют только три электронных облака — одного s-электрона и двух р-электронов. Происходит sp2-гибри- дизация (рис. 6). Но у каждого атома углерода остается по одному р-электрону, облака которых не участвуют в гибридизации.
Н |
|
Н |
|
|
|
|
|
|
|
1200 |
|
Н |
|
Н |
С |
С |
|
|
|
|
|
|
||
Н |
1200 |
Н |
С |
С |
Н |
Н |
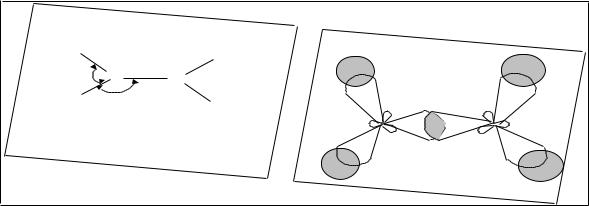
Рис. 6. Схема образования -связей в молекуле этилена
Оси этих электронных облаков направлены перпендикулярно плоскости молекулы и перекрываются между собой выше и ниже плоскости молекулы. Образуется второй тип связи между атомами углерода. Эта связь называется -связью (рис. 7).
19