Материал: Ткачёв С.В. Введение в органическую химию

10. Укажите общую формулу сложного эфира:
а) R – O –R б) R – OН |
в) R – O – C |
O |
г) NH2 |
– R – COOН |
|
OR |
|||||
|
|
|
|
4. УГЛЕВОДОРОДЫ. ПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
Углеводороды — самые простые органические соединения. В состав углеводородов входят только два элемента: углерод и водород. В зависимости от характера связей между атомами в углеродной цепи углеводороды делят на предельные (насыщенные), непредельные (ненасыщенные) и ароматические углеводороды.
Предельные углеводороды. Углеводороды с общей формулой CnH2n+2, которые не присоединяют водород и другие элементы, называются предельными (насыщенными) углеводородами или алканами (парафинами). В общей формуле буква n — число атомов углерода в молекуле данного углеводорода.
Группа соединений, в которой каждый следующий член отличается от предыдущего на одну метиленовую группу (–СН2–), называется гомологическим рядом. Сходные по химическим свойствам соединения в гомологическом ряду называются гомологами. Например, гомологический ряд метана дан в табл. 2.
|
|
|
Таблица 2 |
|
Предельные углеводороды |
|
|
|
|
|
|
Формула |
Название |
Радикал |
Название радикала |
СН4 |
Метан |
СН3– |
Метил |
С2Н6 |
Этан |
С2Н5– |
Этил |
С3Н8 |
Пропан |
С3Н7– |
Пропил |
С4Н10 |
Бутан |
С4Н9– |
Бутил |
С5Н12 |
Пентан |
С5Н11– |
Пентил |
С6Н14 |
Гексан |
С6Н13– |
Гексил |
С7Н16 |
Гептан |
С7Н15– |
Гептил |
С8Н18 |
Октан |
С8Н17– |
Октил |
С9Н20 |
Нонан |
С9Н19– |
Нонил |
С10Н22 |
Декан |
С10Н21– |
Децил |
Остаток углеводорода без одного атома водорода называется алкильной группой или радикалом. Названия алкильных групп образуются от названий соответствующих алканов заменой окончания -ан на окончание -ил.
10

4.1. ЭЛЕКТРОННОЕ И ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ АЛКАНОВ
Простейший представитель алканов — метан СН4. Строение его молекулы можно выразить структурной (а) или электронной (б) формулой:
Н |
Н |
Н – С – Н |
Н С Н |
Н |
Н |
|
|
а |
б |
Однако эти формулы не отражают пространственного строения молекулы.
Экспериментально установлено, что молекула метана СН4 имеет форму тетраэдра с углом в 109028 между связями С – Н (рис. 3). Поскольку в молекуле метана четыре связи атома углерода расположены тетраэдрически и практически одинаковы, то для объяснения этого факта американский химик Л. Полинг в 1931 г. ввел понятие гибридизации. Сразу отметим, что гибридизиция — это не процесс, в результате которого атомы изменяются, а это просто способ, удобный для объяснения экспериментальных фактов. Согласно Л. Полингу гибридизация — это образование новых орбиталей с одинаковой энергией и симметрично расположенных в пространстве. Новые орбитали он назвал смешанными
или гибридными.
Как известно, в основном (невозбужденном) состоянии атом углерода имеет электронную конфигурацию 1s22s22p2, что изображается следующей схемой:
1s2 |
|
2s2 |
|
|
|
2p2 |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
При образовании химической связи атом углерода переходит в возбужденное состояние и один из 2s-электронов переходит на 2р-орбиталь:
1s2 |
|
2s1 |
|
|
|
2p3 |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
sр3 – гибридные орбитали
В возбужденном состоянии атом углерода имеет четыре неспаренных электрона: один 2s-электрон и три 2р-электрона — 1s22s12p3. При «сме-
11
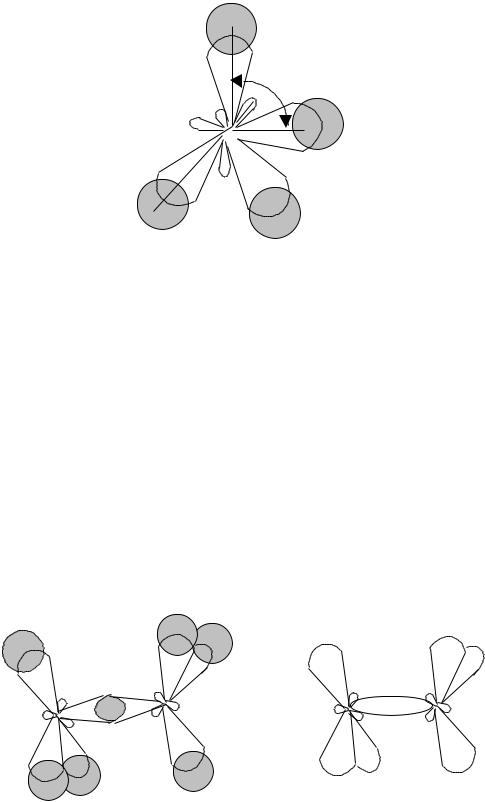
шивании» одной 2s-орбитали и трех 2р-орбиталей образуются четыре одинаковые sp3-гибридные орбитали (sp3-гибридизация). Все четыре sp3-гибридные орбитали строго ориентированы в пространстве, образуя тетраэдр (рис. 3).
Н
109028
Н
С
Н
Н
Рис. 3. Образование четырех связей между sp3-гибридными орбиталями атома углерода и 1s-орбиталью атома водорода в молекуле метана
sp3-Гибридные орбитали перекрываются с 1s-орбиталями четырех атомов водорода. Образуется прочная тетраэдрическая молекула с четырьмя -связями, которые направлены под углом 109028 друг к другу (рис. 3). В молекулах алканов в образовании -связей всегда участвуют гибридные sp3-орбитали. Например, молекула этана С2Н6 образована перекрыванием двух гибридных орбиталей атомов углерода с углом 109028 между связями С – Н (рис. 4). Во всех других алканах углеродная цепь имеет в пространстве форму зигзага также с углом в 109028 между связями С – Н (рис. 5).
Для атома углерода возможны еще sp2- и sp-гибридизации, которые описываются в разделах, посвященных химическим свойствам непредельных углеводородов и бензолу. О типе гибридизации орбиталей, участвующих в образовании связей, судят по величинам углов между связями в молекуле.
|
|
|
Н |
|
|
Н |
|
|
Н |
|
|
|
|
|
|
|
|
|
|
|
Н |
Н |
Н |
|
|
|
|
||
|
|
|
|
|
|
С |
|
С |
С |
С |
|
|
|
|
|||
|
|
|
Н Н |
Н |
|
Н |
Н |
|
Н |
|
|
|
|
|
|
Рис. 4. Образование молекулы этана
12
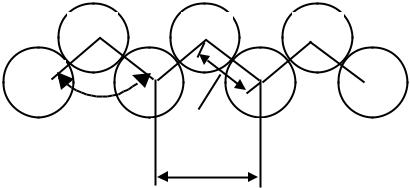
C |
C |
C |
C |
|
C |
109028 |
0,154 нм |
|
|
0,25 нм |
|
Рис. 5. Зигзагообразное строение углеродных цепей
4.2. ИЗОМЕРИЯ И НОМЕНКЛАТУРА АЛКАНОВ
Вокруг -связей возможно свободное вращение. Из-за этого в гомологическом ряду алканов наблюдается только изомерия цепи, которая характеризуется различным порядком соединения атомов углерода. Метан, этан и пропан не имеют изомеров. Бутан существует в виде двух изомеров; пентан — трех. С увеличением числа атомов углерода в молекуле число возможных изомеров увеличивается. Гексан существует в виде пяти изомеров, декан С10Н22 имеет семьдесят пять изомеров.
Для составления названий предельных углеводородов с разветвленной цепью, его рассматривают как продукт замещения атомов водорода различными радикалами. Затем поступают так.
1.Выбирают в формуле наиболее длинную углеводородную цепь и нумеруют атомы углерода с того конца, к которому ближе разветвление.
2.Называют радикалы (начиная с простейшего) и при помощи цифр указывают их место у нумерованных атомов углерода. Если у одного
итого же атома углерода находятся два одинаковых радикала, тогда номер повторяют дважды.
Число одинаковых радикалов указывают при помощи чисел на греческом языке («ди-два», «три-три», «тетра-четыре» и т. д.).
Полное название данному углеводороду дают по числу атомов углерода в нумерованной цепи. Названия углеводородов, начиная с пентана, образованы от греческих названий чисел. Для обозначения формулы углеводородов нормального строения в начале формулы названия ставят букву н: н-бутан, н-гексан и т. д.
4.3.ФИЗИЧЕСКИЕ СВОЙСТВА АЛКАНОВ
Унормальных алканов с увеличением длины углеводородной цепи повышаются температуры кипения и увеличиваются плотности. Метан, этан, пропан и бутан при нормальных условиях — газы, от пентана до
13

пентадекана (С15Н32) — жидкости, а следующие гомологи — твердые вещества. Температура кипения н-алканов выше, чем разветвленных изомеров. Алканы неполярны и поэтому практически нерастворимы в воде. Но они растворяются в органических растворителях, например, в бензоле
ичетыреххлористом углероде. В чистом состоянии алканы бесцветны
иимеют слабый запах.
Алканы широко распространены в природе, содержатся в нефти, природных и попутных газах.
4.4.ХИМИЧЕСКИЕ СВОЙСТВА АЛКАНОВ
1.При обычных условиях алканы химически малоактивны и не реагируют со щелочами, кислотами и окислителями. Для алканов характерны реакции замещения, так как все атомы в молекуле связаны прочными
-связями.
При нагревании алканы вступают в реакции замещения с галогенами (реакции галогенирования), с разбавленной азотной (реакции нитрования) и концентрированной серной (реакции сульфирования) кислотами.
h |
420 C |
+ H2O |
|
CH4 + Cl2 CH3Cl + HCl |
CH4 + HONO2 CH3NO2 |
||
CH3Cl + Cl2 |
h |
t C |
|
CH2Cl2 + HCl |
CH4 + HOSO3H CH3SO3H + H2O |
||
CH2Cl2 + Cl2 |
h |
|
|
CHCl3+ HCl |
|
|
|
CHCl3 + Cl2 |
h |
|
|
CCl4 + HCl |
|
|
|
При нагревании смеси метана с хлором (реакция хлорирования) выше 100 С или при освещении образуется смесь хлоропроизводных метана: хлорметан, дихлорметан, трихлорметан и тетрахлорметан. Эта реакция называется цепной реакцией и осуществляется в три стадии.
А. Инициирование (зарождение цепи). Гомолитическое расщепле-
ние молекулы хлора с образованием свободных радикалов: Cl
h h
Cl  Cl Cl + Cl
Cl Cl + Cl
Свободные радикалы — это атомы или группы атомов с неспаренными электронами ( H, Cl, CH3)
Б. Развитие цепи. Радикалы хлора взаимодействуют с углеводородом и образуются свободные углеводородные радикалы.
Н
Cl + Н
+ Н С
С Н
Н  H
H Cl +
Cl +  CH3
CH3
Н
14