Материал: Ткачёв С.В. Введение в органическую химию
9. Укажите физические свойства углеводородов: а) растворимы в воде; б) растворимы в бензине;
в) с увеличением молекулярной массы температура кипения повышается;
г) горючие вещества.
10.Укажите реагент, который позволит отличить этилен от ацетилена: а) щелочной раствор перманганата калия; б) бромная вода;
в) аммиачный раствор хлорида меди (I); г) концентрированная серная кислота.
11.Какая из реакций носит название реакции М. Г. Кучерова:
а) тримеризация ацетилена; б) окисление непредельных углеводородов раствором пермангана-
та калия;
в) гидратация ацетилена в присутствии Hg2+; г) гидратация этилена?
12. Какой тип реакции характерен для ацетиленовых углероводоро-
дов:
а) разложения; |
в) присоединения; |
б) замещения; |
г) обмена? |
13. Укажите вещества, которые обесцвечивают бромную воду:
а) изопрен; |
в) бутин-2; |
б) полиэтилен; |
г) 2-метилбутен-2. |
14.Укажите реакции, в которые вступают углеводороды с двойными
итройными связями:
а) гидратации; б) гидрирования;
в) присоединения галогеноводородов; г) полимеризации.
15. Укажите, какие вещества можно получить из ацетилена: а) винилхлорид; б) бензол;
в) уксусный альдегид; г) метан.
35

6. АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ (АРЕНЫ)
Ароматические углеводороды — это углеводороды, в молекулах которых имеется бензольное кольцо или ядро. Общая формула ароматических углеводородов CnH2n–6. Простейший представитель бензол. Его эмпирическая формула С6Н6.
6.1.СТРОЕНИЕ МОЛЕКУЛЫ БЕНЗОЛА
В1865 г. немецкий химик А. Ф. Кекуле предложил циклическую формулу бензола. Согласно А. Ф. Кекуле молекула бензола представляет собой замкнутый правильный шестигранник (цикл), в котором атомы углерода соединены между собой чередующимися простыми и двойными связями. Кроме того, каждый атом углерода связан с атомом водорода.
или
Однако эта формула не объясняет многих свойств бензола. Бензол не проявляет свойства ненасыщенных соединений: он не обесцвечивает бромную воду и раствор перманганата калия. Для бензола более характерны реакции замещения, а не присоединения. Понять это противоречие помогло изучение строения молекулы бензола современными физическими методами.
Было установлено, что молекула бензола имеет циклическое строение, и что все шесть атомов углерода лежат в одной плоскости. Расстояния между центрами соседних атомов углерода в молекуле одинаковы и равны 0,140 нм. Это говорит о том, что в бензоле нет простых и двойных связей.
Электронная теория так объясняет это явление. Все атомы углерода в молекуле бензола находятся в состоянии sp2-гибридизации. Три гибридных электронных облака каждого атома углерода образуют в плоскости кольца две -связи с соседними атомами углерода и одну -связь с атомом водорода. Углы между этими связями равны 120° (рис. 9). Облако четвертого электрона, которое не участвует в гибридизации, расположено перпендикулярно к плоскости -связей. Каждое такое облако одинаково перекрывается с электронными облаками обоих соседних с ним атомов углерода (рис. 10, а). В проекции на плоскость молекулы эти электронные облака будут казаться перекрывающимися окружностями (рис. 10, б). В молекуле образуются не три отдельные -связи, а единая -электронная система из шести электронов, общая для всех атомов углерода (рис. 10, в).
36
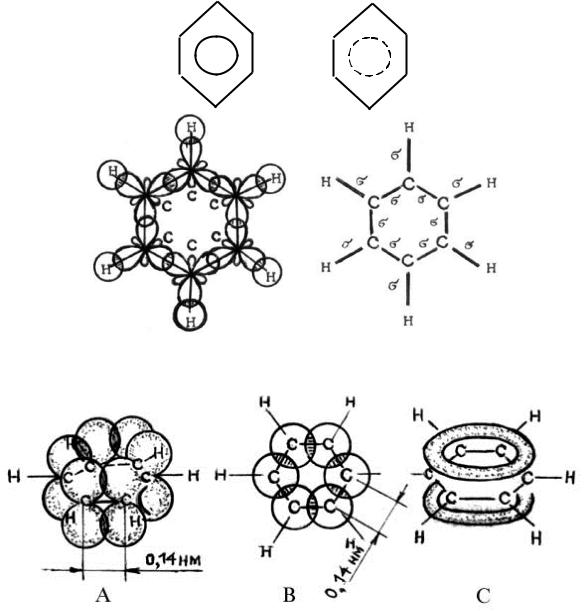
Под влиянием этого общего для молекулы -электронного облака и сокращаются расстояния между атомами углерода с 0,154 до 0,140 нм. Сочетание шести -связей с единой -системой называется ароматической связью. Цикл из шести атомов углерода, связанных ароматической свя-
зью, называется бензольным кольцом или бензольным ядром. Посколь-
ку электронная плотность распределяется в молекуле равномерно, все связи между атомами углерода оказываются совершенно одинаковыми. Графически это можно изобразить так:
Рис. 9. Схема образования -связей в молекуле бензола
а |
|
б |
|
в |
|
|
|
|
|
Рис. 10. Схема образования -связей в молекуле бензола:
а, б — боковое перекрывание облаков р-электронов в двух проекциях; в — распределение электронной плотности молекулярного -облака над плоскостью и под плоскостью атомных ядер
37

6.2. ИЗОМЕРИЯ И НОМЕНКЛАТУРА
При замещении водородных атомов в молекуле бензола различными радикалами образуются гомологи бензола: метилбензол (I), этилбензол (II), пропилбензол (III):
|
C – CH3 |
|
|
C – CH2 – CH3 |
|
C – CH2 – CH2 – CH3 |
|||
|
|
|
|
|
|
||||
HC |
|
CH |
HC |
|
|
CH |
HC |
|
CH |
|
|
|
|
||||||
HC |
|
CH |
|
|
|
||||
|
|
||||||||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
||
HC |
CH |
HC |
|
CH |
|||||
|
|
|
|
||||||
|
CH |
|
|
CH |
|
CH |
|||
|
|
|
|
|
|
||||
|
(I) |
|
|
(II) |
|
(III) |
|||
|
|
|
|
|
|
||||
или сокращенно: С6Н5 – СН3, |
С6Н5 – С2Н5, |
С6Н5 – С3Н7. Радикал С6Н5 – |
|||||||
называют фенилом. |
|
|
|
|
|
|
|
||
Для гомологов бензола характерна изомерия положения заместителей. Соединения ряда бензола, у которых два заместителя стоят у соседних атомов углерода (положение 1,2), называются орто-соединениями (о-). В мета-соединениях (м-) заместители расположены через один атом углерода (положение 1,3), в пара-соединениях (п-) — через два атома углерода (положение 1, 4). Ниже приводятся формулы трех изомеров ксилола: орто- (I), мета- (II) и пара- (III):
|
CH3 |
|
|
CH3 |
|
CH3 |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||
6 |
|
|
1 |
CH3 |
6 |
|
1 |
|
2 |
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
2 |
|
|
|
6 |
|
|
|
|
2 |
|||
|
|
|
|
|
|
|
|
||||||||
5 |
|
|
|
|
|
|
|
3 |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
3 |
5 |
|
5 |
|
|
|
|
|
||||
|
|
|
|
|
|
|
3 |
||||||||
|
4 |
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
4 |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
CH3 |
||||
|
(I) |
|
|
(II) |
|
(III) |
|||||||||
При помощи цифр в названии вещества указывают положение замещающих групп. Например, вышеприведенные формулы соединений могут быть названы так: 1,2-диметилбензол (I), 1,3-деметилбензол (II), 1,4-диметилбензол (III).
Известны ароматические соединения, в боковых цепях которых имеются радикалы непредельных углеводородов. Простейшим представителем таких углеводородов является винилбензол или стирол:
38
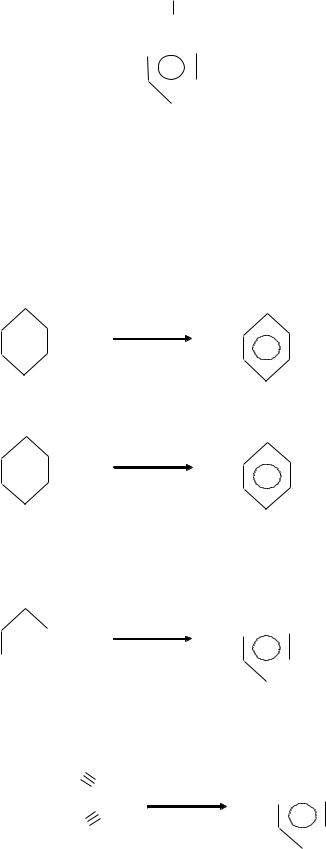
HC = CH2
C
HC CH
CH
HC  CH
CH
CH
6.3.ПОЛУЧЕНИЕ БЕНЗОЛА И ЕГО ГОМОЛОГОВ
Впромышленности источниками ароматических углеводородов являются каменный уголь и нефть. Например, бензол и гомологи бензола образуются соответственно из цикллогексана и его производных, находящихся в нефти, при дегидрировании:
|
CH2 |
|
|
CH |
|
|
|
|
|
|
|
H2C |
CH2 |
Pt или Pd |
HC |
CH |
+ 3H2 |
|
|
|
|||
H2C |
CH2 |
300 °C |
HC |
CH |
|
|
|
||||
|
CH2 |
|
|
CH |
|
|
|
|
|
|
|
HC – CH3 |
|
|
C – CH3 |
|
|
|
|
|
|
|
H2C |
CH2 |
Pt , 300 °C |
HC |
CH |
+ 3H2 |
|
|
|
|||
H2C |
CH2 |
|
HC |
CH |
|
|
|
||||
|
CH2 |
|
|
CH |
|
|
|
|
|
|
При тех же условиях н-гексан превращается в бензол:
CH2
H2C |
CH3 Pt , 300 °C |
H2C  CH3
CH3
CH2
CH
HC CH
CH
+ 4H2
HC  CH
CH
CH
При пропускании ацетилена при 450–500 °С над активированным углем образуется также бензол:
HC |
HC |
CH |
|
||||
|
C, 400–500 |
||||||
|
|
|
|
+ |
|
|
|
|
|
|
|
|
CH |
|
|
HC |
|
HC |
|
||||
|
|
|
|
|
|
|
|
CH HC CH HC
CH HC  CH
CH
CH
39