Материал: Ткачёв С.В. Введение в органическую химию

Для качественного определения фенола в водных растворах используют его взаимодействие с хлоридом железа (III)FeCl3. Образуется фиолетовая окраска раствора.
Применение. Фенол применяют для производства фенолформальдегидных пластмасс, красителей, лекарств, взрывчатых веществ и других продуктов. Фенол токсичен, вызывает ожоги кожи и применяется в медицине как антисептик.
ВОПРОСЫ И УПРАЖНЕНИЯ
1.Что такое фенолы? Чем фенолы отличаются от ароматических спиртов по химическому строению?
2.Какие типы изомерии известны для фенолов?
3.Напишите формулы одно- и двухатомных фенолов.
4.Объясните взаимное влияние атомов в молекуле фенола.
5.Имеется вещество следующего строения:
HO – 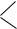

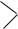 – CH2OH
– CH2OH
Как оно будет взаимодействовать: а) с натрием; б) с гидроксидом натрия? Напишите уравнения реакций.
6. Напишите структурные формулы соединений:
а) м-нитрофенол; |
в) о-крезол; |
б) n-бромфенол; |
г) 2,6-диметилфенол. |
7. Напишите уравнения реакций для превращения:
СаС2 С2Н2 С6Н6 С6Н5Br C6H5OH C6H2Br3OH
ЗАДАЧИ
1.Бромная вода, которая содержит 6 г брома, полностью прореагировала с 23,5 г водного раствора фенола. Определите массовую долю фенола в растворе. (Ответ: 5%)
2.При нейтрализации 100 г водного раствора фенола потребовалось
25 мл раствора гидроксида калия с массовой долей его 40 % ( = 1,4 г/мл). Сколько бромной воды с массовой долей брома 1 % надо прилить к 100 г раствора фенола, чтобы весь фенол прореагировал? (Ответ: 12 кг)
3. При действии избытка натрия на смесь этанола и фенола выделилось 6,72 л водорода (н.у.). Для полной нейтрализации этой же смеси потребовалось 25 мл раствора гидроксида калия с его массовой долей 40 % ( =1,4 г/мл). Определите состав исходной смеси (в % по массе). (Ответ: 40,6 % С2Н5ОН; 59,4 % С6Н5ОН)
55
ТЕСТОВЫЙ САМОКОНТРОЛЬ ПО ТЕМЕ «СПИРТЫ. ФЕНОЛЫ»
1. Укажите общую формулу предельных одноатомных спиртов:
а) CnH2n+1OH; б) CnH2n+2OH; в) CnH2nOH; г) CnHn+1OH.
2.Охарактеризуйте соединение СН3 – СН(ОН) – СН2 – СН3: а) предельный одноатомный спирт; б) двухатомный спирт; в) бутанол-1; г) бутанол-2.
3.В молекуле глицерина содержится:
а) три первичные гидроксильные группы; б) три вторичные гидроксильные группы;
в) одна первичная и две вторичные гидроксильные группы; г) две первичные и одна вторичная гидроксильная группы.
4.Укажите вторичные спирты:
а) 2 метил-бутанол-1; |
в) гексанол-2; |
б) гексанол-1; |
г) 2,2-диметилпентанол-3. |
5. Укажите третичный спирт: |
|
а) бутанол-1; |
в) 2-метилпропанол-2; |
б) бутанол-2; |
г) пропанол-1. |
6.Какие виды изомерии возможны для предельных одноатомных спиртов:
а) цис-транс-изомерия; б) изомерия положения гидроксильной группы;
в) изомерия углеродного скелета; г) изомерия классу простых эфиров?
7.Сколько изомерных спиртов отвечает общей формуле С4Н9ОН:
|
а) 1; б) 2; в) 3; |
г) 4? |
|
|
|
8. |
Укажите изомеры: |
|
|
|
|
|
а) СН3СН2ОСН2СН3; |
|
|
|
|
|
б) СН3–СН2 – СН2 –СН2ОН; |
|
|
|
|
|
в) СН3–СН(ОН)–СН2СН3; |
|
|
|
|
|
г) СН3–ОСН2СН2СН3. |
|
|
|
|
9. |
Укажите ароматический спирт: |
|
|
|
|
|
а) С6Н5ОН; б) С2Н5ОН; |
г) С6H5СH2OH; в) |
CH2 – CH2 |
||
|
|
|
|
||
OH OH
56
10.Укажите способы промышленного получения этанола: а) гидратация ацетилена; б) гидратация этилена; в) брожение глюкозы.
г) гидролиз галогеналкилов водным раствором щелочи.
11.Какие реакции ведут к образованию этиленгликоля: а) окисление этилена раствором перманганата калия; б) гидратация ацетилена;
в) взаимодействие 1,2-дихлорэтана с водным раствором щелочи; г) дегидратация глицерина?
12.Метанол и этанол растворяются в воде благодаря: а) кислой природе; б) диссоциации воды;
в) полярной гидроксильной группе; г) присутствию алкильных групп.
13.Охарактеризуйте свойства глицерина: а) вязкая и бесцветная жидкость; б) хорошо растворим в воде; в) имеет сладковатый вкус;
г) неядовит и легко усваивается организмом.
14.Укажите соединение, которое имеет наибольшую растворимость
вводе:
а) этиленгликоль; |
в) бутанол-1; |
б) бутан; |
г) пентанол-1. |
15.Укажите вещества, с которыми реагирует глицерин: а) натрий; б) азотная кислота; в) медь;
г) свежеосажденный гидроксид меди.
16.Сколько простых эфиров образуется при нагревании смеси метанола, этанола и серной кислоты при температуре ниже 140 °С:
|
а) 1; |
б) 2; |
в) 3; |
г) 4? |
17. |
Укажите вещества, с которыми реагирует этанол при определен- |
|||
ных условиях: |
|
|
|
|
|
а) уксусная кислота; |
|
в) метанол; |
|
|
б) азотная кислота; |
|
г) гидроксид натрия. |
|
18. |
При взаимодействии с некоторыми веществами этанол образует: |
|||
|
а) сложные эфиры; |
|
в) ацетальдегид; |
|
|
б) этилен; |
|
|
г) простые эфиры. |
57
19. Укажите, какие вещества образуются при нагревании спиртов с
концентрированной серной кислотой: |
|
а) алкоголяты; |
в) простые эфиры; |
б) альдегиды; |
г) этиленовые углеводороды. |
20.Укажите области применения этанола: а) получение бутадиена-1,3; б) получение диэтилового эфира;
в) дезинфицирующее средство в медицине; г) растворитель.
21.Укажите области применения глицерина: а) производство взрывчатых веществ; б) приготовление мазей;
в) для получения синтетического волокна-лавсана; г) топливо.
22.Укажите формулы спиртов:
а) СН3–СН(ОН)СН3; |
в) С6Н5СН2ОН; |
б) СН3–С6Н4–ОН; |
г) НО–С6Н4–ОН. |
23.Охарактеризуйте свойства фенола:
а) бесцветное кристаллическое вещество; б) ядовитое вещество; в) вызывает ожоги кожи; г) антисептик.
24.Укажите вещества, с которыми реагирует фенол:
а) азотная кислота; |
в) бромная вода; |
б) бром; |
г) карбонат кальция. |
25. Укажите вещества, которые реагируют с гидроксидом натрия:
а) СН3ОН; б) С6Н5СН2ОН; в) С6Н5ОН; г) СН3–С6Н4–ОН.
26.Укажите реакции, в которых проявляются слабокислотные свойства фенола:
а) диссоциация в водных растворах; б) гидрирование; в) взаимодействие с натрием;
г) взаимодействие с гидроксидом натрия.
27.Бромная вода реагирует с фенолом с образованием:
а) бромбензола; |
в) 1,3-дибромфенола; |
б) 1,2-дибромфенола; |
г) 2,4,6-трибромфенола. |
28. 23 г металлического натрия реагирует с фенолом с образованием:
а) одного моль кислорода; |
в) половины моль водорода; |
б) одного моль водорода; |
г) двух моль водорода. |
58

29.Для качественного обнаружения фенола используют: а) раствор гидроксида аммония; б) бромную воду;
в) раствор хлорного железа (III); г) раствор йода.
30.Укажите области применения фенола: а) получение красителей и лекарств;
б) получение фенолформальдегидных пластмасс; в) получение уксусного альдегида; г) бактерицидное средство.
9. АЛЬДЕГИДЫ
Альдегиды — это органические вещества, молекулы которых содер-
жат функциональную группу атомов – C |
O |
соединенную с углево- |
|
||
|
H, |
|
дородным радикалом. Общая формула предельных (насыщенных) альде-
O
гидов CnH2n+1C .
H
Группа – C – называется карбонильной группой.
O
Вещества, содержащие карбонильную группу, связанную с двумя углеводородными радикалами, называются кетонами. Общая формула кето-
нов: |
R – C – R |
O
Радикалы могут быть одинаковыми и различными.
9.1. НОМЕНКЛАТУРА И ИЗОМЕРИЯ АЛЬДЕГИДОВ
Названия альдегидов образуются от названий соответствующих органических кислот, в которые они превращаются при окислении (муравьиный альдегид; уксусный альдегид и т. д.). По международной номенклатуре названия альдегидов образуются от названий соответствующих углеводородов при помощи суффикса -аль. Нумерацию начинают с альде-
3 |
2 |
1 |
O |
|
гидной группы. Например: CH |
CH2 |
C |
2-метилпропаналь |
|
3 |
|
|
|
H |
|
|
|
|
|
|
CH3 |
|
|
|
59