Материал: Ткачёв С.В. Введение в органическую химию
Этиленгликоль и глицерин — бесцветные сиропообразные жидкости, сладковатого вкуса, хорошо растворимые в воде. Этиленгликоль ядовит. Глицерин гигроскопичен, неядовит, легко усваивается организмом. Подобно одноатомным спиртам они реагируют с активными металлами, галогеноводородами, органическими и неорганическими кислотами.
|
CH2 – OH |
|
|
CH2 – ONa |
|||
|
|
+2Na |
|
|
|
+H2 |
|
|
|
||||||
|
|
|
|||||
|
CH2 – OH |
|
|
CH2 – ONa |
|||
|
CH2 – OH |
|
|
CH2Cl |
|||
|
|
+2HCl |
|
|
|
+2H2O |
|
|
|
|
|||||
|
CH2 – OH |
|
|
CH2Cl |
|||
CH2 – OH |
|
|
CH2 – ONO2 |
||||
|
|
|
|
||||
CH2 – OH +3HO–NO2 |
CH2 – ONO2 +3H2O |
||||||
|
|
|
|
|
|
|
|
CH2 – OH |
|
|
CH2 – ONO2 |
||||
Присутствие нескольких гидроксильных групп в молекулах многоатомных спиртов увеличивает подвижность и способность к замещению атомов водорода в гидроксильных группах. Например, если к свежеприготовленному гидроксиду меди (II) прилить глицерин, то образуется раствор ярко-синего цвета — глицерат меди. Это качественная реакция на многоатомные спирты. Одноатомные спирты с гидроксидом меди (II) не взаимодействуют.
|
|
|
|
|
|
H |
|
|
||||
H2C – O –H |
|
|
|
|
O – |
|
CH2 |
|
|
|||
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ HO–Cu –OH + H–O–CH |
|
|
||||||
C – O |
H |
|
|
|||||||||
|
|
|||||||||||
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2C – OH |
|
|
HO – CH2 |
|
|
|||||||
|
|
|
|
|
H |
|
|
|||||
|
H2C – O |
Cu |
|
O – |
|
CH2 |
|
|
||||
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
O– CH |
+ 2H2O |
||||||
|
HC – O |
|
||||||||||
|
|
|||||||||||
|
H |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO – CH2 |
|
|
|||||
|
H2C – OH |
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
||||
Глицерат меди — комплексное соединение (стрелкой показаны химические связи, которые образуются по донорно-акцепторному механизму).
Этиленгликоль применяется для получения лавсана — ценного синтетического волокна и используется для приготовления антифризов — низкозамерзающих жидкостей. В медицине глицерин используется для
50
смягчения кожи рук и приготовления мазей. Кроме того, глицерин применяется для получения синтетических смол и взрывчатых веществ, например, нитроглицерина.
ВОПРОСЫ И УПРАЖНЕНИЯ
1.Какие вещества называются спиртами? Напишите общую формулу гомологического ряда предельных одноатомных спиртов.
2.Составьте структурные формулы всех изомерных спиртов, отвечающих формуле С5Н11ОН. Назовите их.
3.Какие спирты называются: а) первичными; б) вторичными; в) третичными?
4.Как делятся спирты в зависимости от числа гидроксильных групп? Напишите формулы одно-, двух- и трехатомных спиртов.
5.Какие типы изомерии возможны для алканолов?
6.Составьте структурные формулы спиртов: а) 2-метилбутанола-1; б) 3,3 диметилпентанола-2.
7.Объясните, почему один из атомов водорода в молекулах одноатомных спиртов является более подвижным.
8.Как из пропана можно получить пропанол-1? Составьте уравнения соответствующих реакций.
9.Почему температура кипения у спиртов намного выше, чем у соответствующих углеводородов?
10.Напишите реакцию взаимодействия метилового спирта с хлороводородом.
11.При нагревании смеси этилового и пропилового спиртов с концентрированной серной кислотой образуется смешанный этилпропиловый эфир. Какие еще эфиры могут образоваться при этом? Напишите уравнения реакций.
12.Напишите уравнения реакций, с помощью которых пропанол-1 превращается в пропанол-2.
13.Как получают метиловый и этиловый спирты? Напишите уравнения реакций.
14.Где применяют метанол и этанол?
15.Каково физиологическое действие спиртов?
16.Что такое этиленгликоль и глицерин?
17.Как химическим способом отличить глицерин от этанола? Где применяют глицерин и этиленгликоль?
51
18. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
а) метан хлорметан метанол метанолят натрия; б) метан ацетилен этилен этанол бутадиен-1,3 бутан
бутен-1 бутанол-2; в) карбонат кальция карбид кальция ацетилен этанол
хлористый этил этилен этиленгликоль.
ЗАДАЧИ
1.Оксид углерода (IV), который образовался при брожении 100 г раствора глюкозы, пропустили через гидроксид кальция. Образовалось 10 г карбоната кальция. Вычислите массовую долю глюкозы в растворе. (Ответ: 9 %)
2.Сколько воздуха по объему необходимо для сжигания 1 л метанола
( =0,80 г/см3)? (Ответ: 4 м3)
3.Сколько литров раствора этанола с массовой долей его 96 % можно получить из 1000 м3 этилена (н.у.)? Плотность этанола 0,80 г/см3.
(Ответ: 2673,9 л)
4.Сколько граммов метанола сгорело, если при этом образовался СО2 объемом 56 л (н.у.)? (Ответ: 80 г)
5.Какой максимальный объем водорода (н.у.) может быть выделен натрием из глицерина, взятого в количестве 1 моль? (Ответ: 33,6 л.)
6.К 10,5 г этиленового углеводорода прилили 40 г брома. Какова формула спирта, из которого получили этиленовый углеводород? (Ответ:
С3Н7ОН)
7.Найти молекулярную формулу алканола, если при взаимодействии 13,8 г его с металлическим натрием выделился водород, которого достаточно для гидрирования 3,36 л пропилена. (Ответ: С2Н5ОН)
8.При дегидратации 18 г гомолога метанола образовался углеводород и 5,4 г воды. Установите молекулярную массу и формулу спирта.
(Ответ: 60 г/моль, С3Н8О)
9. К 16,6 г смеси этанола и пропанола добавили избыток металлического натрия. Выделилось 3,36 л водорода. Определить массовый состав исходной смеси. (Ответ: пропанол — 12 г; этанол — 4,6 г)
8. ФЕНОЛЫ
Фенолы — это производные ароматических углеводородов, в молекулах которых одна или несколько гидроксильных групп связаны с бензольным ядром.
– H |
– OH фенол (гидроксибензол) |
52
8.1. НОМЕНКЛАТУРА И ИЗОМЕРИЯ ФЕНОЛОВ
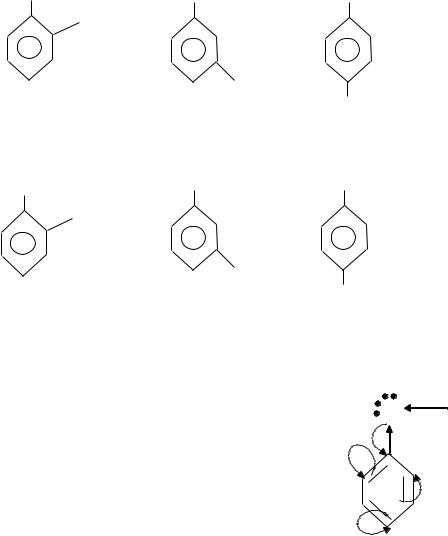
Известны одноатомные фенолы — С6Н5ОН — фенол, СН3С6Н4ОН — крезолы или гидрокситолуолы; двухатомные фенолы — С6Н4(ОН)2 — дигидроксибензолы; трехатомные фенолы — С6Н3(ОН)3 — тригидроксибензолы. Для фенолов возможна изомерия положения заместителей в бензольном кольце и изомерия боковой цепи. Например: о-крезол (1), м-крезол (2) n-крезол (3); двухатомные фенолы — 1,2 дигидроксибензол (4); 1,3 дигидроксибензол (5), 1,4 дигидроксибензол (6).
OH |
OH |
OH |
|
CH3 |
|
(1) |
(2) |
(3) |
|
|
CH3 |
|
|
CH3 |
OH |
OH |
OH |
|
|
|
|
OH |
|
(4) |
(5) |
(6) |
|
|
|
|
|
OH |
|
|
OH |
8.2.ЭЛЕКТРОННОЕ СТРОЕНИЕ ФЕНОЛА
ИЕГО ПОЛУЧЕНИЕ
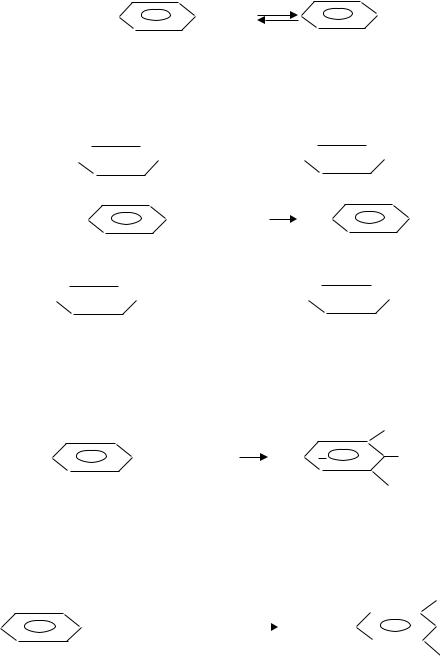
Электронное строение. Бензольное кольцо в фе- |
O |
H |
|
ноле обладает свойством притягивать к себе электроны |
|||
|
|
||
атома кислорода гидроксильной группы. Смещение не- |
1 |
|
|
поделенной пары электронов атома кислорода в сторону |
|
||
|
2 |
||
бензольного кольца увеличивает полярность связи |
6 |
||
|
|||
О – Н. Водородный атом становится более подвижным |
5 |
3 |
|
и реакционноспособным. Гидроксильная группа делает |
|
|
|
атомы водорода более подвижными в положениях 2, 4, 6 |
4 |
|
бензольного кольца. Таким образом, имеет место взаимное влияние атомов в молекуле фенола. Это взаимное влияние отражается на свойствах фенола.
Получение. Фенол выделяют из каменноугольной смолы при коксовании каменного угля. Разработаны и синтетические методы получения фенола.
53
8.3. ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА ФЕНОЛА
Физические свойства. Фенол — бесцветное, кристаллическое вещество с характерным запахом. При комнатной температуре плохо растворяется в воде, но при 70 °С растворяется в воде в любых соотношениях.
Химические свойства. Обусловлены присутствием в молекуле фенола гидроксильной группы и бензольного кольца.
1. Реакции с участием гидроксильной группы.
а) Фенол (1) в водных растворах диссоциирует и образует фенолятионы (2).
– OH |
– O– + H+ |
(1) |
(2) |
Поэтому фенол называют и карболовой кислотой.
б) Взаимодействие со щелочами с образованием фенолятов. Спирты со щелочами не реагируют.

 – OH + NaOH
– OH + NaOH 

 – ONa + H2O
– ONa + H2O
в) Взаимодействие с активными металлами с образованием фенолятов.
2 |
– OH + 2Na |
2 |
– ONa + H2 |
Феноляты легко разлагаются при действии кислот. Фенол — более слабая кислота, чем угольная.

 –ONa+H2O+CO2
–ONa+H2O+CO2 
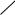

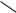 OH + NaHCO3
OH + NaHCO3
2. Реакции с участием бензольного кольца.
Реакции замещения в бензольном кольце фенола идут легче, чем у бензола, и в более мягких условиях.
а) Взаимодействие с бромной водой:
Br
– OH +3Br2 |
Br |
OH + 3HBr |
Br
2,4,6-трибромфенол плохо растворим в воде и выпадает в осадок, поэтому реакция его образования может служить для обнаружения фенола.
б) Нитрование. Образуется пикриновая кислота.
|
|
|
|
|
|
|
NO2 |
|
– OH +3HO–NO2 |
H2SO4 |
O2N– |
|
|
|
|
|
OH + 3H2O |
|
|
|
|
|
||||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
NO2 |
|
54