Материал: Сыровая А.О. и др Аминокислоты глазами химиков, фармацевтов, биологов. Т. 2
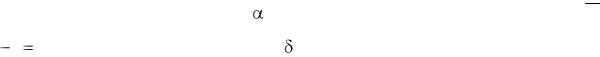
третбутиламиновой соли. Однако при усовершенствовании этого продукта было показано, что аргининовая соль периндоприла наряду с высокой биодоступностью имеет более высокую стабильность сравнительно с третбутиламиновой солью периндоприла.
Можно также отметить, что антитромботический препарат на основе тенектеплазы (рекомбинантный фибринспецифический активатор плазминогена в форме порошка для приготовления раствора для инъекций) в качестве вспомогательного вещества также содержит аргинин [20]. В патентной документации утверждается, что предпочтительно использование в технологии получения данного препарата аргинин.
Таким образом, можно констатировать о значимой области применения аргинина в качестве вспомогательного вещества готовых лекарственных форм и возможности использования указанной; аминокислоты с целью повышения стабильности препаратов.
Клиническое значение L-аргинина, несмотря на его длительное применение в медицинской практике, не уменьшается, а, напротив, возрастает, а круг показаний к его использованию расширяется. L-аргинин также используется в качестве безопасного вспомогательного вещества в составе готовых лекарственных форм.
Обмен аргинина. Характерной химической особенностью аргинина является наличие в его молекуле наряду с -аминогруппой, еще и амидиновой группы
(NH2 C NH), расположенной у -аминогруппы. Амидиновой группе принадлежит важная роль в обмене азотистых веществ в организме человека и животных. Амидная группа аргинина подвижна и с помощью амидинфераз переносится на другие вещества. Она отщепляется также путем гидролиза с образованием молекулы мочевины. Участвующий в этой реакции фермент известен под названием аргиназы. При перенесении амидиновой группы на глицин появляется гуанидинуксусная кислота – предшественник креатина. При
156
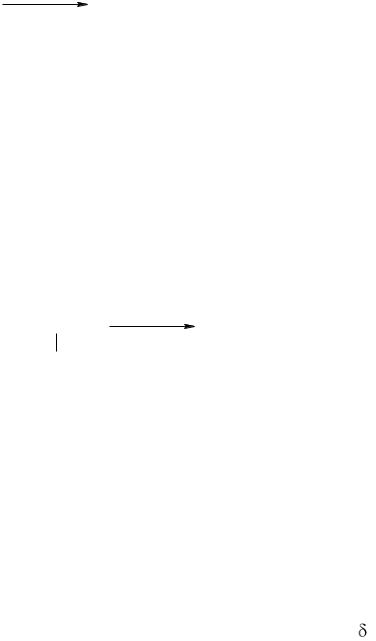
перенесении амидиновой группы, а также при гидролитическом еѐ отщеплении
аргинин превращается в орнитин (рис. 6).
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
C |
|
|
|
|
NH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH |
+ |
H2O |
|
|
|
CH2 |
|
|
|
|
|
|
NH2 |
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
+ |
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
CH2 |
|
|
|
|
|
|
O |
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
C |
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
CH |
|
|
|
|
|
|
|
|
|
NH |
|
|
|
|
|
||||||||||||||||||||
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Мочевина |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HC |
|
NH2 |
||||||||||||||||||
CH |
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
||||||||||
HC |
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Орнитин |
|
|
|
|
|
|
|
|
|
|
|||||||||||
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
Аргинин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
C |
|
|
|
|
|
NH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH |
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
||
NH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
NH |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
CH2 |
+ |
|
CH2 |
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
NH |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|||
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
Глицин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HC |
|
NH2 |
|
|
|
|
|
|
|
|
|
|
||||
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Гуанидинуксуная |
||||||||||
HC |
|
|
NH2 |
|
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Орнитин |
|
|
|
|
|
кислота |
||||||||
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
Аргинин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
Рис. 6. Образование мочевины, орнитина и гуанидинуксусной кислоты из аргинина.
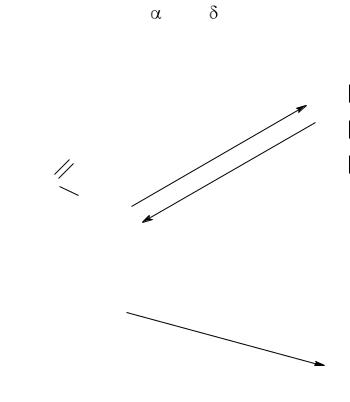
Орнитин, в результате переаминирования |
-аминогруппы, дает |
полуальдегид глутаминовой кислоты, который окисляется с образованием
глутаминовой кислоты (рис. 7).
157
Орнитин, наряду с этим, может явиться источником образования пролина.
Перенесение амидиновой группы от аргинина – процесс необратимый, тем не менее из орнитина в организме образуется аргинин. Происходит это в результате превращения его в цитруллин, а затем цитруллина в аргинин. Превращение аргинина может начаться с процесса его окислительного дезаминирования. В этом случае из аргинина получается -кето- -гуанидинвалерьяновая кислота.
NH2
ам инирование CH2
O CH2
C |
|
|
|
|
|
|
CH |
|
|
||||||||
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
HC |
|
|
NH2 |
||||||||||
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
CH2 |
|
COOH |
|||||||||||||
|
|
Орнитин |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||
HC |
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
COOH |
|
COOH |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||
Полуальдегид |
Окисление |
|
|
|
|
|
|
|
|
|
|||||||
глутаминовой |
|
|
|
CH2 |
|
|
|||||||||||
|
|
|
|
|
|||||||||||||
|
|
|
|
||||||||||||||
кислоты |
|
|
|
|
|
CH2 |
|
|
|||||||||
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
HC |
|
NH2 |
||||||
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
COOH |
||||||||
Глутаминовая
кислота
Рис. 7. Образование глутаминовой кислоты.
У млекопитающих животных аргинин предварительно гидролизуется с образованием орнитина, который затем уже подвергается дальнейшим превращениям.
158
Продуктами превращения орнитина могут быть пролин и глутаминовая кислота.
Синтез аргинина у животных, хотя и возможен, но он ограничен. Это подтверждается следующим примером. При кормлении молодых животных пищей, в белках которых отсутствует какая-либо незаминимая аминокислота, они теряют в весе и погибают. Если же кормить молодых животных пищей, не содержащей аргинина, наблюдается замедление роста, но животные не погибают. Эти данные показывают, что у животных аргинин синтезируется, но размеры этого синтеза недостаточны для того, чтобы обеспечить интенсивный синтез белков (при наличии других аминокислот), имеющий место во время роста молодого организма.
Благодаря синтезу орнитина из пролина аргинин, в известной мере заменим. Чем интенсивнее синтез орнитина, тем меньше организм зависит от поступления аргинина с белками пищи [2].
ЛИТЕРАТУРА
1. Бабушкина А. В. L-аргинин с точки зрения доказательной медицины / А. В.
Бабушкина // Український медичний часопис. – 2009. – № 6(74). – |
С. 43–48. |
2. Фердман Д. Л. Биохимия / Д. Л. Фердман. – М. : Высшая школа. – |
1962. – 615 |
с.
3. Bryan N. S. Discovery of the nitric oxide signaling pathway and targets for drug development / N. S. Bryan, K. Bian, F. Murad // Frontiers in Bioscience. – 2009. – №
14. Р. 1–18.
4. Алмакаева Л. Г. Аргинин и его применение в медицине и фармации / Л. Г. Алмакаева, Е. В. Литвинова // Ліки України. – 2011. – № 1(5). – С. 23–26.
5. Аминокислоты и их производные в биологии и медицине: Материалы II междунар. науч. конф., 10-12 окт. 2001 г., Гродно. / Под общ. ред. Л. И. Нефѐдова.
– Гродно : ГрГУ, 2001. – 124 с.
159
6. Аргинин в медицинской практике (Обзор литературы) / Степанов Ю. М., Кононов И. Н., Журбина А. И., Филиппова А. Ю. // Сучас. гастроентерологія. –
2005. – №4. – С. 121–127.
7. Воger R. Н. and Воdе-Воgеr S. М. Тhе сclinical pharmacology оf L-Arginine // Аnn.
Реv. Рharmaсоl. Тохicol. – 2001. – V. 41 – Р. 79–99.
8. Граник В. Г. Метаболизм L-аргинина. // Хим-фарм. журн. – 2003. –№ 3. – С. 3– 20.
9. Bode-Boger S. M. Effect of L-arginine supplementation on NO production in man // European Journal of Clinical Pharmacology. – 2006. – V. 62, Supplement 13. – P. 91– 99.
10. Wu G., Meininger C. J. Arginine nutrition and cardiovascular function. //J. Nutr. – 2000. – V. 130. – P. 2626–2629.
11.Rector T. S., Bank A. J., Mullen K. A., Tschumperlin L. K. Randomized, doubleblind, placebo-controlled study of supplemental oral L-arginine in patients with heart failure. // Circulation. – 1997. – V. 18. – P. 1674–1679.
12.Kelly B. S., et al. Oral arginine improves blood pressure in renal transplant and hemodialysis patients. //J. Parenter. Enteral. Nutr. – 2001. – V. 25. – P. 194–202.
13.Neri I., et al. Effects of acute L-arginine infusion on non-stress test in hypertensive pregnant women. // J. Matern. Fetal. Neonatal. Med. – 2004. – V. 16. – P. 23–28.
14.Palloshi A., et al. Effect of oral L-arginine on blood pressure and symptoms and endothelial function in orations with systemic hypertension, positive exercise tests, and normal coronary arteries. // Am. J. Cardiol. – 2004. – V. 93. – P. 933–938.
15.Campisi R., Czernin J., Schoder H., et al. L-Arginine normalizes coronary vasomotion in long-term smokers // Circulation. – 1999. – V. 99. – P. 491–497.
16.Hutchison J., Sudhir K., Sievers R. E., et al. Effects of L-arginine on atherogenesis and endothelial dysfunction due to secondhand smoke // Hypertension. – 1999. – V. 34.
– P. 44–50.
160