Материал: Сыровая А.О. и др Аминокислоты глазами химиков, фармацевтов, биологов. Т. 2

нарушение азотистого равновесия, истощение мышц и нарушение кальцификации костей, а также ряд изменений в печени и легких. Лизин участвует в утилизации жирных кислот, необходимых для производства энергии. Помогает устранять некоторые проблемы связанные с бесплодием. Лизин катализирует процессы ферментативных превращений. В процессах ферментации е-аминогруппа радикала лизина осуществляет прикрепление субстрата, подвергающегося ферментативному превращению, к ферменту. Так, например, соединение биотина с белком осуществляется через -аминогруппу радикала лизина белковой молекулы и карбоксильную группу боковой цепи молекулы биотина. Лизин входит в состав нуклеотидпептидов, являющихся промежуточным продуктом в синтезе белка. Реже лизин встречается в липопептидах – метаболитах в биосинтезе белков. В качестве диаминокислоты входит в состав белков рибосом и глюкагона-пептида – гормона, синтезирующегося в -клетках островковой части поджелудочной железы. Принимает участие в обмене белков и углеводов. L-
форма лизина снижает содержание триглицеридов в сыворотке крови. Участвует в синтезе аналогичного никотину алкалоида – анабазина. Способствует абсорбции кальция и поддерживает баланс азота во взрослом организме, участвует в производстве антител, гормонов и ферментов, способствует образованию коллагена и восстановлению тканей. Дефицит лизина вызывает у людей головную боль, головокружение, повышенную чувствительность к шуму, понижение аппетита, тошноту, рвоту, ферментные нарушения, анемию, лейкемию,
истощение, нарушение репродуктивной функции. Он способствует улучшению сосредоточения. Недостаточность лизина может проявляться в покраснении глаз,
выпадении волос, неспособности к концентрации, раздражительности, недостатке энергии, замедлении роста. Вводят в пищу детей для повышения аппетита, при лечении тяжелых отравлений. Он снижает повышенный уровень триглицеридов в сыворотке крови, усиливает иммунитет к вирусным инфекциям. Следует отметить
166
способность лизина уменьшать вероятность и/или предупреждать герпесную инфекцию.
Высоким содержанием лизина отличаются все молочные продукты, однако наибольшую ценность по содержанию лизина представляют творог и обрат,
получаемый в результате сепарирования молока. Важным источником лизина являются сычужные сыры. При свертывании молока сычужным ферментом образующийся сгусток в большей степени обогащен лизином, чем сгусток,
образующийся в результате молочнокислого брожения. Особенностью содержания лизина в мясе является то, что он содержится и в соединительнотканных белках (4% от веса белка). Наиболее богат лизином белок мышечной ткани – миозин и белок крови – гемоглобин. В них лизина в 2,5 раза больше, чем в соединительнотканном белке коллагене. Яйца в качестве источника лизина представляют меньшую ценность по сравнению с мясом и творогом. Они содержат наполовину меньше лизина (0,8 г на 100 г, тогда как в мясе 1,5 г лизина на 100 г). В частях яйца лизин распределен неравномерно. В наибольшем количестве лизин представлен в яичном белке, в котором лизина в 2 раза больше,
чем в белке желтка. Таким образом, с точки зрения содержания лизина белок является более ценным, чем желток. Недостаточность лизина в хлебных злаках является основным фактором, снижающим ценность белков этих продуктов. Недостаток лизина в белках зерновых культур сказывается на общем аминокислотном балансе всего пищевого рациона. С удалением зародыша и наружных оболочек продукт (мука сортовая, манная крупа и др.) еще в большей степени обедняется лизином. Резко выделяются высоким содержанием лизина бобовые культуры – соя, горох, фасоль. Это продукты,
как бы самой природой предназначенные для компенсации недостающего лизина в хлебных злаках. В соевой муке количество лизина более чем в 10
раз превышает его содержание в пшеничной муке, в гороховой муке – в 5
167
раз [1, 3]. Лучшие натуральные источники: рыба, молоко, бобы, мясо, сыр,
дрожжи, яйца, соевые продукты, все богатые белком продукты. Содержится в авокадо, арахисе, рыбе, креветках, пивных дрожжах, сыре, яйцах,
помидорах, картофеле, красном вине.
L-лизин входит в состав многих биологически активных добавок. В
случае повышенной усталости, несконцентрированности, если глаза склонны наливаться кровью, присутствует тошнота, головокружения,
выпадения волос, и анемии, в этом случае у человека может быть дефицит лизина. С возрастом людям, особенно мужчинам, требуется больше лизина,
чем в молодости. Лизина не достает в некоторых зерновых белках, таких как глиадин (в пшенице) и зеин (в кукурузе). Добавки лизина в хлебные продукты улучшают качество их белков. При герпесе определенно показаны лизиновые добавки по 3-6 грамм ежедневно плюс пища, богатая лизином
[1].
Катаболизм лизина. Лизин составляет исключение из общего правила,
согласно которому первой стадией катаболизма аминокислоты является удаление альфа-аминогруппы путем переаминирования. В тканях млекопитающих ни альфа-, ни эпселон-аминогруппы L-лизина не участвуют в переаминировании. В
организме млекопитающих углеродный скелет L-лизина переходит в состав альфа-аминоадипат а и альфа-кетоадипат а (катаболизм аминокислот,
образующих ацетил-КоА: метаболическая карта). Первоначально полагали, что деградация L-лизина идет через стадию образования пипеколиновой кислоты – циклической иминокислоты. В печени L-лизин действительно превращается в пипеколат, однако распад L-лизина происходит через стадию образования сахаропина − интермедиата биосинтеза лизина у грибов. L-лизин сначала конденсируется с альфа-кетоглутаратом, при этом отщепляется молекула воды и образуется шиффово основание Далее происходит восстановление этого
168
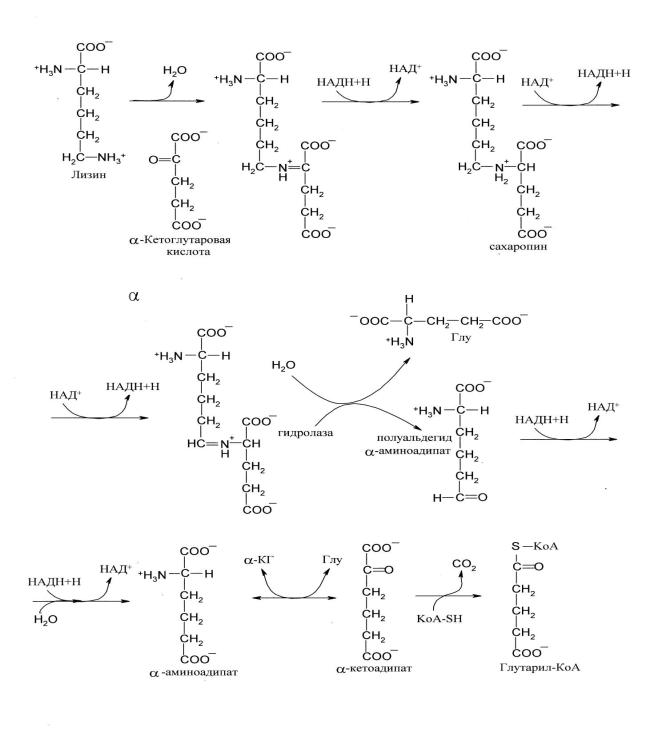
соединения в сахаропин при участии соответствующей дегидрогеназы, а затем окисление сахаропина другой дегидрогеназой. Расщепление продукта водой приводит к образованию L-глутамата и L-альфа-аминоадипат-дельта-
полуальдегида (рис. 2).
-кетоглутарат
Рис. 2. Катаболизм лизина
169
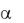
Суммарный эффект этой серии реакций эквивалентен удалениюэпселон-
аминогруппы лизина путем переаминирования; L-лизини альфа-кетоглутарат превращаются в альфа-аминоадипат-дельта-полуальдегид и глутамат. В качестве кофакторов впроцессе участвуют НАД и НАДН, при этом в итоге не происходит ни окисления, ни восстановления.
В ходе дальнейшего катаболизма альфа-аминоадипат путем переаминирования превращается в альфа-кетоадипат, после чего, вероятно,
происходит окислительное декарбоксилирование альфа-кетоадипата с образованием глутарил-КоА. Лизин является одновременно и гликогенной, и
кетогенной аминокислотой; природа же катаболитов глутарил-КоА,
образующихся в организме млекопитающих, не установлена.
Описаны два редких метаболических нарушения катаболизма лизина. Оба они являются следствием дефектности ферментов, осуществляющих катаболизм лизина до ацетоацетил-КоА, и в обоих случаях первичное нарушение, вероятно,
блокирует превращение L-лизина и альфа-кетоглутарата в сахаропин [4].
Физические и химические свойства лизина. L-лизин (Lys) является представителем диаминомонокарбоновых кислот. Его молекулярная масса равняется 146,19 а. е. м.
L-лизин кристаллизуется в виде бесцветных игл или гексагональных пластинок и плавится с разложением при температуре 224 – 225° С. Хорошо растворим в воде, в кислотах и основаниях, трудно растворим в спирте и нерастворим в эфире.
В молекуле лизина -атом углерода асимметричен, то есть все четыре группы, с которыми он связан, различны. Поэтому молекула лизина может существовать в форме двух конфигураций, зеркально противоположно ориентированных в пространстве, вследствие чего она обладает оптической активностью, выражающейся в способности вращать плоскость поляризованного света. Изомер, вращающий плоскость поляризованного света вправо, называется
170