Материал: Шмид Р. Наглядная биотехнология и генетическая инженерия
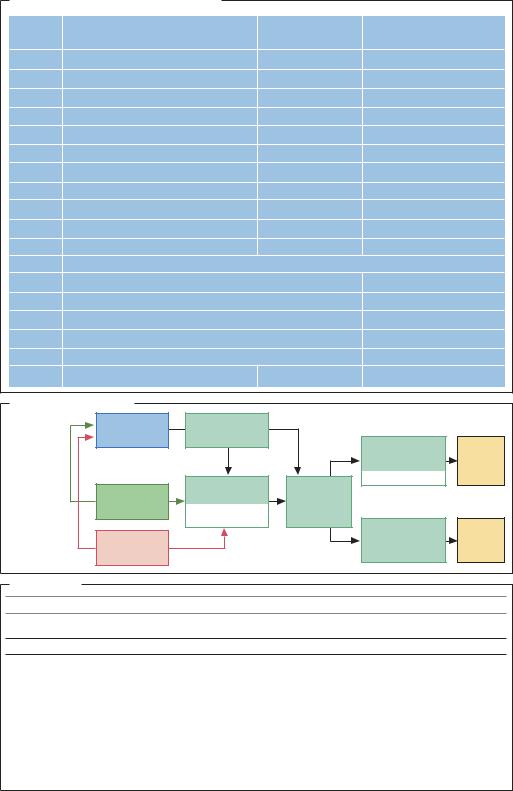
Классификация ферментов и примеры
ЕС-номер |
Название, функция |
Кофактор |
Примеры |
|
|
|
|
1.x.y.z |
Оксидоредуктазы |
|
|
1.1.y.z |
Действуют на СН–ОН-группу |
NAD+, NADP+, PQQ |
Алкогольдегидрогеназа |
1.1.3.z |
Действуют на СН–ОН-группу |
FAD+ |
Глюкозооксидаза |
1.3.y.z |
Действуют на С–Н-группу |
Гем, Fe2+ |
Стероид-11β-гидроксилаза |
2.x.y.z |
Трансферазы |
|
|
2.4.y.z |
Переносят гликозильные группы |
|
Гликозилтрансфераза |
2.6.1.z |
Переносят NH2-группы на С=О |
Пиридоксальфосфат |
Трансаминаза |
3.x.y.z |
Гидролазы |
|
|
3.1.y.z |
Гидролизуют эфирные связи |
|
Липазы, эстеразы |
3.2.y.z |
Гидролизуют гликозидные связи |
|
α-Амилаза |
3.4.y.z |
Гидролизуют пептидные связи |
|
Субтилизин, трипсин |
4.x.y.z |
Лиазы |
|
|
|
Катализируют реакции присоединения по двойным связям |
|
|
4.x.y.z |
Добавление (удаление) NH2-группы к (от) двойной связи |
Аспартаза |
|
5.x.y.z |
Изомеразы |
|
|
5.1.y.z |
Рацемизация D- и L-аминокислот |
|
Аланинрацемаза |
5.3.y.z |
Внутримолекулярные оксидоредуктазы |
|
Ксилозо(глюкозо)-изомераза |
6.x.y.z |
Лигазы |
|
|
6.2.y.z |
Образование C–S связей |
|
ATФ, КоА-SH |
Ацетил-КоА-синтетаза |
||
Получение ферментов |
|
|
|
|
||
|
|
Микро- |
Ферментация |
|
|
|
|
|
организмы |
|
|
|
|
|
|
|
|
Высушивание |
Техни- |
|
|
|
|
|
|
||
|
|
|
|
|
в псевдо- |
ческие |
|
|
|
|
|
ожиженном слое |
фер- |
|
|
|
Выделение |
|
гранулирование |
менты |
|
|
|
|
|
|
|
Клонирование |
|
Растительный |
из клеток |
Концент- |
|
|
и экспрессия |
|
материал |
отделение |
рирование |
|
|
|
|
|
твердых частиц |
|
|
Аналити- |
|
|
|
|
|
|
|
|
|
Животный |
|
|
Тонкая очистка |
ческие |
|
|
|
|
фер- |
||
|
|
материал |
|
|
|
менты |
Применение |
|
|
|
|
|
|
Источник |
|
Примеры |
|
|
Применение |
|
Животные ткани |
Панкреатические ферменты, |
|
в соответствии с GMP* |
|
||
|
|
сычужный фермент, пепсин |
|
|
|
|
Растительные ткани |
Папаин, бромелаин |
|
в соответствии с GMP* |
|
||
Микроорганизмы: |
|
|
|
|
|
|
а) традиционно исполь- |
Bacillus subtilis, Aspergillus niger и A. oryzae, |
GRAS (generally recognized as safe) – |
|
зуемые для получения |
Mucor javanicus, Rhizopus sp., Saccharomyces |
признаны безопасными в соответствии |
|
продуктов питания |
cerevisiae, Kluyveromyces fragilis и K. lactis, |
с положениями AMFEP (Международная |
|
|
Leuconostoc oenus |
ассоциация производителей ферментов |
|
|
|
для пищевой промышленности) |
|
б) ферменты |
Bacillus stearothermophilus, B. licheniformis, |
Специальная процедура |
|
хорошо изученных |
B. coagulans, B. megaterium и B. circulans, |
согласования |
|
микроорганизмов |
Klebsiella aerogenes |
|
|
* GMP (good manufacturing practice) – «Правила организации производства и контроля качества лекарственных средств», |
|||
принятые Всемирной организацией здравоохранения. — Прим. перев. |
75 |
||
|
|
||
Ферменты |
Ферментативный катализ |
в реакциях химического синтеза связаны с |
|
|
ВВЕДЕНИЕ. Преимущества использования ферментов |
|
в их высокой субстратной специфичностью. В про- |
|
мышленности, как правило, применяют ферменты, |
|
которые не требуют дополнительных кофакторов: |
|
гидролазы, лиазы, изомеразы и некоторые оксидоре- |
|
дуктазы. К настоящему времени гены многих фер- |
|
ментов клонированы, поэтому появилась возмож- |
|
ность получать эти ферменты без побочных |
|
активностей и с некоторыми улучшенными в резуль- |
|
тате генно-инженерных манипуляций свойствами. |
|
ОКСИДОРЕДУКТАЗЫ. На сегодняшний день охаракте- |
|
ризованно около 850 оксидоредуктаз. Эти ферменты |
|
катализируют окислительно-восстановительные ре- |
|
акции в присутствии кофермента. В случае оксидаз |
|
коферментом является молекула ФАД, ковалентно |
|
связанная с ферментом. Оксидоредуктазы широко |
|
применяются в аналитических методах. Дегидрогена- |
|
зы используются для аналитических, а также препа- |
|
ративных целей в качестве восстановителей карбок- |
|
сильных или окислителей гидроксильных групп. |
|
Процедура очистки кофакторов, например NAD(P)+ |
|
или NAD(P)H, требует значительных затрат, поэтому |
|
использование этих веществ в очищенном виде явля- |
|
ется экономически невыгодным. Часто в технологи- |
|
ческий процесс включают дополнительную реакцию с |
|
недорогими субстратами, в результате которой обра- |
|
зуются необходимые кофакторы. Значительными |
|
преимуществами обладает мембранный фермента- |
|
тивный реактор, в котором для синтеза кофактора |
|
используется производное NAD(P)H и формиатде- |
|
гидрогеназа. В последнее время ведутся активные |
|
исследования возможностей применения перокси- |
|
даз, диоксигеназ и Р450-монооксигеназ, катализи- |
|
рующих определенные реакции гидроксилирования. |
|
Эти ферменты содержат железо-серный кластер или |
|
гемовую группу, играющие роль кофактора. |
|
ТРАНСФЕРАЗЫ. К настоящему времени известно |
|
около 950 ферментов, относящихся к классу транс- |
|
фераз. В промышленности эти ферменты не находят |
|
применения. |
|
ГИДРОЛАЗЫ. К классу гидролаз относится более |
|
1000 ферментов, в том числе протеазы, липазы и |
|
эстеразы, имеющие большое значение в современ- |
|
ной биотехнологии. По сути эти ферменты можно |
|
рассматривать как трансферазы, переносящие ту или |
|
иную группу на молекулу воды. Гидролазы катализи- |
|
руют гидролиз связей С–О, C–N, C–C и др. и могут |
|
применяться для синтеза или гидролиза сложных |
|
эфиров и амидов. Так, термолизин, выделенный из |
|
Bacillus stearothermophilus, используют для синтеза |
|
аспартама из L-аспарагиновой кислоты и L-фенил- |
76 |
аланина, пенициллинамидазу из клеток E. coli – для |
гидролиза пенициллина G до 6-аминопенициллано- |
вой кислоты. Липаза из Pseudomonas cepacia служит для промышленного производства аминов из пред- шественников-амидов, липаза из Serratia marcescens используется для энантиоселективного гидролиза оксирана – предшественника дилтиазема, применяемого для снижения кровяного давления. С помощью липазы из клеток Rhizomucor miehei производят синтетическое масло какао, а ацилазу аминокислот из Aspergillus oryzae применяют для энантиоселективного гидролиза N-ациламинокислот.
ЛИАЗЫ. К лиазам относятся ферменты, которые разрывают связи С–С, С–О, С–N и др., при этом не требуется наличия кофакторов. К настоящему времени описано более 300 лиаз. Аспартазу из E. coli используют для промышленного производства L-аспа- рагиновой кислоты из фумаровой. Процедура очистки фермента требует дополнительных затрат, поэтому в промышленности используют целые клетки E. coli, а не выделенный фермент. Акрилонитрилгидратаза из Pseudomonas chloraphis катализирует присоединение молекулы воды к акрилонитрилу. В результате этой реакции образуется акриламид – важнейший продукт для получения полимера полиакриламида. Оксинитрилазы обеспечивают стереоселективное присоединение HCN к альдегиду; при гидролизе нитрила образуются D- или L-аминокисло- ты. Альдолазы, выделенные, к примеру, из печени кролика, используются при стереоселективном синтезе гексоз из С3-компонентов.
ИЗОМЕРАЗЫ. Известно около 140 ферментов, относящихся к классу изомераз. Ферментам этого типа не требуется кофактор. Изомеризация D-глюкозы и D-фруктозы, катализируемая глюкозоизомеразой, является важнейшим процессом в производстве искусственных подсластителей. Этот фермент внутриклеточный, и для этой реакции, как правило, используют дезактивированные иммобилизованные клетки
Streptomyces.
ЛИГАЗЫ. К классу лигаз, их известно 117, относятся ферменты, катализирующие соединение двух молекул, сопряженное с гидролизом АТФ. Теоретически использование лигаз в технологическом процессе весьма перспективно, однако необходимо найти дешевые пути синтеза кофактора – АТФ. Такие системы разрабатываются в лабораторных условиях, но пока не находят применения в технологических процессах.
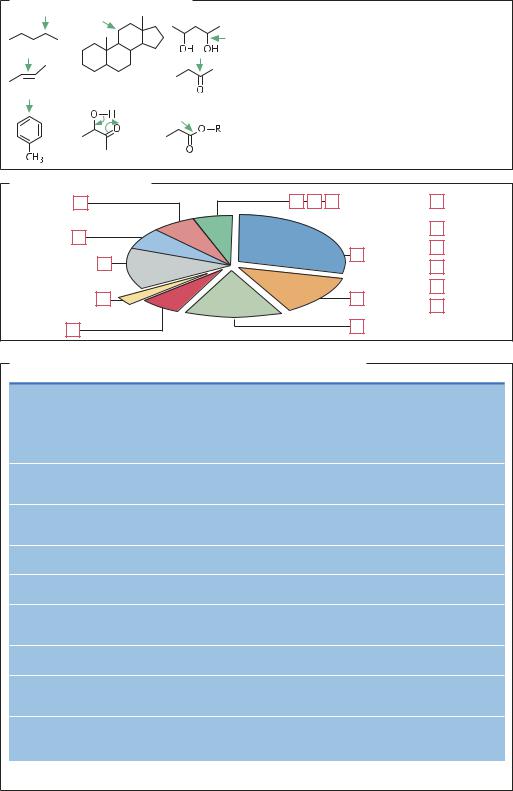
Ферменты в химическом синтезе |
|
|
|
|
|
|
|
|
|||
|
|
1 |
4 |
Преимущества ферментов в реакциях химического синтеза |
|||||||
|
|
1 |
Стерео- и субстрат-специфичное окисление |
||||||||
|
|
|
|
||||||||
|
|
|
|
2 |
неактивированных С–Н групп |
|
|
||||
|
|
|
|
Стереоселективные реакции присоединения |
|||||||
2 |
|
|
|
3 |
по активированным двойным связям |
|
|
||||
|
|
|
3 |
Стереоселективное восстановление |
|
|
|||||
|
|
|
4 |
карбонильных групп |
|
|
|
||||
5 |
|
6 |
7 |
Стереоселективное восстановление |
|
|
|||||
|
5 |
гидроксильных групп |
|
|
|
||||||
|
|
|
|
Субстрат-специфичное замещение |
|
|
|||||
|
|
|
|
6 |
в ароматических соединениях |
|
|
||||
|
|
|
|
Субстрат-специфичная изомеризация |
|
|
|||||
|
|
|
|
7 Субстрат-специфичные и стереоселективные реакции |
|||||||
|
|
|
|
|
гидролиза и этерификации |
|
|
||||
Ферменты в биокатализе |
|
|
|
|
|
|
|
|
|||
Пероксидазы |
1 |
|
|
2 |
4 |
5 |
Лиазы, |
1 |
Оксидо- |
||
и оксигеназы |
|
|
редуктазы |
||||||||
|
|
|
|
|
трансферазы, |
||||||
В том числе: |
|
|
|
|
|
|
|
изомеразы |
2 |
Трансферазы |
|
Oчищенные |
|
1 |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||
ферменты |
|
|
|
|
|
|
|
|
3 |
Гидролазы |
|
|
|
|
|
|
|
|
3 |
Липазы |
|||
|
|
|
|
|
|
|
|
||||
Оксидоредуктазы |
1 |
|
|
|
|
|
|
||||
|
|
|
|
|
|
4 |
Лиазы |
||||
(целые клетки) |
|
|
|
|
|
|
|
5 |
Изомеразы |
||
Другие гидролазы |
|
|
|
|
|
|
Эстеразы |
||||
3 |
|
|
|
|
3 |
6 |
Лигазы |
||||
|
|
|
|
|
|
|
|
|
|
||
Нитрилазы |
3 |
|
|
|
|
|
3 |
Протеазы |
|
|
|
Примеры использования ферментов в технологических процессах
|
|
Реакция |
Фермент |
Ежегодное |
Фирма- |
|
|
|
|
потребление, т |
производитель |
|
|
|
|
|
|
|
|
Расщепление пенициллина G |
Пенициллинамидаза* |
40 000 |
North China |
|
3 |
||||
|
|
с образованием |
из E. coli |
|
Pharmaceuticals |
|
|
6-аминопенициллановой кислоты |
|
|
|
|
Расщепление рацемата N-ацил- |
Ацилаза* |
5 000 |
Tanabe Sejyaku, |
|
|
3 |
||||
|
|
DL-аминокислот с образованием |
из Aspergillus sp. |
|
Degussa, DSM |
|
|
|
|||
|
|
L-аминокислот |
|
|
|
|
|
Обработка NH3 |
Аспартаза* из E.coli |
10 000 |
Tanabe Sejyaku |
|
4 |
||||
|
|
фумаровой кислоты с образованием |
|
|
|
|
|
|
|
|
|
|
|
L-аспарагиновой кислоты |
|
|
|
|
|
Гидролиз крахмала до D-мальтозы |
α-Амилаза, |
100 000 |
Различные фирмы |
|
3 |
||||
|
и D-глюкозы |
глюкоамилаза |
|
|
|
|
|
|
|
||
|
Изомеризация D-глюкозы в D-фруктозу Глюкозоизомераза* |
100 000 |
Clinton Corn |
||
|
5 |
||||
|
|
|
из Streptomyces sp. |
|
Products |
|
Синтез акриламида из акрилонитрила |
Нитрилгидратаза* |
30 000 |
Nitto Chemicals |
|
|
3 |
||||
|
|
|
из Pseudomonas |
|
|
|
|
|
|
|
|
|
|
|
chloraphis |
|
|
|
|
Расщепление рацемата |
Липаза* из |
10 000 |
BASF |
|
3 |
||||
|
|
фенилэтиламинов |
Pseudomonas cepacia |
|
|
|
|
|
|
||
|
|
Трансэтерификация пальмового масла |
Липаза* из |
1000 |
Unilever |
|
3 |
||||
|
и метилового эфира стеариновой |
Rhizomucor miehei |
|
|
|
|
|
|
|
||
|
|
кислоты с образованием масла какао |
|
|
|
|
|
Дегалогенирование |
Дегалогеназа* из |
Технология |
Dow Chemicals |
|
3 |
||||
|
1-хлорпропандиола |
термофильных |
разрабатывается |
|
|
|
|
|
|||
организмов
* Иммобилизованный фермент.
77
Ферменты |
Ферменты в клинических анализах |
||
роль играют лабораторные анализы, где широко при- |
этом анализируют не конечные продукты реакции, а |
||
|
ВВЕДЕНИЕ. При клинической диагностике важную |
метод определения глюкозы – кинетический. При |
|
|
меняются ферменты различных классов. При этом |
измеряют начальную скорость реакции (метод на- |
|
|
используется свойство фермента специфически ка- |
чальных скоростей). Когда концентрация субстрата |
|
|
тализировать реакцию, в которой участвует лишь |
значительно ниже Km (менее 1/10), скорость реак- |
|
|
один компонент сложной среды. Чтобы получить пра- |
ции линейно зависит от концентрации субстрата. При |
|
|
вильный результат анализа, в ферментном препара- |
таком методе анализа особенно важно соблюдать по- |
|
|
те должны отсутствовать другие активности; поэтому |
стоянные условия реакции, поэтому этот метод ле- |
|
|
к степени очистки ферментов, применяемых при про- |
жит в основе действия автоматических анализато- |
|
|
ведении |
клинических анализов, предъявляются |
ров. Каталитический метод анализа основан на том, |
|
очень жесткие требования. Анализы большого числа |
что количество анализируемого вещества является |
|
|
проб проводят с помощью лабораторных автомати- |
лимитирующим фактором в циклическом каталити- |
|
|
ческих анализаторов, тест-полосок или биосенсоров. |
ческом процессе, в котором оно разлагается в ходе |
|
|
Ферменты также применяются в качестве репортер- |
одной ферментативной реакции и образуется в ходе |
|
|
ных соединений (маркеров) в реакциях специфиче- |
другой. Количество анализируемого вещества опреде- |
|
|
ского связывания антител или нуклеиновых кислот |
ляют по изменению количества одного из участников |
|
|
(иммунный или ДНК-анализ): в присутствии избытка |
циклического процесса. Так определяют, например, |
|
|
субстрата ферменты значительно увеличивают ин- |
концентрацию КоА в сопряженных реакциях, катали- |
|
|
тенсивность сигнала. Объем рынка ферментов, ис- |
зируемых фосфотрансацетилазой, цитратсинтазой и |
|
|
пользуемых в целях медицинской диагностики, со- |
малатдегидрогеназой. |
|
|
ставляет около 6 млрд долл. США в год. |
ПОЛУЧЕНИЕ И СВОЙСТВА. Объемы производства |
|
|
МЕТОДЫ ДЕТЕКТИРОВАНИЯ. В ферментативном ана- |
ферментов, используемых в медицине при проведе- |
|
|
лизе чаще всего используются фотометрические, |
нии лабораторных анализов, невелики, однако эти |
|
|
флуорометрические или люминометрические мето- |
препараты ферментов должны иметь очень высокую |
|
|
ды регистрации продукта реакции. Если продукт реак- |
чистоту. Обычно это внутриклеточные белки, кото- |
|
|
ции нельзя определять непосредственно, используют |
рые образуются в клетке в малых количествах, поэ- |
|
|
дополнительные ферменты, так называемую сопря- |
тому для их выделения и очистки используют специ- |
|
|
женную систему ферментативных реакций, продукты |
альные методы. К настоящему времени получено |
|
|
которых можно зрегистрировать. Например, в гидро- |
много рекомбинантных штаммов-суперпродуцентов. |
|
|
ксилазной реакции за восстановлением NAD(P)H |
Методами генетической инженерии в ген фермента |
|
|
можно наблюдать на длинах волн 334, 340 или |
могут быть внесены изменения, и такой белок будет |
|
|
366 нм. Современные спектрофотометры позволяют |
обладать свойствами, оптимальными для своего вы- |
|
|
проводить измерения в очень малых объемах образ- |
деления и применения. Наряду с чистотой и высокой |
|
|
ца (несколько микролитров). |
специфичностью фермент должен оставаться актив- |
|
|
ФЕРМЕНТАТИВНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ КОНЦЕН- |
ным в течение достаточно продолжительного вре- |
|
|
ТРАЦИИ. Ферментативные методы делятся на сле- |
мени, поэтому в препарат добавляют различные ста- |
|
|
дующие: |
|
билизаторы, благодаря чему при хранении при тем- |
|
а) метод конечной точки титрования; |
пературе до +40 °С ферменты теряют менее 20% |
|
|
б) кинетический метод; |
активности в год. |
|
|
в) метод ферментативного катализа. |
|
|
|
Конечная точка титрования дает возможность опре- |
|
|
|
деления количества субстрата или косубстрата, |
|
|
|
которое полностью превратилось в продукт. Так с по- |
|
|
|
мощью алкогольдегидрогеназной реакции опреде- |
|
|
|
ляют содержание спирта, а с помощью лактатгидро- |
|
|
|
геназной – лактата. Такой анализ выполняется всего |
|
|
|
за несколько минут. Окончание реакции (конечная |
|
|
|
точка) достигается тем быстрее, чем меньше Km или |
|
|
|
чем больше Vmax, т. е. пока концентрация субстрата |
|
|
|
самая высокая. Примером определения концентра- |
|
|
|
ции субстрата по продукту сопряженной реакции |
|
|
|
является |
ферментативное определение глюкозы |
|
78 |
с помощью гексокиназы и глюкозо-6-фосфат- |
|
|
дегидрогеназы. Другой, значительно более быстрый |
|
||
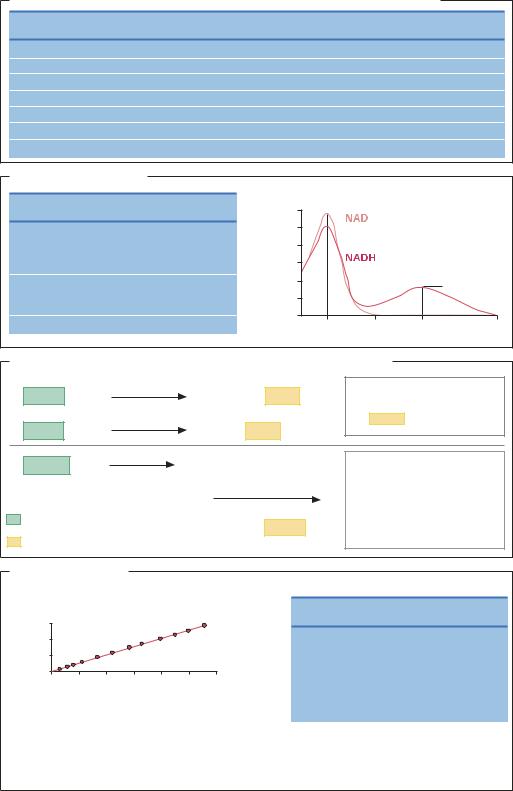
Ферменты, применяемые при проведении лабораторных клинических анализов |
|
|
||||||||||||||
Фермент |
|
|
|
ЕС-номер |
Анализируемое вещество |
|
Детектируемое |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
вещество |
|
||
Алкогольдегидрогеназа |
|
|
1.1.1.1. |
Этанол, другие спирты, альдегиды |
NADH |
|
|
|||||||||
Глюкозооксидаза |
|
|
1.1.3.4. |
Глюкоза |
|
|
|
|
Окраска |
|
||||||
Пируваткиназа |
|
|
2.7.1.40 |
Фосфоенолпируват, АДФ |
|
|
|
|
|
|||||||
Креатинкиназа |
|
|
3.5.3.3. |
Креатинин |
|
|
|
|
|
|
|
|||||
Цитратлиаза |
|
|
4.1.2.6. |
Лимонная кислота |
|
|
NAD+ |
|
|
|||||||
Маннозо-6-фосфатизомераза |
5.3.1.8. |
Манноза |
|
|
|
|
|
|
|
|
||||||
Сукцинил-КоА-синтетаза |
|
6.2.1.4. |
Сукцинат |
|
|
|
|
|
|
|
|
|||||
Методы детектирования |
|
|
|
|
|
|
|
|
|
|
|
|
||||
Метод |
|
|
|
Чувствительность |
|
Определение концентрации NADH |
|
|
||||||||
|
|
|
|
|
1,2 |
|
|
|
|
|
|
|||||
|
|
|
|
|
метода, ммоль/л |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Фотометрический |
|
|
10–6–10–5 |
|
|
Поглощение |
1,0 |
|
|
|
|
|
|
|||
Флуорометрический |
|
|
|
|
0,4 |
|
|
|
|
|
|
|||||
– по продукту реакции |
|
|
|
|
|
0,8 |
|
|
|
|
|
|
||||
– кинетический |
|
|
10–7–10–6 |
|
|
|
0,6 |
|
|
|
|
|
|
|||
– каталитический |
|
|
10–9–10–8 |
|
|
|
|
|
|
|
|
|
||||
– по продукту реакции |
|
|
10–9–10–8 |
|
|
|
|
|
|
|
|
0,315 |
|
|||
|
|
|
|
|
0,2 |
|
|
|
|
|
|
|||||
– каталитический |
|
|
10–15–10–14 |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
0 |
|
|
|
|
|
|
|||||
Люминометрический |
|
|
10–13–10–8 |
|
|
|
260 |
300 |
340 |
|
400 |
|||||
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
Длина волны, нм |
|
|||
Определение концентрации субстрата по количеству продукта реакции |
|
|
|
|
||||||||||||
а |
|
Алкоголь- |
|
|
|
|
|
|
|
|
|
|
|
|||
|
дегидрогеназа |
|
|
|
|
|
|
Прямое определение |
|
|||||||
|
Этанол |
Ацетальдегид + |
NADH |
+ H+ |
|
|||||||||||
|
+ NAD+ |
|
|
|
продукта |
|
|
|
|
|||||||
|
|
Лактат- |
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
или NADH |
|
|
|
|
|||
|
Лактат |
дегидрогеназа |
Пируват + |
NADH |
+ H+ |
|
|
|
|
|||||||
|
+ NAD+ |
|
|
|
|
|
|
|
|
|||||||
б |
|
Гексокиназа |
|
|
|
|
|
|
|
|
|
|
|
|||
|
Глюкоза |
+ ATФ |
|
|
|
Глюкозо-6-фосфат + AДФ |
Определение количества |
|
||||||||
|
|
|
|
|
|
Глюкозо-6-фосфат- |
продукта реакции |
|
|
|||||||
|
Глюкозо-6-фосфат |
+ |
NADP+ + |
дегидрогеназа |
|
|
в сопряженных реакциях: |
|
||||||||
|
H O |
|
|
|
|
|
с высокоспецифичной |
|
||||||||
|
Определяемое |
|
|
|
2 |
|
|
|
|
|
глюкозо-6-фосфатдегидрогеназой |
|||||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
и с менее специфичной |
|
|||||
|
соединение (аналит) |
|
|
6-Фосфоглюконат |
+ |
NADPH |
+ H+ |
|
||||||||
|
|
|
гексокиназой |
|
|
|
|
|||||||||
|
Вещество, концентрацию |
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
которого можно измерить |
|
|
|
|
|
|
|
|
|
|
|
|
|||
Кинетический метод |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Кинетический метод определения глюкозы с использованием |
Количество фермента и Km |
|
|
|
||||||||||||
гексокиназы и глюкозо-6-фосфатдегидрогеназы NADPH |
|
Аналит |
Фермент |
|
Km, |
|
v/Km, |
|||||||||
через 10 с после добавления фермента в анализатор |
|
|
|
|
||||||||||||
с |
0,6 |
|
|
|
|
|
|
|
|
|
|
|
|
моль/л |
МЕ/л* |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
/10 |
0,4 |
|
|
|
|
|
|
|
|
АДФ |
Аденилаткиназа |
1,6 ∙ 10–3 |
1600 |
|||
340 |
0,2 |
|
|
|
|
|
|
|
|
Глюкоза |
Гексокиназа |
|
1,0 ∙ 10–4 |
100 |
||
|
|
|
|
|
|
|
|
Глицерин |
Глицеринкиназа |
5,0 ∙ 10–5 |
50 |
|||||
A |
0,0 |
|
|
|
|
|
|
|
|
|||||||
|
20 |
|
|
40 |
60 |
|
|
Мочевая |
Уратоксидаза |
|
1,7 ∙ |
10–5 |
17 |
|||
|
0 |
|
|
|
|
кислота |
|
|
|
|
|
|||||
|
|
Глюкоза, ммоль/л |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
Фумаровая Фумараза |
|
1,7 ∙ |
10–6 |
1,7 |
||||||
Уравнение Михаэлиса–Ментен: |
|
|
|
|
|
|
||||||||||
|
|
|
|
|
кислота |
|
|
|
|
|
||||||
v = vmax × [S]/(Km + [S]) |
|
|
|
|
|
|
|
Чем выше Km, тем больше фермента необходимо |
||||||||
При концентрации субстрата [S], когда [S]<< Кm |
|
|
|
|||||||||||||
(Кm – константа Михаэлиса, характеризует сродство |
|
|
добавить к пробе, для того чтобы за несколько |
|||||||||||||
|
|
минут в продукт превратилось 99% субстрата. |
||||||||||||||
фермента к субстрату), скорость v ферментативной |
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||
реакции прямо пропорциональна концентрации |
|
|
|
|
|
|
|
|
|
|
||||||
субстрата [S]. |
|
|
|
|
|
|
|
|
|
|
|
|
|
79 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|