Материал: Шмид Р. Наглядная биотехнология и генетическая инженерия
Специальные продукты
70
Биотрансформация
ВВЕДЕНИЕ. Биотрансформация – основная функция организма, необходимая для осуществления нормального обмена веществ и обезвреживания токсичных веществ, в том числе ксенобиотиков. В биотехнологии под термином биотрансформация принято понимать биокатализ, то есть процесс ферментативного превращения природного или синтетического вещества-предшественника в продукт с необходимыми свойствами. Этот процесс может осуществляться в биореакторах микроорганизмами, целыми клетками животных или растений, их отдельными органеллами, а также иммобилизованными на носителях ферментами или клетками. В последние годы сильно выросла роль генетической инженерии для усовершенствования ферментов и получения рекомбинантных организмов. Термины «биокатализ», «ферментация» и «биотрансформация» в определенном смысле можно считать синонимами. Процесс биотрансформации включает одну или несколько стадий – каждую стадию катализирует отдельный фермент. Применение выделенных ферментов имеет ряд преимуществ: можно оптимизировать температурный режим проведения реакции, так как белок менее чувствителен к условиям среды, чем более сложные биологические системы (органеллы или клетки); отсутствует необходимость поддерживать стерильные условия реакции; фермент взаимодействует с субстратом более эффективно. Использование органелл или целых клеток более целесообразно в тех случаях, когда выделение фермента является сложной процедурой, если очищенный фермент нестабилен или процесс трансформации включает несколько стадий и все необходимые ферменты находятся в клетке.
МИКРООРГАНИЗМЫ используются как для получения природных метаболитов (например, глу-тами- новой кислоты), так и для превращения веществ, которые не являются их природными субстратами (к примеру, гидроксилирование стероидов по 11β-по- ложению). Как правило, ферменты катализируют реакции нормального метаболизма с высокой субстратной специфичностью. Экспрессия генов или целых генных кластеров, клонированных из другого организма, позволяет расширить круг веществ, подвергающихся биотрансформации, как, к примеру, в случае получения индиго. Метаболическая инженерия и белковый дизайн позволяют находить новые метаболические пути на основе анализа генома и играют важную роль при разработке методов промышленной биотрансформации.
ЖИВОТНЫЕ КЛЕТКИ широко используются для синтеза фармацевтических препаратов и антител в биореакторах. В настоящее время проводятся работы по созданию искусственной печени для очищения крови от некоторых токсических веществ. Токсины, выделен-
ные из крови при диализе, в результате биотрансформации осаждаются на молекулах альбумина.
РАСТИТЕЛЬНЫЕ КЛЕТКИ. Наиболее известный пример использования растительных клеток для биотрансформации – реакции специфического гидроксилирования. Так, в культуре Digitalis lanata в результате гидроксилирования дигитоксина по положению 12 образуется дигоксин. Биореакторы для культивирования растительных клеток по техническим причинам пригодны лишь для ограниченного числа процессов, например для синтеза таксола (PaclitaxelTM) Taxus brevifolia.
ОТДЕЛЬНЫЕ ФЕРМЕНТЫ целесообразно применять, если реакция биотрансформации проходит всего в одну стадию и может протекать в системе in vitro. В большинстве случаев в промышленности используются не требующие кофакторов ферменты, например, для реакций субстрат-специфичного гидролиза или этерификации. В последнее время изолированные ферменты также стали применяться для осуществления реакций присоединения по двойной связи, например в карбонильных группах.
«РЕКОМБИНАНТНЫЕ» ПУТИ ОБМЕНА ВЕЩЕСТВ. Наиболее яркими примерами использования этого подхода в промышленности является производство аскорбиновой кислоты в Erwinia herbicola (см. ранее)
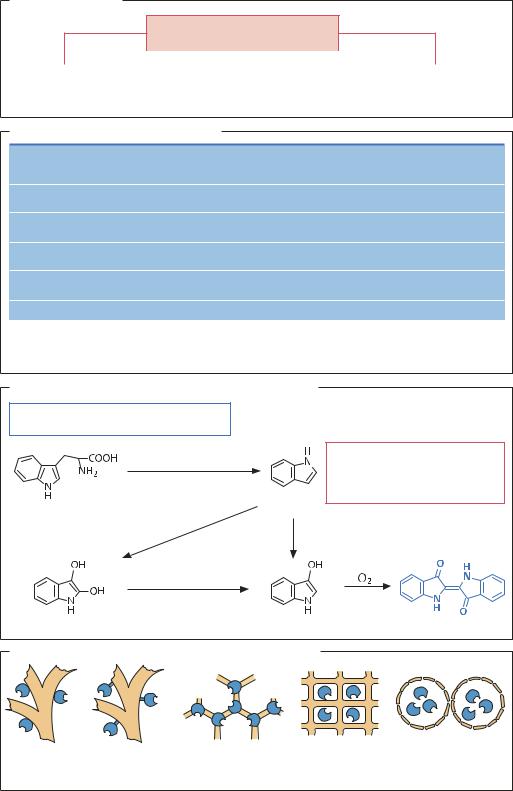
иполучение индиго в рекомбинантных клетках Escherichia coli. Методами генетической инженерии в клетках E. coli была дополнительно усилена активность триптофаназы, катализирующей реакцию превращения триптофана в индол, а затем с помощью TOL-плазмиды в клетки был введен ген нафталиндиоксигеназы из Pseudomonas sp. Полученный рекомбинантный штамм обладает способностью синтезировать индиго – один из самых распространенных красителей для тканей. Для получения L- или D-аминокислоты из синтетических гидантоинов используют хозяйские клетки E. coli с векторными кассетами, содержащими рекомбинантные гидантоиназы
икарбамилазы («синтетическая биология»).
Биотрансформация
Биотрансформация/биокатализ
Синтез необходимых продуктов
|
|
|
|
|
|
|
Ферментация |
|
«Покоящиеся» или иммобилизованные клетки |
|
Ферментативный катализ |
||
Живые клетки |
|
Kлетки в виде суспензии |
|
Один или несколько |
||
в биореакторах |
|
или иммобилизованные на носителе |
|
изолированных ферментов |
||
|
|
|
|
|
|
|
Примеры реакции биотрансформации
Реакция |
Организм/Фермент |
Процесс |
Фирма-разработчик |
|
|
|
|
D-сорбит → L-сорбоза |
Acetobacter suboxydans |
Ф |
Roche |
Фенил-D-лактат → 4-гидроксифенил- |
Beauveria gossypii |
Ф |
BASF |
D-лактат |
|
|
|
Фумаровая кислота → |
Escherichia coli |
ИмК |
Tanabe, DSM |
L-аспарагиновая кислота |
|
|
|
D-глюкоза → D-фруктоза |
Глюкозоизомераза |
ИмК, ИмФ |
Novo, Clinton |
|
из Streptomyces sp. |
|
|
D,L-ацетоксиметоксифенилэтиламин → |
Липаза из Pseudomonas |
ИмФ |
BASF |
L-фенилэтиламин |
cepacia |
|
|
Триптофан → индиго |
Pекомбинантный штамм E. coli |
ИмРК |
Genencor |
||
Ф – ферментация; |
|
|
|
|
|
ИмК – иммобилизованные клетки; |
|
|
|
|
|
ИмФ – иммобилизованные ферменты; |
|
|
|
|
|
ИмРК – иммобилизованные рекомбинантные клетки |
|
|
|
|
|
Производство индиго в рекомбинантных штаммах E. coli |
|
|
|||
Мутантный штамм E. coli – |
|
|
|
|
|
суперпродуцент индола |
|
|
|
|
|
|
|
|
Клонирование генов |
||
|
Триптофаназа |
|
из Pseudomonas sp.: |
||
|
|
|
а нафталиндиоксигеназа |
||
|
|
|
б ксиленоксидаза |
||
Триптофан |
|
Индол |
|
|
|
|
а |
б |
Ксиленоксидаза |
|
|
|
Нафталин- |
|
|||
|
|
|
|
|
|
|
диоксигеназа |
|
|
|
|
Спонтанная дегидратация |
|
|
|
|
|
цис-Индол-2,3-дигидродиол |
|
Индоксил |
|
Индиго |
|
Некоторые способы иммобилизации клеток и ферментов |
|
|
|||
Адсорбция |
Ковалентное |
Образование |
Включения |
Микрокапсулирование |
на носителе |
связывание |
поперечных |
в нерастворимый |
|
|
с носителем |
сшивок |
гель |
|
71
Copyright ОАО «ЦКБ «БИБКОМ» & ООО «Aгентство Kнига-Cервис»
Специальные продукты
72
Биотрансформация стероидов
ВВЕДЕНИЕ. Одним из примеров экономически выгод- |
мышленного использования такой реакции является |
||
ной биотрансформации является получение стерои- |
гидроксилирование одного из промежуточных проду- |
||
дов из стеролов. |
ктов синтеза гидрокортизона – соединения Рейх- |
||
СТЕРОИДЫ. К группе стероидов относятся более |
штейна «S» (вещество названо по имени Тадеуша |
||
10 000 природных и синтетических соединений, |
Рейхштейна – швейцарского химика, лауреата Нобе- |
||
многие из которых имеют важное фармацевтическое |
левской премии 1950 г., который впервые выделил |
||
значение. В качестве примеров можно привести |
кортизон и установил его структуру). Реакция проте- |
||
витамин D2 (кальциферол), кортикостероиды (проти- |
кает в клетках плесневого гриба Curvularia lunata. |
||
вовоспалительные средства), эстрогены и гестагены |
Чтобы предотвратить гидроксилирование по 7α- |
||
(женские половые гормоны), спиронолактон (моче- |
и 14α-атомам, «S»-вещество предварительно ацети- |
||
гонное средство). В промышленном синтезе сте- |
лируют по 17-гидроксигруппе. В процессе фермента- |
||
роидов используются различные типы биотранс- |
ции реакция биотрансформации идет с высокой сте- |
||
формации: например, отщепление боковой цепи |
реоспецифичностью. |
|
|
β-ситостерола с образованием андроста-4-ен- |
БИОСИНТЕЗ ПРЕГНЕНОЛОНА ИЗ САХАРОВ. При созда- |
||
3,17-диона (АД) или андроста-1,4-диен-3,17-диона |
нии рекомбинантного дрожжевого штамма, синтези- |
||
(АДД) и гидроксилирование 11-β-атома кортексоло- |
рующего прегненолон из сахаров, был использован |
||
на (также называемого соединением Рейхштей- |
новый экспериментальный подход. В процессе обра- |
||
на «S»). Аналогично получению индиго в клетках |
зования микостерола в дрожжах синтезируется эрго- |
||
E. coli, возможно осуществить процесс синтеза пре- |
стерол. В рекомбинантных штаммах были произведе- |
||
гненолона из сахаров в клетках дрожжей, и хотя эти |
ны следующие перестройки генома: во-первых, |
||
методы пока не используются в промышленности, |
выключен ген фермента, ответственного за окисли- |
||
очевидно, что в будущем биотрансформация станет |
тельное отщепление боковой цепи в |
-22-ненасы- |
|
очень важным технологическим приемом. |
щенных продуктах; во-вторых, в геном встроены три |
||
ОТЩЕПЛЕНИЕ БОКОВЫХ ЦЕПЕЙ. Традиционно основ- |
гена ферментов, участвующих в синтезе стеролов |
||
ным сырьем для производства стероидов служит |
крупного рогатого скота, и ген Arabidopsis thaliana |
||
диосгенин – природный стерол растительного проис- |
(резуховидка, двудольное травянистое растение), ко- |
||
хождения, главный поставщик – Мексика. Другие |
дирующий |
-7-редуктазу. Полученные рекомбинант- |
|
источники – желчные кислоты, которые поставляет |
ные штаммы, в которых экспрессируются все эти |
||
мясоперерабатывающая промышленность, и стигма- |
ферменты, обладают способностью синтезировать |
||
стерол – побочный продукт производства витамина Е |
прегненолон при росте на D-глюкозе. Кроме того, |
||
из соевого масла. Процессы превращения этих ве- |
если в |
клетках осуществлять |
коэкспрессию |
ществ в важные фармацевтические продукты (корти- |
3β-гидроксистероид-дегидрогеназы человека, из пре- |
||
костероиды, половые гормоны или спиронолактон) |
г-ненолона образуется прогестерон. Клонирование |
||
состоят из множества стадий. Поэтому для отщепле- |
гена монооксигеназы P450, которая осуществляет |
||
ния боковых цепей, в частности от β-ситостерола из |
избирательное гидроксилирование, приводит к гидро- |
||
соевого или рапсового масла, представляется пер- |
ксилированию молекулы прогестерона по положе- |
||
спективным использование таких микроорганизмов, |
ниям 11β-, 17α- и 21. Таким образом рекомбинант- |
||
как Mycobacterium, Nocardia, Arthrobacter или Cory- |
ный штамм дрожжей синтезирует гидрокортизон из |
||
nebacterium. В результате ферментативной реакции |
сахаров. Научные достижения, основанные на фунда- |
||
образуется андроста-4-ен-3,17-дион и андроста-1,4- |
ментальных исследованиях в области молекулярной |
||
диен-3,17-дион – предшественники эстрогенов и ге- |
биологии, используются в разработках компании |
||
стагенов, а также кортикостероидных гормонов. Дру- |
Sanofi-Aventis при оптимизации штаммов дрожжей |
||
гие источники сырья для производства стероидов, |
методами метаболической инженерии. Это приводит |
||
такие как холестерол или желчные кислоты, также |
к появлению конкурентоспособной технологии. |
||
могут быть использованы для биотрансформации, |
|
|
|
однако пока эти методы экономически невыгодны.
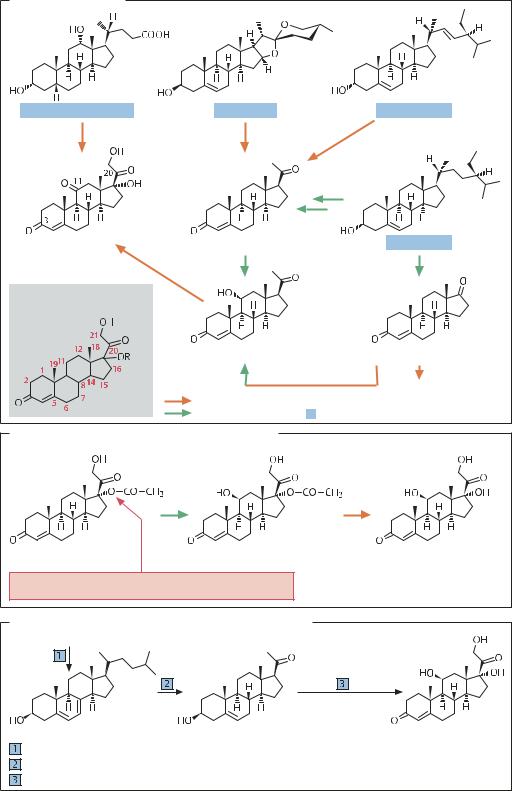
ГИДРОКСИЛИРОВАНИЕ 11β-АТОМА. Гидроксилирование – одна из важнейших стадий синтеза стероидов с заданной структурой. В настоящее время получены обширные коллекции микроорганизмов, в каждом из которых гидроксилирование протекает по определенному положению, что позволяет осуществлять гидроксилирование предшественников стероидов по всем возможным положениям. Важным примером про-
Copyright ОАО «ЦКБ «БИБКОМ» & ООО «Aгентство Kнига-Cервис»
Биосинтез стеролов |
|
|
Дезоксихолевая кислота |
Диосгенин |
Стигмастерол |
26 стадий |
5 стадий |
|
|
|
4 стадии |
Кортизон |
Прогестерон |
β-Ситостерол |
|
7 стадий |
|
Реакции гидроксилирования, |
|
|
осуществляемые различными |
|
|
микроорганизмами |
|
|
|
11-α-Гидроксипрогестерон |
Андроста-4-ен-3,17-дион (АД) |
|
Химические реакции |
Половые гормоны |
|
|
|
|
Ферментация |
Доступное промышленное сырье |
Гидроксилирование соединения Рейхштейна «S» |
|
|
в положении 11β в клетках Culvularia lunata |
|
|
17-Ацетат соединения |
17-Ацетат гидроксикортизона |
Гидрокортизон |
Рейхштейна «S» |
|
|
Ацетилирование субстрата по 17-гидроксигруппе препятствует |
|
|
гидроксилированию в положениях 7α и 14α. |
|
|
Синтез стероидов в рекомбинантных штаммах дрожжей |
|
|
Сахар |
|
|
|
|
|
|
|
|
21 |
|
|
|
11 |
17 |
|
|
3β-Гидроксистероид- |
|
|
|
|
дегидрогеназа, |
|
|
Эргостерол |
Прегненолон |
P450 моноокси- |
Био-гидрокортизон |
|
геназы CYP17A1, |
||||
Обмен веществ дрожжей |
|
CYP21A1, CYP11B1 |
|
|
|
|
|
|
|
Клонированные гены крупного рогатого скота, человека и растений |
|
|
||
Клонированный ген млекопитающих |
|
|
|
73 |
|
|
|
|
|
Ферменты |
Ферменты |
ВВЕДЕНИЕ. Применение ферментов животного, рас- |
|
тительного и микробного происхождения в промыш- |
|
|
ленном производстве или в аналитических целях |
|
началось около 100 лет назад. В 1970 г. иммобили- |
|
зованые ферменты были впервые использованы как |
|
биокатализаторы для химического превращения ве- |
|
щества (ферментативная трансформация). Развитие |
|
методов генетической инженерии и возможность по- |
|
лучения рекомбинантных белков с измененными |
|
свойствами открывает новые перспективы фермен- |
|
тации. |
|
КЛАССИФИКАЦИЯ ФЕРМЕНТОВ. В соответствии с ме- |
|
ждународной классификацией ферменты разделены |
|
на 6 классов, согласно типам реакций, которые они |
|
катализируют. К настоящему времени описаны тыся- |
|
чи разнообразных ферментов с различными функция- |
|
ми. Как правило, ферменты с аналогичными функци- |
|
ями, выделенные из разных организмов, несколько |
|
отличаются по структуре. При оценке возможностей |
|
использования фермента в биотехнологии необходи- |
|
мо располагать данными о его биологических свойст- |
|
вах. Так, около трети всех описанных ферментов яв- |
|
ляются мембраносвязанными, они нестабильны в |
|
очищенном виде. Для осуществления ферментатив- |
|
ной реакции многим оксидоредуктазам, трансфера- |
|
зам, лигазам и синтазам необходимы кофакторы, на- |
|
пример NADH, ATФ или кофермент А, поэтому |
|
использование таких ферментов в биотехнологиче- |
|
ских целях не всегда экономически выгодно из-за вы- |
|
соких цен на кофакторы. Гидролазам и изомеразам |
|
кофакторы не требуются, поэтому эти ферменты ши- |
|
роко используются в промышленности. Для большин- |
|
ства аналитических и диагностических исследований |
|
особенно важна высокая специфичность ферментов |
|
по отношению к субстрату. |
|
ПОЛУЧЕНИЕ ФЕРМЕНТОВ. Способ выделения и очист- |
|
ки фермента зависит от источника (животные, расти- |
|
тельные или микробные клетки), конкретной задачи, |
|
необходимого количества, а также биологических |
|
свойств фермента (растворимый или мембраносвя- |
|
занный белок). Ферменты, секретируемые во внекле- |
|
точное пространство, удается получать в больших ко- |
|
личествах (например, протеазы для производства |
|
стиральных порошков). В этом случае процедура очи- |
|
стки фермента значительно упрощена: после отделе- |
|
ния клеток следует стадия концентрирования культу- |
|
ральной жидкости методом ультрацентрифугирования |
|
или осаждения. Затем – высушивание распылением |
|
или в псевдоожиженном слое, после чего препарат |
|
фермента готов к промышленному использованию. |
|
Полученные таким способом препараты часто содер- |
|
жат значительные примеси посторонних белков, |
74 |
поэтому при их применении могут иметь место побоч- |
ные ферментативные реакции. В промышленности |
эти посторонние активности часто не влияют на производственный процесс. Для диагностических, аналитических и терапевтических целей чаще используют внутриклеточные ферменты, и в этом случае необходимы препараты ферментов с высокой степенью очистки. После разрушения клеток клеточный дебрис удаляют центрифугированием, а внутриклеточное содержимое концентрируют. Затем для удаления посторонних белков последовательно проводят несколько стадий хроматографического разделения компонентов полученного раствора. Степень очистки фермента определяют по следующим критериям: 1) удельная активность фермента; 2) активность других компонентов препарата; 3) электрофоретическая картина разделения компонентов препарата. Многие ферменты, использующиеся в промышленности, получены путем ферментации в рекомбинантных штаммах микроорганизмов. Методы генетической инженерии позволяют получать продукт с меньшим числом побочных активностей, следовательно, его очистка требует значительно меньших затрат.
РАЗРЕШЕНИЕ НА ИСПОЛЬЗОВАНИЕ. Ферменты являются природными белками, поэтому их использование во всех областях, за исключением пищевой промышленности или медицины, не требует специальных разрешений. Компоненты пищевых продуктов, полученные из природного сырья с помощью ферментов (например, изоглюкоза), относятся к «природным» и применяются наравне с естественными. В соответствии с постановлениями Международной ассоциации производителей ферментов для пищевой промышленности (AMFEP), при производстве продуктов питания разрешено использование ферментов животного и растительного происхождения, а также продуктов так называемых «безопасных» микробных штаммов. Применение ферментов, выделенных из других микроорганизмов, разрешается лишь после прохождения многочисленных и весьма дорогостоящих процедур тестирования и утверждения, поэтому использование таких ферментов в промышленных масштабах оказывается экономически невыгодным.