Материал: Шмид Р. Наглядная биотехнология и генетическая инженерия
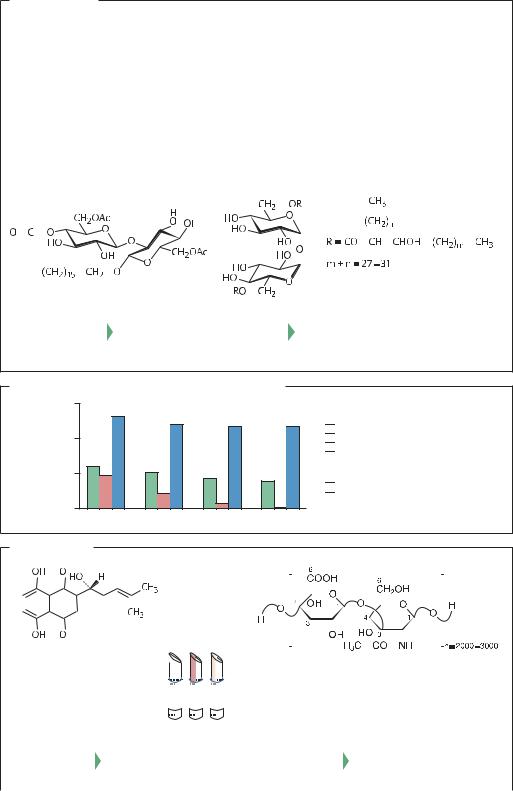
Биодетергенты
|
|
|
|
|
|
|
Продуцент |
Структурные компоненты |
|
|
|
|
|
||||||||||||
Софорозолипиды |
Torulopsis bombicola |
Софороза, жирные гидроксикислоты |
|
|
|
|
|
||||||||||||||||||
Целлобиозолипид |
Ustilago maydis |
Целлобиоза, жирные кислоты |
|
|
|
|
|
||||||||||||||||||
Рамнозолипид |
Pseudomonas aeruginosa |
Рамноза, жирные кислоты |
|
|
|
|
|
||||||||||||||||||
Трегалозолипид |
Corynebacterium, Arthrobacter |
Трегалоза, жирные кислоты |
|
|
|
|
|
||||||||||||||||||
Кориномиколат |
Corynebacterium, Arthrobacter |
Эфир миколовой кислоты и моно-, ди- и трисахаридов |
|||||||||||||||||||||||
Эмульзан |
Acinetobacter calcoaceticus |
Полианионный гетерополисахарид, M |
~ 106 Да |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
Сурфактин |
Bacillus subtilis |
Ацилированный гептапептид |
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
Софорозолипид |
|
|
Трегалозолипид |
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Инокулят |
|
Ферментация |
Arthrobacter sp. |
|
Источники углерода, азота |
|
|
и фосфора, морская вода; |
|
|
нефть для индукции синтеза |
|
|
|
Биодетергенты и удаление нефтяных загрязнений
Остаточное содержание |
полициклических |
ароматических |
углеводородов, ppm |
300 |
|
200 |
|
100 |
|
0 |
Май |
|
Июль |
Сентябрь |
Ноябрь |
Очистка |
|
|
Солюбилизация, |
|
Выход продукта |
хроматография |
|
до 100 г/л |
|
|
|
Загрязнение участка прибрежной отмели площадью 2 м2 нефтью

 10 × загрязнение 1 литром нефти
10 × загрязнение 1 литром нефти

 10 × загрязнение 1 литром нефти; с добавлением трегалозодикориномиколата в концентрации 1 г/л;
10 × загрязнение 1 литром нефти; с добавлением трегалозодикориномиколата в концентрации 1 г/л;
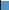
 10 × загрязнение 1 литром нефти; с добавлением неионных детергентов
10 × загрязнение 1 литром нефти; с добавлением неионных детергентов
в концентрации 100 мл/л (диспергирует лучше, но затрудняет деградацию)
Биокосметика
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Шиконин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
Гиалуроновая кислота |
|
|
|
|
|
|
|
|
|
||||||
|
С16Н16O5 |
288,30 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
MR |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
Тпл |
143 °С |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
Код CAS |
517-89-5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
Lithospermum |
|
Реактор |
|
Выход |
|
|
|
|
|
|
|
|
|
|
|
Выход |
|
|
|||||||||
|
erythrorhizon |
|
|
|
|
|
продукта |
|
Streptococcus |
|
|
|
|
|
|
|
|
|||||||||||
|
|
Объем |
|
|
|
Ферментация |
|
5–10 г/л |
|
|
||||||||||||||||||
|
Иммобилизо- |
|
несколько |
|
Несколько |
|
equi |
|
|
|
|
|
|
|
после 10 ч |
|
||||||||||||
|
ванные клетки |
|
сотен литров |
|
г/л |
|
|
|
|
|
|
|
|
|
|
|
|
|
65 |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Специальные продукты
66
Микробные полисахариды
ВВЕДЕНИЕ. Растительные полисахариды (крахмал, целлюлоза, гуммиарабик, гуаровая смола, пектин, альгинаты, агар и др.) и их полусинтетические производные играют важную роль в современных технологиях, в том числе в качестве загустителей в пищевой промышленности или при заводнении нефтяных скважин. Производство полисахаридов растительного происхождения достигает нескольких десятков тысяч тонн в год. Внеклеточные микробные полисахариды также могли бы найти применение в самых разнообразных отраслях промышленности, однако из-за значительных производственных затрат их использование пока ограничено. Наибольшее значение имеют ксантан и декстран. Гиалуроновая кислота уже применяется в биокосметике.
КСАНТАН представляет собой разветвленный гетерополисахарид, состоит из пяти остатков гексоз (глюкозы, маннозы и глюкуроновой кислоты). Молекулярная масса ксантанов – от 2 до 12 тыс. кДа. Ксантановые смолы имеют высокую вязкость (в зависимости от числа групп пирувата в полимере) и по ряду свойств сходны с пластмассой. Эти вещества безвредны для человека, поэтому их добавляют в качестве стабилизаторов и загустителей во многие пищевые продукты. Кроме того, благодаря устойчивости в растворах электролитов ксантаны добавляют к буровому шламу при бурении нефтяных скважин. Ксантаны образуются в клетках Xanthomonas campestris при аэробном росте на среде с глюкозой. Получение ксантанов осуществляют, как правило, в процессе периодической ферментации, используя в качестве источника углерода глюкозу, а в качестве источника азота – пептон, нитрат аммония и мочевину. Клонирование генов β-галактозидазы (lacZ) и лактопермеазы (lacY) из Escherichia coli в геном X. сampestris позволило получить штамм, использующий в качестве источника углерода молочную сыворотку (отходы молочной промышленности). Из-за образования ксантанов культуральная жидкость становится очень вязкой (до 10 000 сантипуаз). Для сохранения аэробных условий роста в этом случае особое значение имеют мешалки специальной конструкции. Как правило, ксантаны из среды осаждают растворителем – изопропанолом. В современной промышленности производство ксантанов достигает 30 000 т/год. ДЕКСТРАНЫ – очень важные вещества, которые могут служить заменителями плазмы крови. Благодаря тому, что полимерные цепи в этих веществах имеют поперечные сшивки, образуются сетчатые структуры, которые очень эффектны при очистке белков разного размера. Декстраны также применяются в пищевой промышленности. Разветвленные цепи декстранов, состоящие только из остатков глюкозы, связанных между собой α-1,6-связями, имеют моле-
кулярную массу ~5 107 Да. У дрожжей и некоторых бактерий декстраны играют роль резервных полисахаридов. В качестве примера продуцента декстрана можно назвать Streptococcus mutans, бактерию, которая обитает в кариозной полости зуба человека. Образование декстрана приводит к появлению бактериального налета («камней»). Для промышленного получения декстрана используют Leuconostoc mesenteroides: в течение 24 ч в клетках этого микроорганизма из сахарозы образуется до 500 г/л декстрана. Декстран выделяют из культуральной жидкости осаждением этанолом, затем гидролизуют кислотой и еще раз осаждают этанолом. Декстран с молекулярной массой 75 000 Да используют как заменитель плазмы крови, а с молекулярной массой 40 000 Да – в качестве антитромболитика при полостных операциях.
ДРУГИЕ МИКРОБНЫЕ ПОЛИСАХАРИДЫ. Pseudomonas aeruginosa и Azotobacter vinelandii синтезируют альгинаты, по строению аналогичные альгинатам из водорослей. Альгинаты часто используют в качестве носителей для иммобилизации клеток при проведении различных биокаталитических реакций. Некоторые базидиомицеты синтезируют полимер склероглюкан, главная цепь которого образована остатками глюкозы, соединенными β-1,3-связями, а в местах разветвления остатки глюкозы присоединены β-1,6- связями. Склероглюкан, как и геллан, образующийся в клетках Auromonas elodea, используется как пищевая добавка. Пуллулан – глюкан с разветвленной цепью, в которой остатки глюкозы соединены α-1,4- (90%) и α-1,6- (10%) связями. Из пуллулана изготовляются тонкие пленки, не пропускающие кислород, которые используются для защиты пищевых и других продуктов от окисления. Промышленное получение микробных полисахаридов пока является очень дорогостоящим и экономически невыгодным процессом, поэтому такие полимеры еще не нашли широкого применения в современных технологиях.
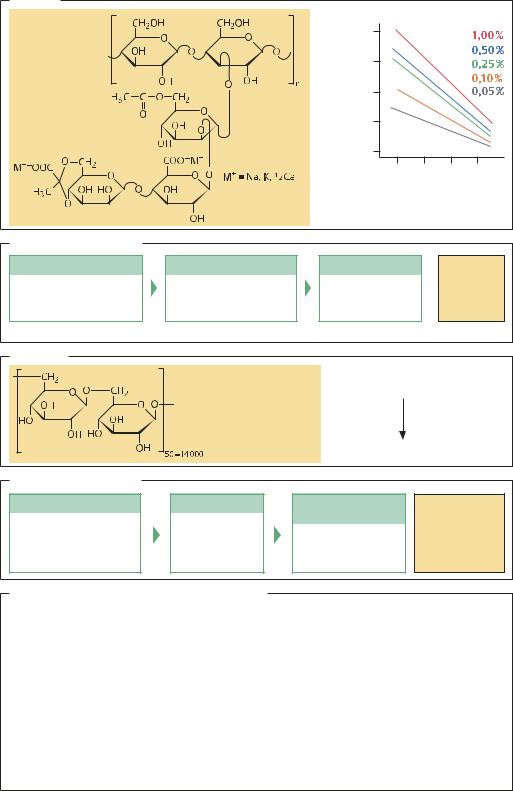
Ксантан |
|
|
|
|
|
|
|
Степень |
|
|
Псевдопластические свойства |
|
|||
|
|
|
|
|
|
|
|
полимеризации |
|
|
10 000 |
|
|
|
|
~ 10 000 |
|
|
вязкость,с |
|
|
|
|
|
|
|
1000 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Кажущаяся мПа |
100 |
|
|
|
|
|
|
10 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
1 |
10 |
100 |
1000 |
|
|
|
|
log скорости сдвига, с–1 |
|||
|
Код CAS |
11138-66-2 |
0,05–1%-я суспензия |
|
|
|
|
|
ксантана в воде, 25 °C |
|
|
||||
Ферментация и очистка |
|
|
|
|
|
|
|
Предферментация |
Биореактор |
Выделение |
|
Выход |
|||
Xanthomonas campestris*; |
Объем более 120 м3, |
Пастеризация, |
|
продукта |
|||
глюкоза или декстран, |
40–80 ч, 28 °С, рН 7,0, |
осаждение этанолом |
|
до 30 г/л |
|||
|
после 60 ч |
||||||
источник азота |
специальные мешалки |
или 2-пропанолом |
|
||||
|
ферментации |
||||||
|
(из-за высокой вязкости) |
|
|
|
|||
|
|
|
|
|
|
||
* X. campestris – растительный патоген, вторая степень биологической опасности |
|
|
|
|
|||
Декстран |
|
|
Биосинтез |
|
|
|
|
|
1,6-α-D-глюкоза; |
|
|
|
|||
|
(1,6-α-D-глюкозил)n + сахароза |
||||||
|
степень полимеризации |
||||||
|
~ 28 000; |
|
|
|
|
|
|
|
1,2-, 1,3- |
|
|
Декстран-сахараза |
|||
|
и 1,4-гликозидные связи |
|
|||||
|
Код CAS |
9004-54-0 |
(1,6-α-D-глюкозил)n+1 + фруктоза |
||||
Ферментация и очистка |
|
|
|
|
|
Биореактор |
Выделение |
Гидролиз |
|
Leuconostoc mesenteroides |
Осаждение |
и фракционирование |
Выход продукта |
|
|
||||
1) |
Инокуляция. |
этанолом, |
Декстраны |
100 г/л через 24 ч |
2) |
Фаза синтеза; сахароза |
ацетоном |
разного размера |
(утилизируется |
|
в качестве источника |
или метанолом |
|
~ 45% сахарозы) |
|
углерода, 23 °С |
|
|
|
Производство и использование полисахаридов |
|
|
||
Полисахарид |
Объем |
Цена, |
Микроорганизм- |
Применение |
|
производства, |
долл./кг |
продуцент |
|
|
т/год |
|
|
|
Ксантан |
40 000 |
10 |
Xanthomonas |
Пищевая добавка, при заводнении |
|
|
|
campestris |
нефтяных скважин |
Декстран, |
2000 |
35–390 |
Leuconostoc |
Заменитель плазмы крови, пищевая |
производные |
600 |
400–2800 |
mesenteroides |
добавка, биохимический реактив |
декстрана |
|
|
|
|
Гиалуроновая |
500 |
2000–100 000 |
Streptococcus equi |
Хирургия, косметология |
кислота |
|
|
|
|
|
|
|
|
|
Микробные полисахариды, производимые в небольших объемах:
альгинат (Azotobacter), курдлан (Agrobacterium, Rhizobium), геллан (Auromonas),
пуллулан (Pullularia), целлюлоза (Acetobacter)
67
продукты |
Биоматериалы |
|
масляной кислоты все чаще находят применение в со- |
||
|
ВВЕДЕНИЕ. Материалы на основе поли-3-гидрокси- |
|
Специальные |
временной промышленности. Необычными свойства- |
|
ми, чрезвычайно интересными для технологического |
||
|
||
|
применения, обладают природные белки натурального |
|
|
шелка (фиброин и спидроин) или белок мидий, поэто- |
|
|
му в настоящее время ведутся активные исследования |
|
|
возможностей получения этих веществ методами ге- |
|
|
нетической инженерии. Производные бактериородоп- |
|
|
сина, синтезируемого Halobacterium salinarum, воз- |
|
|
можно, найдут применение в качестве оптического |
|
|
носителя информации. |
|
|
ПОЛИМЕРЫ, СПОСОБНЫЕ К БИОРАЗЛОЖЕНИЮ. В про- |
|
|
мышленности уже получают из L-молочной кислоты |
|
|
полилактид (Nature WorksTM). Производится также сопо- |
|
|
лимер получаемого биотехнологическим путем 1,3-про- |
|
|
пандиола и терефталевой кислоты (SoronaTM). При полу- |
|
|
чении 1,3-пропандиола используются рекомбинантные |
|
|
штаммы E. coli, метаболизм которых изменен внедрени- |
|
|
ем гена глицерин-дегидратазы методами метаболиче- |
|
|
ской инженерии. Многие микроорганизмы, например |
|
|
Ralstonia eutropha, в определенных условиях способны |
|
|
запасать в клетке полигидроксимасляную кислоту, со- |
|
|
держание которой может достигать 90% сухой клеточ- |
|
|
ной массы. Состав запасных полимеров зависит от со- |
|
|
става питательной среды, поэтому, добавляя в среду |
|
|
роста различные вещества-предшественники, можно уп- |
|
|
равлять процессом образования продукта. Для техноло- |
|
|
гического применения наиболее интересен сополимер |
|
|
3-гидроксимасляной и 3-гидроксивалериановой кислот, |
|
|
который проявляет свойства полипропилена, однако в от- |
|
|
личие от последнего может разлагаться биологическим |
|
|
путем. Получение этого сополимера ферментацией пока |
|
|
очень дорогой процесс, поэтому это вещество находит |
|
|
лишь ограниченное применение – в медицине (препарат |
|
|
Biopol®). Оперон синтеза поли-3-гидроксимасляной кис- |
|
|
лоты содержит 3 гена, которые уже клонированы. Транс- |
|
|
формация растений и клеток Escherichia coli плазмидами, |
|
|
содержащими эти гены, позволила получать поли-3-гид- |
|
|
роксимасляную кислоту с выходом до 95% сухой клеточ- |
|
|
ной массы. Для выделения образующегося в клетках по- |
|
|
лимера используют экстракцию органическими |
|
|
растворителями или энзиматическое расщепление. |
|
|
ФИБРОИН И СПИДРОИН. Белки образуются в специаль- |
|
|
ных железах гусеницы тутового шелкопряда (Bombyx |
|
|
mori) для создания кокона при окукливании, а также в |
|
|
паутинных железах многих паукообразных (например, |
|
|
паука крестовика Nephila claviceps). Натуральное волок- |
|
|
но имеет очень хорошие технические перспективы, в ча- |
|
|
стности для создания парашютной ткани, так как многие |
|
|
их свойства уникальны. Волокна каркасной нити паути- |
|
|
ны, состоящие из белка спидроина, при равной толщине |
|
|
волокна в несколько раз прочнее стали и при этом спо- |
|
|
собны растягиваться на 30% своей длины без разрыва |
|
68 |
(BioSteelTM). Фиброин и спидроин являются фибрилляр- |
ными белками, гены которых удалось клонировать и модифицировать для экспрессии в клетках E. coli и Pichia pastoris. Выход рекомбинантных белков фиброина и спидроина составляет около 1 г/л.
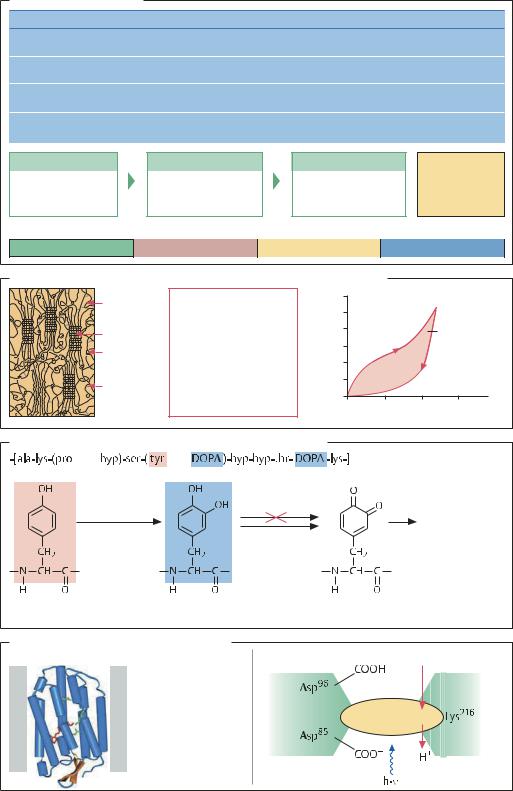
БЕЛКИ С АДГЕЗИОННЫМИ СВОЙСТВАМИ. Мидии Mytilus edulis обладают способностью прикрепляться к раковинам ракообразных или поверхности обшивки кораблей
итаким образом перемещаться на большие расстояния. Эти моллюски синтезируют специфический белок, проявляющий адгезионные свойства. Белок-предшествен- ник имеет молекулярную массу 130 кДа и состоит преимущественно из полярных аминокислот – тирозина, серина, треонина, лизина и пролина. В ходе посттрансляционных модификаций остатки тирозина и пролина преобразуются в о-гидрокситирозин или 3- или 4-гидро- кси-L-пролин соответственно. На воздухе полипептиптидные цепи полимеризуются, и образуются дихиноны. Методами генетической инженерии удалось осуществить гетерологичную экспрессию фрагмента белка адгезии размером 25 кДа в клетках E. coli с достаточно высоким выходом. Однако в этих клетках-хозяевах не происходит посттрансляционных модификаций белков, поэтому выделенный рекомбинантный продукт обрабатывают ферментом тирозиназой, который гидролизует остатки тирозина до о-гидрокситирозина, что обеспечивает образование поперечных сшивок между полипептидными цепями. Полученный белок используют в медицинских целях, в том числе в стоматологии для заполнения полостей в зубе.
БАКТЕРИОРОДОПСИН. Галобактерия Halobacterium salinarum обитает в средах с повышенным содержанием поваренной соли: концентрация NaCl 3–5 М является нормальной для ее роста. При фототрофном росте бактериородопсин служит в качестве протонного насоса
итаким образом снабжает клетку энергией. Молекулы бактериородопсина формируют в клеточной мембране агрегаты (бляшки), которые легко выделяются в составе так называемой «пурпурной мембраны», на 75% по массе состоящей из белков и на 25% из липидов. Препараты «пурпурных мембран» очень стабильны. Кофактор бактериородопсина ретиналь и процесс его цис-транс- изомеризации связан с необычной функцией: бактериородопсин действует как светозависимый протонный насос, число оборотов которого может достигать 100 в секунду. В восстановленной форме бактериоро-
допсин имеет пурпурный цвет (λmax = 570 нм), а при протонировании ретиналя и остатка лизина в положе-
нии 216 становится желтым (λmax = 410нм). Замена определенных аминокислотных остатков путем направленного мутагенеза дает возможность регулировать скорость циклического светозависимого изменения цвета бактериородопсина. Чрезвычайно перспективным представляется использование бактериородопсина и его производных в качестве оптического носителя информации (фотоэлемента).
Ферментация и очистка |
|
|
|
|
|
|
|
|
|
|
||
Организм |
Продукт |
|
|
|
|
Фирма-производитель |
|
|||||
Ralstonia eutropha |
Сополимер 3-гидроксимасляной |
|
|
Metabolix (коммерческий продукт) |
|
|||||||
|
и 3-гидроксивалериановой кислот |
|
|
|
|
|
|
|
|
|||
Escherichia coli |
Поли(3-гидроксимасляная кислота), |
|
|
ATO-DLO |
|
|
|
|
|
|||
|
клонирован оперон из Alcaligenes latus |
|
|
|
|
|
|
|
|
|||
Lactobacillus |
Хирально чистый L-полилактид |
|
|
Cargill (производство) |
|
|||||||
|
из L-молочной кислоты |
|
|
|
|
|
|
|
|
|
||
E. coli |
Сополимер пропан-1,3-диола |
|
|
DuPont, Geneva (производство) |
|
|||||||
с генами Klebsiella |
и терефталевой кислоты |
|
|
|
|
|
|
|
|
|
||
Ralstonia eutropha |
|
|
Биореактор |
|
|
Выделение |
|
|
|
|
|
|
Гетеротрофный |
|
Непрерывная |
|
Ферментативные |
|
|
Выход продукта |
|
||||
штамм-продуцент |
|
ферментация, глюкоза, |
методы |
|
|
|
более 80 г/л |
|
||||
|
|
пропионовая кислота, |
|
|
|
|
|
(более 2 г/л в ч) |
|
|||
|
|
30 °С, ~ 40 ч |
|
|
|
|
|
|
|
|
|
|
Структура оперона синтеза поли(3-гидроксимасляной кислоты) из Ralstonia eutropha |
|
|
|
|
||||||||
Промотор |
|
|
РНК-Синтаза |
3-Кетотиолаза |
Ацетил-КоА-редуктаза |
|
||||||
Волокна каркасной нити паутины паука-крестовика (Nephila claviceps) |
|
|
|
|
||||||||
|
β-слои |
Основной компонент |
разрыв,на |
Н/м |
6 |
|
|
|
|
|
||
|
(gly–gly–x)12-спейсер |
|
|
|
|
|
|
|||||
|
Аморфные |
белка каркасной нити |
|
|
5 |
|
|
|
|
|
||
|
нити |
|
(gly–pro–gly–gly–x)3–63 – |
|
|
|
|
|
|
|
||
|
|
|
|
2 |
4 |
|
|
|
Энергия, |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Водородные |
Эластичность |
35% |
Прочность |
9 |
3 |
|
|
|
выделяющаяся |
|
|
|
10 |
|
|
|
|
в виде тепла |
|
|||||
|
Сшивки |
|
|
|
|
2 |
|
|
|
|
||
|
|
|
Прочность |
4 109 Н/м2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
мостики |
Прочность |
105 Дж/кг |
|
|
0 |
|
|
|
|
|
|
|
|
|
на разрыв |
|
|
0 |
5 |
|
10 |
15 |
|
|
|
|
|
|
|
|
|
|
Растяжимость, % |
|
|||
Белок с адгезионными свойствами из мидий Mytilus edulis |
|
|
|
|
|
|
|
|||||
или |
|
|
или |
|
|
|
|
hyp |
= |
4-гидроксипролин |
|
|
|
|
|
|
|
|
|
|
DOPA = |
3,4-дигидрокси- |
|
||
|
|
|
|
|
|
|
|
|
|
фенилаланин |
|
|
Тирозиназа |
|
Аскорбиновая кислота |
|
|
Окисление, |
|
||||||
из шампиньонов |
|
|
|
|
|
|
|
образование |
|
|||
|
|
|
|
|
|
|
|
|
|
сшивок |
|
|
|
|
|
|
Кислород воздуха |
|
|
|
|
и связывание |
|
||
|
|
|
|
|
|
|
|
с поверхностью |
|
|||
|
|
|
|
|
|
|
|
|
|
|
||
Генно-инженерный |
|
|
Активирован в виде преполимера, |
|
|
|
|
|
|
|
||
белок-предшественник |
|
стабилизирован аскорбиновой кислотой |
|
|
|
|
|
|||||
Бактериородопсин как протонный насос |
Донор |
|
|
|
|
|
Поток |
|
||||
Цитоплазма |
|
|
|
|
|
|
|
|
|
|||
|
|
|
протонов |
|
|
|
|
|
протонов |
|
||
|
|
Бактериородопсин |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
||
|
|
(по рентгено- |
|
|
|
|
|
|
|
|
|
|
Мембрана |
Мембрана |
структурным данным |
|
|
|
|
|
|
|
|
|
|
с разрешением 0,23 нм); |
|
|
Ретиналь-CH = NH |
|
|
|||||||
|
|
|
|
|
|
|||||||
|
|
красным |
|
|
|
|
|
|||||
|
|
обозначен ретиналь, |
|
|
|
|
|
|
|
|
|
|
|
|
зеленым – |
|
|
|
|
|
|
|
|
|
|
|
|
Asp85, Asp96, Lys216 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Акцептор |
|
|
|
|
|
Протонирование |
|
|
|
|
|
|
протонов |
|
|
|
|
|
ретиналя |
69 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|