Материал: Шмид Р. Наглядная биотехнология и генетическая инженерия
Специальные продукты
60
Витамины
ВВЕДЕНИЕ. Витамины используются как лекарственные препараты, а также как пищевые и кормовые добавки. Мировой объем рынка витаминов составляет около 3 млрд долл. США в год. Большинство витаминов получают путем химического синтеза или экстракции из растительного материала. Биотехнологическим путем производятся витамины В2, В12 и С.
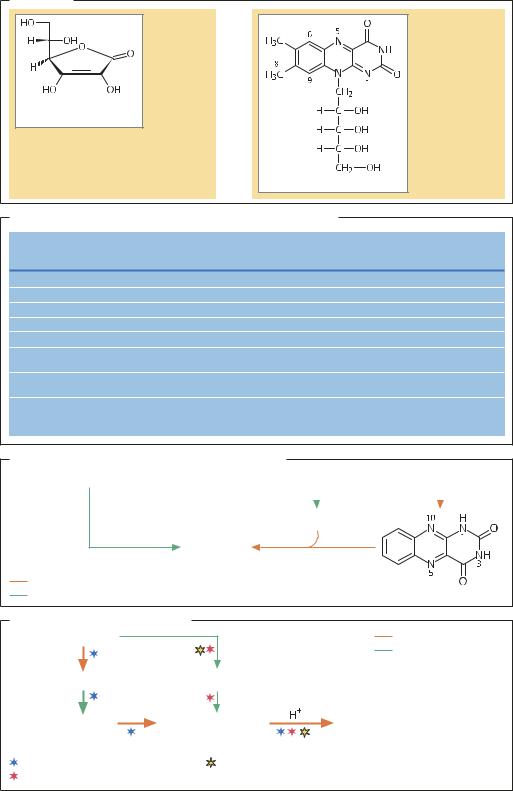
ВИТАМИН В2 (РИБОФЛАВИН). Рибофлавин в форме ФМН или ФАД – важнейший кофермент в окисли- тельно-восстановительных процессах. В свободном виде рибофлавин присутствует только в молоке. Недостаток этого витамина в пище приводит к кожным патологиям, нарушению роста и глазным болезням. У животных рибофлавин образуется в сложной многостадийной реакции из гуанозинтрифосфата. В промышленности витамин В2 получают одним из трех способов: химическим синтезом, ферментацией или химико-ферментативным методом. В последние годы по экологическим и экономическим соображениям стали использовать ферментативные технологии. Рибофлавин производят путем ферментации штам- мами-суперпродуцентами Ashbya gossypii. В биореактор в качестве источника углерода добавляют мелассу, а в качестве источника азота – соевая мука; выход рибофлавина составляет до 15 г/л за 72 ч. После удаления клеток продукт очищают хроматографически. При химико-ферментативном методе получения витамина В2 аллоксазиновое кольцо синтезируют химическим способом, а затем также путем химической реакции соединяют его с остатком D-ри- бозы, которую в свою очередь получают из D-глюкозы в клетках мутантных штаммов Bacillus pumilus. Такой метод пока не нашел широкого применения в промышленности.
ВИТАМИН В12 (ЦИАНОКОБАЛАМИН). В качестве кофермента производное витамина В12 (5'-дезокси- аденозилкобаламин) участвует в чрезвычайно важных реакциях метилирования и изомеризации. Этот витамин является необходимым компонентом пищи человека и большинства животных. При недостатке витамина В12 в пище может развиться так называемая злокачественная (пернициозная) анемия. Около половины производимого в мире витамина В12 используется в качестве кормовых добавок при разведении сельскохозяйственных животных. Биосинтез из почти 30 реакций включает стадию образования 5'-дезоксиаденозилкобаламина через 5-амино-4-оксовалериановую (δ-аминолевулиновую) кислоту при конденсации сукцинил-КоА и глицина. Промышленное производство витамина В12 осуществляется исключительно ферментацией с использованием Propionibacterium shermanii или Pseudomonas denitrificans. В биореакторы в качестве сырья добавляют мелассу и аммонийные соли, а также вещест-
ва-предшественники – соли кобальта и 5,6-диметил- бензимидазол. Через 120 ч после начала ферментации содержание витамина В12 в среде может достигать 150 мг/л. К настоящему времени клонированы все гены Propionibacterium shermanii, продукты которых участвуют в биосинтезе витамина В12, а методами метаболической инженерии ведутся работы по созданию новых штаммов-суперпродуцентов.
ВИТАМИН С (L-АСКОРБИНОВАЯ КИСЛОТА). Аскорбиновая кислота является «физиологическим восстановителем» и участвует во многих реакциях как кофактор, а также служит в качестве антиоксиданта, восстанавливающего кислородные радикалы. Дефицит витамина С приводит к возникновению цинги (скорбута) – заболевания соединительной ткани. Аскорбиновая кислота продается в аптеках, ее также добавляют в продукты питания в качестве антиоксиданта. Годовое производство витамина С достигает 95 000 т. Промышленный способ получения аскорбиновой кислоты из D-глюкозы основан на комбинации химического синтеза и ферментации. По методу Рейхштейна–Грюсснера реакция окисления D-сорби- та в L-сорбозу осуществляется в непрерывном режиме с помощью иммобилизованных клеток Acetobacter suboxydans в две стадии. При этом необходима интенсивная и постоянная подача воздуха в реактор. Через 24 ч ферментации выход продукта практически количественный. По методу Соноямы происходит окисление D-глюкозы клетками Erwinia sp. до 2,5-ди- окси-D-глюкозы с последующим восстановлением до 2-оксо-L-гулоновой кислоты с помощью Corynebacterium sp.; эффективность переработки сырья на первой стадии составляет 94% через 24 ч, а на второй – 92% через 66 ч. Затем образовавшаяся 2-оксо-L-гулоновая кислота легко превращается в кислых условиях в L-аскорбиновую. Гены ферментов, которые осуществляют две указанные реакции, в настоящее время клонированы, и специалистами фирмы Genentech получен рекомбинантный штамм Erwinia herbicola, который осуществляет весь процесс превращения D-глюкозы в 2-оксо-L-гулоновую кислоту с последующим окислением в L-аскорбиновую кислоту. Однако рост клеток полученного рекомбинантного штамма Erwinia herbicola значительно замедляется в присутствии D-глюкозы, поэтому пока этот метод получения витамина С экономически невыгоден.
Витамины |
|
|
|
|
|
С17Н20N4O6 |
|
|
|
MR |
376,36 |
|
|
Код CAS |
83-88-5 |
L-аскорбиновая кислота |
|
|
|
(витамин С) |
|
|
|
С6Н8O6 |
|
|
|
MR |
176,13 |
Рибофлавин |
|
Код CAS |
50-81-7 |
|
|
|
|
(витамин В2) |
|
Способы промышленного получения и объемы производства |
|
||
Витамин |
Объем |
Способ получения |
Применение |
|
производства, |
|
|
|
т (2004 г.) |
|
|
А и про-А |
β-Каротин |
2 900 |
Химический синтез |
Корм для животных, краситель |
В1 |
Тиамин |
3 300 |
Химический синтез |
Корм для животных, здравоохранение |
В2 |
Рибофлавин |
4 000 |
Ферментация (100%) |
Корм для животных, здравоохранение |
В6 |
Пиридоксаль |
3 400 |
Химический синтез |
Корм для животных, здравоохранение |
В12 |
Кобаламин |
23 |
Ферментация |
Медицина, корм для животных |
С |
Аскорбиновая |
95 000 |
Химико-ферментативный |
Пищевая добавка, здравоохранение |
|
кислота |
|
способ |
|
D3 |
Кальциферол |
45 000 |
Химический синтез |
Медицина |
|
|
|
(из дегидрохолестерина) |
|
Е |
α-Токоферол |
25 000 |
Химический синтез. |
Корм для животных, |
|
|
3 500 |
Экстракция из растительных |
пищевая добавка |
|
|
|
масел и водорослей |
|
Биотехнологические пути получения рибофлавина
Меласса, источник азота, соли |
D-Глюкоза |
Фенилендиамин + аллоксан |
|||
Ashbya gossypii |
Bacillus pumilus |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
Bacillus sp. |
D-Рибоза |
|
|
||
Candida sp. |
|
|
|||
|
|
|
|
|
|
|
|
Рибофлавин |
|
|
|
(витамин В2) |
|
Химический синтез (более не применяется) |
Аллоксазин |
||
Ферментация или биотрансформация |
|||
Синтез L-аскорбиновой кислоты |
|
||
D-Глюкоза |
|
|
Химический синтез |
|
|
Erwinia herbicola |
Ферментация |
|
|
|
или биотрансформация |
D-Сорбит |
2,5-Диоксо-D-глюконовая кислота |
|
|
Acetobacter |
|
Corynebacterium sp. |
|
suboxydans |
|
|
|
L-Сорбоза |
|
2-Оксо-L-гулоновая |
L-Аскорбиновая кислота (витамин С) |
|
|
кислота |
|
Метод Рейхштейна–Грюсснера |
Метод с рекомбинантным штаммом Erwinia herbicola, |
||
Метод Соноямы |
|
разработанный фирмой Genentech |
|
|
|
61 |
|
|
|
|
|
продукты |
Нуклеозиды и нуклеотиды |
|
ВВЕДЕНИЕ. Уже более 100 лет в Японии известны |
||
|
||
Специальные |
вкусовые качества грибов, сушеной рыбы, некоторых |
|
водорослей и других природных продуктов, которые |
||
|
||
|
содержат 5'-нуклеотиды. Добавление очень неболь- |
|
|
ших количеств 5'-нуклеотидов (0,0005–0,001%) и |
|
|
глутамата натрия в супы, соусы и другие блюда при- |
|
|
водит к улучшению вкуса пищи и позволяет удалить |
|
|
неприятные привкусы, например привкус продуктов |
|
|
после хранения в металлической таре. Интересно, |
|
|
что свойством изменять вкус пищи обладают только |
|
|
инозин-5'-монофосфат, гуанозин-5'-монофосфат и |
|
|
ксантин-5'-монофосфат (ИМФ, ГМФ и КМФ соот- |
|
|
ветственно), в то время как аденозин-5'-монофос- |
|
|
фат, его 2'-, 3'-изомеры, 5'-дезоксирибонуклеотиды |
инуклеозиды в этом отношении инертны. С 1960 г. производство 5'-ИМФ и 5'-ГМФ достигло промышленных масштабов и в настоящее время составляет несколько тысяч тонн в год. Предприятия-изготови- тели этих веществ расположены главным образом в азиатских странах.
СПОСОБ ПРОИЗВОДСТВА. Наиболее распространенными способами производства 5'-ИМФ и 5'-ГМФ являются ферментативный гидролиз РНК и ферментация.
ФЕРМЕНТАТИВНЫЙ ГИДРОЛИЗ РНК. Наиболее доступным источником ДНК и РНК являются дрожжи. Так, в среде с пониженным отношением С/N (меласса и отходы целлюлозной промышленности) содержание РНК в клетках дрожжей Candida utilis на ранних стадиях роста достигает 10–15% сухой массы и может быть еще выше при добавлении в среду Zn2+
ифосфатов. Дрожжи культивируют в аэробных условиях в эрлифтных биореакторах. После отделения клеточной массы РНК экстрагируют горячим щелочным раствором поваренной соли (5–20% NaCl, 100 °С) 8 ч. Затем РНК осаждают, добавляя HCl или этанол. Ферментативный гидролиз РНК осуществляет нуклеаза P1, выделенная из Penicillium citrinum или Streptomyces aureus и предварительно очищенная от неспецифических 5'-нуклеозидаз и фосфатаз. 5'-ИМФ и 5'-ГМФ из гидролизата выделяют адсорбцией на активированном угле, ионообменной хроматографией и осаждением метанолом.
ПОЛУЧЕНИЕ 5'-ИМФ. Классическим способом получения 5'-ИМФ является выделение инозина из клеток Bacillus sp. и других грамположительных бактерий. Инозин, который накапливается в среде роста, может быть отделен от других компонентов осаждением при рН 11. Использование ауксотрофных по аденину мутантов, в которых методами генетической инженерии увеличена проницаемость клеточной мембраны, при оптимальных условиях ферментации позволяет получать до 35 г/л инозина. Перекристал-
62 лизованный инозин при переработке раствором PCl3
в триалкилфосфате наконец превращается в 5'-ИМФ. Однако в настоящее время 5'-ИМФ чаще всего получают с помощью мутантных штаммов
Corynebacterium ammoniagenes, которые выделяют этот продукт во внеклеточное пространство. Штам- мы-суперпродуценты обладают целым рядом особенностей, отличающих их от клеток дикого типа: в них блокирован процесс расщепления 5'-ИМФ, они нечувствительны к концентрации Mn2+ в среде, а, кроме того, их плазматическая мембрана является более проницаемой для 5'-ИМФ. Особенно высокие выходы продукта (до 30 г/л) были получены при использовании клеток, в геном которых клонированы несколько копий гена PRPP-трансферазы – ключевого фермента синтеза 5'-ИМФ.
ПОЛУЧЕНИЕ 5'-ГМФ. Самым распространенным способом получения 5'-ГМФ является синтез 5-амино- 4-имидазолкарбоксиамид-1-рибозид-5'-фосфата (AICAR) в клетках штаммов Bacillus megaterium, ауксотрофных по пуринам, с последующим химическим превращением этого вещества в 5'-ГМФ. Другой метод производства 5'-ГМФ основан на использовании мутантных штаммов Bacillus, в которых блокирован процесс расщепления 5'-ГМФ и искусственно повышено содержание ксантинмонофосфатов. Выходы продукта достигают 40 г/л.
ДРУГИЕ НУКЛЕОТИДЫ. ATФ, цАМФ, NAD+/NADH, NADP+/NADPH, FAD и кофермент А широко используются в биохимических исследованиях. Как правило, их получают ферментацией с мутантными штаммами или в ферментативных реакциях веществ-предшест- венников, синтезированных химическим путем. Например, NAD+ и кофермент А образуются в результате ферментации в клетках мутантных штаммов Brevibacterium ammoniagenes с выходом продукта до 2 г/л.
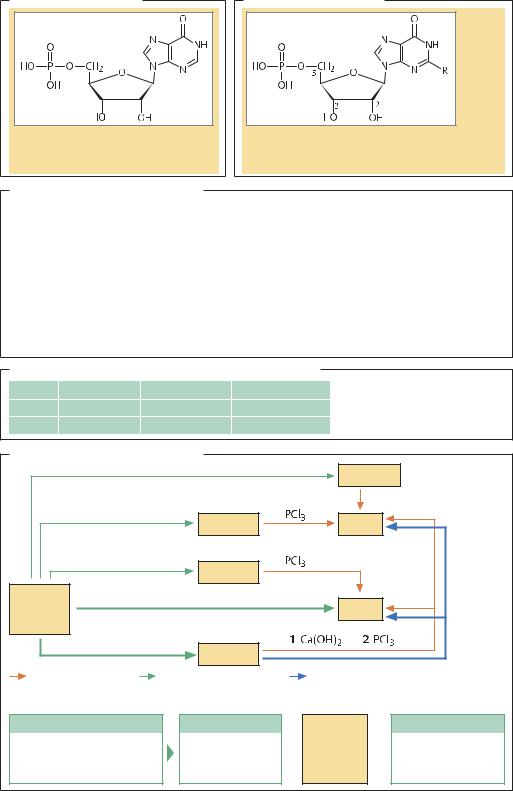
Инозин-5'-монофосфат |
|
С10Н13N4O6P |
|
MR |
348,21 |
Код CAS |
131-99-7 |
Получение и объемы производства |
|
Гуанозин-5'-монофосфат |
|
|
||
R = NH2: гуанозин-5'-монофосфат (5'-ГМФ) |
|
|||
С10Н14N5O8P |
MR |
363,22 |
Код CAS |
85-32-5 |
R = OH: ксантин-5'-монофосфат |
|
|
||
Нуклеозид |
Объем |
Способ получения |
Применение |
|
производства, |
|
|
|
т/год |
|
|
5'-ИМФ |
2000 |
Ферментативный гидролиз РНК из дрожжей, Усилители вкуса |
|
5'-ГМФ |
1000 |
ферментация инозина/гуанозина и их |
|
|
|
фосфорилирование; прямое получение |
|
|
|
5'-ИМФ ферментацией |
|
Инозин |
25 |
Ферментация |
Медицина |
Оротовая кислота |
20 |
Ферментация |
Терапия заболеваний печени |
Аденин, |
22 |
Ферментация |
Медицина |
аденозин, АТФ |
|
|
|
|
|
|
|
Содержание ДНК и РНК в различных микроорганизмах |
|
|
|
||||
|
Бактерии |
|
Дрожжи |
Грибы |
|
|
|
ДНК* |
0,37–4,5 |
|
0,03–0,52 |
0,15–3,3 |
|
* % сухой массы |
|
|
|
|
|
|
|
||
РНК** |
5–25 |
|
2,5–15 |
0,7–28 |
|
** из них 75–80% рРНК |
|
Синтез нуклеотидов и нуклеозидов |
|
|
|
|
|||
|
|
|
Bacillus и другие |
|
5'-Ксантин- |
|
|
|
|
|
|
|
монофосфат |
||
|
|
|
|
|
|
Bacillus subtilis |
|
|
Bacillus megaterium |
|
|
5'-ГМФ |
|
||
|
|
|
AICAR* |
|
|
|
|
|
Corynebacterium ammoniagenes, |
|
|
|
|
||
|
Bacillus subtilis |
|
Инозин |
|
|
|
Нуклеаза Р1 |
|
|
|
|
|
|
из Penicillium |
|
|
|
|
|
|
|
|
|
Меласса, |
|
|
|
|
|
citrinum |
|
Corynebacterium ammoniagenes |
|
|
|
|
|||
гидролизат |
|
|
5'-ИМФ |
|
|||
|
|
|
|
|
|||
крахмала |
|
|
|
|
|
|
|
|
Candida utilis |
рРНК |
|
|
|
|
|
|
|
|
|
|
|
|
|
Химический синтез |
|
Ферментация |
|
Использование ферментов |
|||
* AICAR: 5-амино-4-имидазолкарбоксамид-1-рибозид-5'-фосфат |
|
|
|
||||
|
Ферментация |
|
Выделение |
|
|
|
Химический синтез |
Штаммы-суперпродуценты |
Осаждение |
|
Более 30 г/л |
Из 5'-ИМФ: PCl3 |
|||
|
инозина |
|
|||||
C. ammoniagenes; |
|
при рН 11; |
|
после 42 ч |
в триалкилфосфате, |
||
гидролизат крахмала, |
|
перекристаллизация |
выход более 90% |
||||
|
ферментации |
||||||
неочищенная РНК; рН 6, 30 °С |
|
|
|
||||
|
|
|
|
|
|||
|
|
|
|
|
|
|
63 |
Специальные продукты
64
Биодетергенты и биокосметика
ВВЕДЕНИЕ. Некоторые микроорганизмы в присутствии алканов, в частности в растительных маслах, или на сахаросодержащем субстрате способны синтезировать поверхностно-активные вещества (ПАВ), которые называются биосурфактантами или биодетергентами. В отличие от синтетических ПАВ, производство которых достигает нескольких миллионов тонн в год, весьма дорогостоящие биодетергенты пока находят ограниченное применение, несмотря на то что эти ПАВ проявляют очень высокую биологическую активность и легко разлагаются в природной среде. В настоящее время активно проводят исследования этих веществ с целью их применения для очистки почв и воды; их можно, по-ви- димому, добавлять также в косметические кремы (биокосметика). Все косметические средства, которые получают (полностью или частично) из природных источников, имеют общее название «биокосметика». Методами биотехнологии получают природный краситель шиконин, а также теперь уже широко известный компонент кремов гиалуроновую кислоту.
БИОДЕТЕРГЕНТЫ (ПАВ) синтезируются многими микроорганизмами – прокариотами и эукариотами в присутствии насыщенных углеводородов и в растительных маслах. Хорошо изучены сложные эфиры сахаров и жирных кислот из бактерий: рамнолипиды и трегалолипиды, липопептид сурфактин и гетерополисахарид эмульзан. Из биодетергентов лучше всего изучен софоролипид из дрожжей. Этот гликолипид представляет собой смесь кислоты и лактона и образуется при культивировании клеток дрожжей Torulopsis bombicola в присутствии триглицеринов с выходом более 400 г/л. Переработку культуральной среды выгодно производить сразу по окончании ферментации. Высокоструктурированные синтетические неионные детергенты могут давать коллоидные растворы (это свойство характеризуется специальным параметром – критической концентрацией мицеллобразования, ККМ). В Японии софоролипиды в небольших количествах добавляют в косметические средства по уходу за кожей. Другим перспективным направлением применения биодетергентов является их использование для очистки почв от продуктов нефтепереработки. Соединения с поверхностно-активными свойствами образуются микроорганизмами в присутствии алканов или триглицеринов: например, головневый гриб Ustilago maydis синтезирует целлобиолипид, некоторые представители псевдомонад – рамнолипид, а Rhodococcus erythropolis – тетраэфир трегалозы. В некоторых случаях состав ацильной группы в молекулах гликолипидов зависит от природы алкана или триглицерина в среде роста. Эмульзан – полианионный гетерополисахарид (липополисахарид), который синтезируют клетки Acinetobacter calcoaceticus в присутствии триглицеринов, его выделяют экстракцией
органическими растворителями. Эмульзан проявляет поверхностно-активные свойства на границе раздела воды и нефти и поэтому используется в качестве эмульгатора для уменьшения вязкости нефти. Добавление небольших количеств эмульзана к нефти значительно увеличивает скорость транспорта нефти по нефтепроводам, кроме того, эмульзан используют при очистке нефтедобывающего оборудования и танкеров. Клетки Bacillus subtilis после добавления в среду роста гидрофобных соединений-индукторов синтезируют до 110 мг/л сурфактина – ацетилированного гептапептида с низкой способностью к мицеллообразованию (большое значение критической концентрации мицеллообразования, ККМ). Сурфактин не может назначаться как медицинский препарат из-за своей гематотоксичности. Ни один из биодетергентов не получен с таким высоким выходом, как для софоролипидов.
ШИКОНИН – производное нафтохинона, пигмент лепестков редкого наземного растения воробейника краснокорневого (Lithospermum erythrorhizon). В медицине это вещество используют как противовоспалительное средство, а также описаны случаи его успешного применения в противоопухолевой терапии. В промышленных масштабах шиконин получают из культур растительных клеток. В зависимости от того, соли какого металла добавляют в среду роста, образуется пигмент шиконин с различными оттенками. Это свойство активно используется японскими косметическими фирмами, например, при производстве губной помады.
ГИАЛУРОНОВАЯ КИСЛОТА. По химической природе гиалуроновая кислота – глюкозоаминогликан с молекулярной массой ~107 Да. Этот вязкоэластичный полисахарид входит в состав стекловидного тела глаза, суставной жидкости и связок костей. В промышленности гиалуроновую кислоту получают из пуповины сельскохозяйственных животных или из петушиных гребней. Кроме того, это вещество можно производить ферментацией с генетически модифицированными штаммами Streptococcus equi или S. zooepidemicus. Выход продукта достигает 6 г/л уже через 20 ч ферментации. Молекулы гиалуроновой кислоты образуют в воде структуру, напоминающую сетку, поэтому этот продукт иногда называют молекулярной губкой. Даже 2%-й раствор гиалуроновой кислоты в воде желируется, так прочно взаимодействуют молекулы воды и гиалуроновой кислоты. Это свойство гиалуроновой кислоты находит применение в косметологии: раствор гиалуроновой кислоты хорошо ложится на кожу, образуя пленку, которая активно всасывает влагу из воздуха, препятствуя дегидратации кожи – основной причине возникновения морщин. В медицине гиалуроновая кислота используется прежде всего в пластической хирургии.