Материал: Шмид Р. Наглядная биотехнология и генетическая инженерия
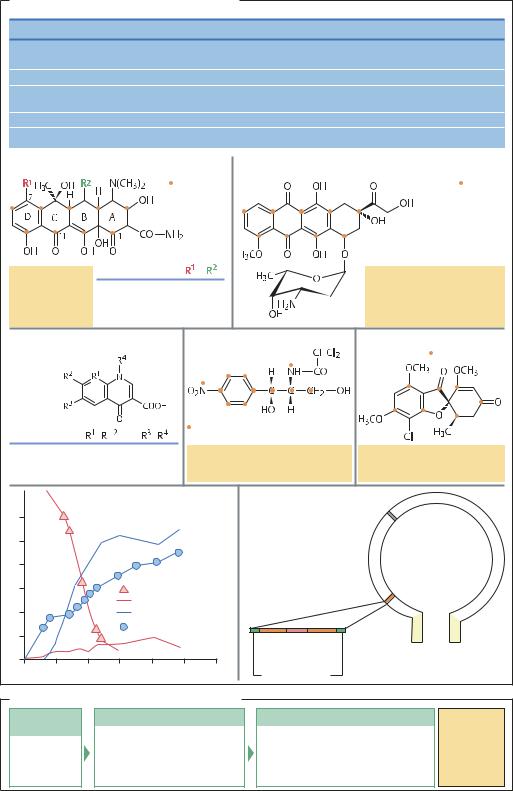
Хиноидные и ароматические антибиотики |
|
|
|
|
|
||||||||
|
|
|
|
Продуцент |
|
|
Применение |
|
|
|
|
||
(Хлор-)тетрациклин |
Streptomyces aureofaciens |
Антибиотик широкого спектра действия; |
|||||||||||
Окситетрациклин |
|
Streptomyces rimosus |
используется в медицине и ветеринарии |
||||||||||
Антрациклины |
|
|
S. peucetius |
|
|
Терапия онкологических заболеваний |
|||||||
Хинолоны |
|
|
Химический синтез |
Антибиотик широкого спектра действия; |
|||||||||
|
|
|
|
|
|
|
|
|
используется в медицине и скотоводстве |
||||
Хлорамфеникол |
|
Химический синтез |
Антибиотик широкого спектра действия |
||||||||||
Гризеофульвин |
|
|
Penicillium griseofulvum |
Борьба с грибковыми заболеваниями растений |
|||||||||
Тетрациклины |
|
|
|
|
|
|
Доксорубицин – представитель антрациклинов |
||||||
|
|
|
|
|
|
С1 из |
|
|
|
|
|
С1 из |
|
|
|
|
|
|
|
ацетата |
|
|
|
|
ацетата |
||
Хлортетрациклин |
|
|
|
|
|
|
|
С27Н29NO11 |
|
|
|||
С22Н23ClN2O8 |
|
Тетрациклин |
|
H |
|
H |
|
MR |
|
543,53 |
|||
MR |
478,89 |
Хлортетрациклин |
Cl |
H |
|
Tпл |
|
204–205 °С |
|||||
Код CAS |
57-62-5 |
Окситетрациклин |
H |
|
OH |
|
Код CAS |
23214-92-8 |
|||||
Налидиксовая кислота |
|
|
Хлорамфеникол |
Гризеофульвин |
|
||||||||
и ципрофлоксацин – хинолиновые |
|
|
|
|
|
|
|
С1 из ацетата |
|||||
антибиотики |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
из р-Аминофенилаланина |
|
|
|
|
||
Налидиксовая |
N |
СН3 |
Н |
СН3 |
|
С11Н12Cl2N2O5 |
С17Н17ClO2 |
|
|
||||
кислота |
|
|
|
|
|
|
|
|
|||||
ЦипрофлоксацинCH С4Н9N2 |
F |
С3Н5 |
MR |
323,13 |
Код CAS 56-75-7 |
MR |
352,77 |
Код CAS 126-07-8 |
|||||
|
|
|
|
|
|
|
|
|
|
ori |
|
|
|
мг/л |
|
|
|
|
|
|
|
|
|
|
Streptomyces |
||
|
|
|
|
|
|
|
|
|
|
|
rimosus |
||
Концентрация, |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
Хлортетрациклин |
Кластер генов, |
|
Линейная хромосома |
|||||||
|
|
|
|
|
|
|
|
|
участвующих |
|
~ 8 млн п.н., |
||
|
|
|
|
Хлорид |
|
|
|
в биосинтезе |
|
Содержание GC ~71% |
|||
|
|
|
|
Тетрациклин |
|
|
окситетрациклина |
|
|
|
|
||
|
|
|
|
|
|
(~ 30 т.п.н.) |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Объем мицелия |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
Поликетидсинтаза |
|
Hестабильные |
||
|
|
|
|
|
|
|
|
|
|
|
|||
0 |
20 |
40 |
60 |
80 |
|
100 |
|
120 ч |
Гены |
|
теломерные участки |
||
|
|
устойчивости |
|
(~ 550 т.п.н.) |
|||||||||
Ферментация и очистка хлортетрациклина |
|
|
|
|
|
||||||||
Предфер- |
|
|
Биореактор |
|
|
Выделение и очистка |
|
Выход |
|||||
ментация |
|
Объем до 150 м3, сахароза, |
Удаление мицелия при пропускании |
||||||||||
|
продукта |
||||||||||||
|
|
|
|||||||||||
Штамм-супер- |
|
жидкий кукурузный экстракт, |
культуры через фильтровальный пресс |
~ 10 г/л |
|||||||||
продуцент |
|
соли, аэрация с интенсивностью |
или сепаратор; многостадийная |
|
после 140 ч |
||||||||
Streptomyces |
|
1 объем реактора/мин, |
|
экстракция н-бутилацетатом, очистка |
ферментации |
||||||||
aureofaciens |
|
28 °С, рН 5,8–6,0; 60–65 ч |
ионообменной хроматографией |
|
55 |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Антибиотики
Поликетидные антибиотики
ВВЕДЕНИЕ. К этой обширной группе относятся макро- |
рые синтезируются только дрожжами и грибами. Та- |
||
лидные, полиеновые, макротетролидные и ансамици- |
ким образом, антибиотики класса полиенов не эффе- |
||
новые антибиотики. Общим в их структуре является |
ктивны в борьбе с бактериями. Амфотерицин В и ни- |
||
наличие макроциклического лактонового или лактам- |
статин используются при грибковой инфекции |
||
ного кольца, которое образуется из длинной цепи ос- |
Candida albicans, а пимарицин – в производстве сыра |
||
татка полигидроксижирной кислоты с концевой гид- |
в качестве консерванта. Полиеновые антибиотики об- |
||
роксильной или |
аминогруппой. |
Циклическая |
ладают нефро- и гепатотоксичными свойствами, поэ- |
молекула может содержать остатки редких сахаров |
тому их применяют только при тяжелых заболевани- |
||
(макролидные антибиотики), ароматические хромо- |
ях. Химическая лабильность этих антибиотиков не |
||
форные группы (ансамицин), участки, представляю- |
позволяет использовать их в качестве противогриб- |
||
щие собой диены (полиеновые антибиотики) или |
кового средства для защиты растений. |
||
иметь структуру полилактона (макротетролидные ан- |
АНСАМИЦИН – это макролактамный антибиотик, со- |
||
тибиотики). Большинство поликетидных антибиоти- |
держащий молекулу ароматического хромофора. |
||
ков образуются в клетках стрептомицетов как вторич- |
Важнейший заменитель ансамицина – рифамицин – |
||
ные метаболиты. |
Препараты |
поликетидных |
синтезируется в Amycolatopsis mediterranei. Оба они |
антибиотиков применяются в медицине, животновод- |
эффективно действуют против грамположительных |
||
стве и пищевой промышленности. Объем рынка мак- |
бактерий и микобактерий. Рифампицин – полусинте- |
||
ролидных антибиотиков медицинского назначения в |
тический антибиотик, в настоящее время является |
||
2004 г. составил 5,7 млрд долл. США. |
важнейшим препаратом, используемым для лечения |
||
МАКРОЛИДНЫЕ АНТИБИОТИКИ – это липофильные |
туберкулеза (возбудитель – Mycobacterium tubercu- |
||
вещества с сильновыраженными основными свойства- |
losis) и проказы. Механизм действия рифампицина |
||
ми. Они представляют собой 10–60-членные макро- |
заключается в связывании β-субъединицы ДНК-за- |
||
циклические лактоны. Синтез этих молекул происхо- |
висимой РНК-полимеразы бактерий. Таким образом, |
||
дит в ходе повторяющихся циклов конденсации |
антибиотик препятствует процессу транскрипции в |
||
аналогично синтезу длинноцепочечных жирных кис- |
бактериальной клетке. Связывания рифампицина с |
||
лот: наращивание цепи происходит в реакциях, катали- |
эукариотическими РНК-полимеразами не происхо- |
||
зируемых поликетидсинтазой. Макролидные антибио- |
дит, поэтому антибиотик успешно используется для |
||
тики слаботоксичны, поэтому их применяют в |
лечения человека. Устойчивость некоторых штаммов |
||
педиатрии. Механизм действия заключается в ингиби- |
к действию рифампицина вызвана изменениями |
||
ровании синтеза белка в клетках грамположительных |
структуры РНК-полимеразы в результате мутаций. |
||
микроорганизмов: молекула антибиотика связывается |
ФЕРМЕНТАЦИЯ И ОЧИСТКА. Для промышленного |
||
с 50S-субъединицей бактериальной рибосомы, что |
производства поликетидных антибиотиков осуществ- |
||
препятствует процессу транслокации растущей поли- |
ляют ферментацию в биореакторах большого объема |
||
пептидной цепи. Устойчивость некоторых штаммов к |
с использованием штаммов-суперпродуцентов. Так, |
||
действию макролидных антибиотиков связана с мети- |
для получения эритромицина применяют штамм Sac- |
||
лированием 23S-рРНК: вероятно, из-за этого не про- |
charopolyspora erythraea (прежнее название – Strep- |
||
исходит связывания молекулы антибиотика с рибосо- |
tomyces erythreus), позволяющий получать до 7 г |
||
мой. Азитромицин, кларитромицин, эритромицин и |
продукта с литра среды после 72 ч ферментации. Ан- |
||
спирамицин используют для лечения бактериальных |
тибиотики выделяются во внеклеточную среду, |
||
инфекций дыхательных путей. Структурно сходный ти- |
откуда их экстрагируют с помощью растворителей, |
||
лозин благодаря своей высокой эффективности был |
а затем очищают хроматографическими методами. |
||
использован против микоплазмоза как добавка к кор- |
|
||
му свиней, что привело к его запрету в странах ЕС (но |
|
||
не в США) из-за высокого риска развития устойчиво- |
|
||
сти патогена. |
|
|
|
ПОЛИЕНОВЫЕ АНТИБИОТИКИ – продукты вторичного метаболизма стрептомицетов; в молекуле этих антибиотиков имеется 26–38-членное лактоновое кольцо, в которое встроена 3–7-членная молекула диена. Диены могут содержать различные боковые группы, в частности остатки аминосахаров, присоединенные гликозидной связью. Действие полиеновых антибиотиков объясняется их взаимодействием с микостеро-
56 лами (например, эргостеролом) – веществами, кото-
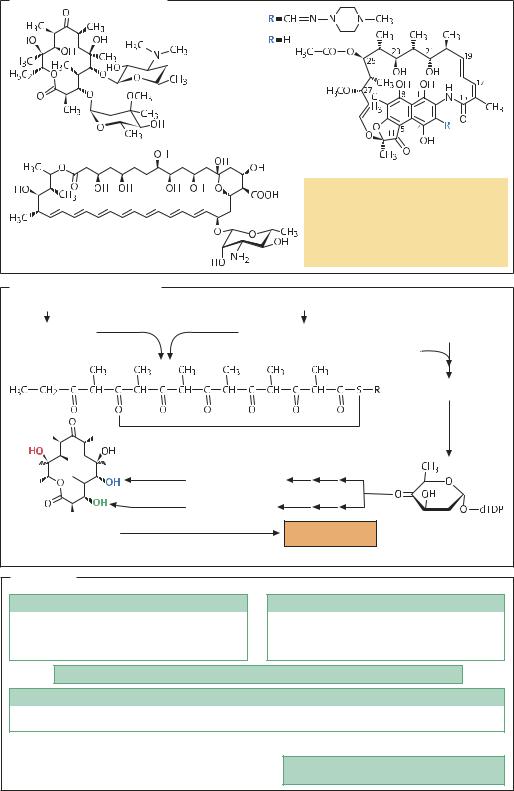
Поликетидные антибиотики |
|
|
|
|
|
|
||
а |
|
|
|
б Рифампицин |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
в Рифамицин |
|
|
|
|
Эритромицин |
|
|
|
|
|
|
|
|
г |
|
|
|
|
|
|
|
|
|
|
|
|
|
a С37Н67NO13 |
б С43Н58N4O12 |
||
|
|
|
|
|
MR |
733,94 |
MR |
822,95 |
|
|
|
|
|
Код CAS 114-07-8 |
Код CAS 13292-46-1 |
||
|
|
|
|
|
в С37Н47NO12 |
г С47Н73NO17 |
||
|
|
|
|
|
MR |
697,78 |
MR |
924,09, |
|
Амфотерицин В |
|
|
Код CAS 6998-60-3 |
Код CAS 1397-89-31 |
|||
|
|
|
|
|
|
|
||
Биосинтез эритромицина А |
|
|
|
|
|
|
||
1 × пропионовая кислота |
|
|
|
6 × сукцинил-KоА |
|
|
||
1 × пропионил-KоА |
|
|
|
6 × 2-метилмалонил-KоА |
2 × D-глюкоза |
|||
|
|
|
|
|
|
2 × дТТФ* |
|
|
|
|
|
|
|
|
|
2 × дТДФ-глюкоза |
|
Гидрокси- |
|
|
|
|
|
|
|
|
лирование |
|
Поликетид, связанный с ферментом |
|
|
|
|||
|
|
|
(предполагаемая стадия) |
|
|
|
||
|
|
Гликози- |
|
дТДФ-D-дезозамин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
лирование |
дТДФ-L-микароза |
|
|
|
||
|
|
|
|
|
|
|
||
Эритромицин С |
|
|
|
Эритромицин А |
2 × дТДФ-4-оксо- |
|||
|
|
|
6-дезокси-D-глюкоза |
|||||
|
|
Метилирование микарозы |
|
|||||
|
|
|
|
|
||||
* дТТФ – дезокситимидинтрифосфат |
|
|
|
|
|
|
||
Получение |
Эритромицин |
|
|
|
Рифамицин/Рифампицин |
|
||
|
|
|
|
|
||||
|
Ферментация |
|
|
|
Ферментация |
|
||
Штамм-суперпродуцент Saccharopolyspora erythrаea, |
Штамм-суперпродуцент Amycolatopsis mediterranei, |
|||||||
непрерывная ферментация в биореакторе объемом |
непрерывная ферментация в биореакторе объемом |
|||||||
более 120 м3, глюкоза, соевая мука, микроэлементы, |
более 120 м3, глюкоза, соевая мука, микроэлементы, |
|||||||
0,2–0,5% пропанол, 33 °С, 70–120 ч |
|
|
0,2–0,5% пропанол, 33 °С, 70–120 ч |
|
||||
Отделение клеточной массы с помощью фильтровального пресса или в сепараторах |
||||||||
Выделение и очистка
Экстракция в противотоке уксуснокислого эфира масляной кислоты, хроматографические методы, перекристаллизация
Выход продукта ~ 7 г/л эритромицина после 72 ч |
|
Выход продукта ~ 7 г/л рифамицина после 72 ч |
|
|
|
Четырехстадийный синтез рифампицина
по методу Манниха
57
Антибиотики
58
Получение новых антибиотиков
ВВЕДЕНИЕ. Несмотря на значительные успехи медицины, связанные с использованием антибиотиков, и большое число новых лекарств, обладающих антибиотическим действием, в современном мире распространяются инфекционные заболевания, уже считавшиеся полностью побежденными, например туберкулез, стрептококковые и стафилококковые инфекции. Появление новых форм возбудителей заболеваний объясняется возникновением устойчивости микроорганизмов к используемому антибиотику (антибиотикам). Гены, обеспечивающие такую устойчивость, распространяются посредством плазмид и/или транспозонов; таким образом возможна передача генетического материала как между сходными (при конъюгации), так и между различными (при фаговой инфекции) организмами. Важной проблемой при поиске новых антибиотиков, как правило, является их высокая токсичность для человека. Грибы, дрожжи и простейшие – эукариоты, и для них характерны общие для эукариот особенности обмена веществ, поэтому большинство веществ, токсичных для этих возбудителей заболеваний, оказываются токсичными и для человека. Очевидно, что актуальность задачи создания новых антибиотиков не ослабевает.
НОВЫЕ СТРАТЕГИИ СКРИНИНГА. Использование классического метода скринига, в частности с применением биочипов, приводит к тому, что из 10 проанализированных веществ 9 имеют новую, ранее неизвестную структуру, но вовсе не обязательно новые свойства. Таким образом, очевидна необходимость разработки новых подходов к поиску веществ, обладающих антибиотическим действием. Приведем несколько примеров принципиально новых стратегий.
а) «Биосинтез, направляемый предшественником» – полусинтетический метод, при котором в среду роста микроорганизма-продуцента добавляют вещества-предшественники антибиотика.
б) Скрининг среди малоизученных микроорганизмов, например миксобактерий, редких актиномицетов, лишайников или губок.
в) Усовершенствование технологии микрочипов. г) Поиск промежуточных продуктов биосинтеза
антибиотиков.
д) Осуществление генетической рекомбинации между различными продуцентами антибиотиков.
е) Поиск предшественников антибиотиков методами «обратной генетики».
ж) Осуществление рекомбинации генов – участников биосинтеза антибиотиков в системе in vitro, и использование полученных ферментов в синтезе новых веществ in vivo (комбинаторный биосинтез).
з) Поиск новых мишеней действия антибиотиков на основе анализа генома патогенных микроорганизмов.
ОБРАТНАЯ ГЕНЕТИКА. Если в определенном организме установлена нуклеотидная последовательность гена фермента, участвующего в биосинтезе антибиотика, эта информация может послужить для поиска генов, кодирующих ту же ферментативную активность в геномной ДНК других организмов. Так была получена важная информация о взаиморасположении генов, ответственных за синтез макролидных антибиотиков.
КОМБИНАТОРНЫЙ БИОСИНТЕЗ. Примером может служить получение новых макролидных антибиотиков с измененными свойствами. Гены, кодирующие три фермента комплекса поликетидсинтазы, катализирующей наращивание углеродной цепи, организованы в виде кластера. Аналогичным образом расположены и гены ферментов, определяющих модификации поликетидной цепи. Клонирование всех этих генов позволило осуществить обмен генами между кластерами, и рекомбинантные ДНК в составе плазмид вновь были внесены в клетки организма-хозяина. Так было получено несколько новых макролидных антибиотиков, не найденных в природе и обладающих специфическими свойствами.
ПОИСК НОВЫХ МИШЕНЕЙ ДЛЯ ДЕЙСТВИЯ АНТИБИОТИКОВ МЕТОДАМИ ГЕНОМНОГО АНАЛИЗА. С каждым годом увеличивается число микроорганизмов, для которых нуклеотидная последовательность генома полностью известна. В качестве примера приведем несколько микроорганизмов – возбудителей заболеваний человека, геном которых в настоящее время секвенирован: Haemophilus influenzae
(1,83 млн п.н., хронический бронхит), Helicobacter pylori (1,67 млн п.н., язвенные заболевания), Borellia burgdorferi (0,91 млн п.н., бореллиоз), Mycobacterium tuberculosum (4,41 млн п.н., туберкулез), Treponema pallidum (1,14 млн п.н., сифилис), Chlamydia trachomatis (1,04 млн п.н., инфекционные заболевания глаз). Анализ генома позволяет выявлять особенности метаболизма или сигнальные пути, специфические для патогенного организма. Впоследствии эта информация может служить для создания антибиотиков, действующих на новые «мишени». Так, в настоящее время проводятся работы по созданию антибиотика, действующего против Helicobacter pylori: по данным геномного анализа предполагаемой мишенью действия этого нового антибиотика могут быть ферменты – участники обмена никеля в микроорганизме.
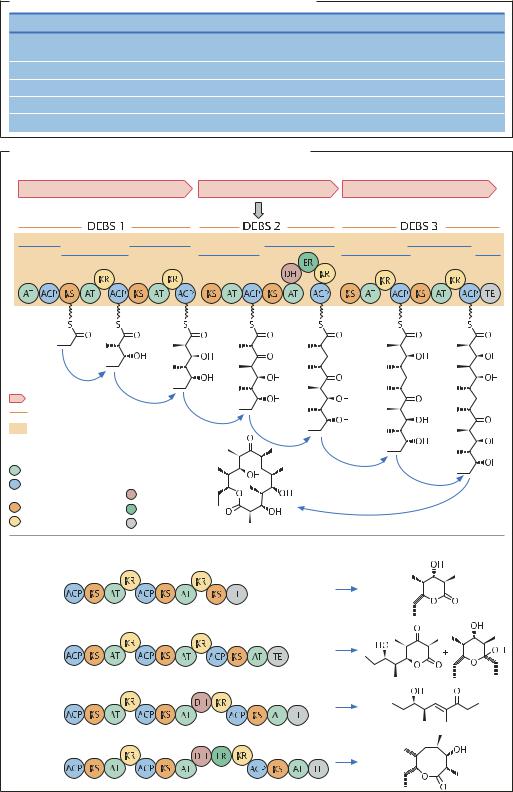
Вещества-предшественники в биосинтезе антибиотиков |
|
||
Антибиотик |
Продуцент |
Структурные элементы |
|
Пенициллины |
Penicillium chrysogenum |
Разнообразные алифатические, ациклические |
|
|
|
и ароматические карбоновые кислоты |
|
Цефалоспорин |
Acremonium chrysogenum |
S-Карбоксиметил-L-цистеин |
|
Блеомицин |
Streptomyces sp. |
Модифицированные амины |
|
Бацитрацин |
Bacillus licheniformis |
D-алло-Аминокислоты |
|
Стрептомицин |
Streptomyces griseus |
2-Дезоксистрептидин |
|
Комбинаторный биосинтез макролидных антибиотиков |
|
||
а Образование мультиферментного комплекса дезоксиэритронолид-В-синтазы (DEBS) 1–3 |
|||
Ген eryAI |
Ген eryAII |
Ген eryAIII |
|
|
|
Транскрипция и трансляция |
|
Начало |
Модуль 2 |
Модуль 4 |
Модуль 6 |
Модуль 1 |
Модуль 3 |
Модуль 5 |
Конец |
Генный кластер |
|
|
|
Мультиферментный комплекс |
|
|
|
Функциональные единицы |
|
|
|
мультиферментного комплекса |
|
|
|
Ацетилтрансфераза |
|
6-Дезоксиэритро- |
|
Белок – переносчик |
Дегидратаза |
нолид В (7) |
|
ацильной группы |
Замыкание |
||
Кетоацилсинтаза |
Еноилредуктаза |
кольца |
|
|
|
||
Кеторедуктаза |
Тиоэстераза |
|
|
б Многообразие вариантов, полученных методом комбинаторного биосинтеза |
Продукт |
||
|
|
|
|
|
|
Экспрессия, |
|
|
|
ферментация |
|
Вариант 1 |
|
|
|
Вариант 2 |
|
|
|
Вариант 3 |
|
|
|
Вариант 4 |
|
|
|
|
|
|
59 |