Материал: Определение характеристик макета БПК-биосенсора на основе дрожжей Debaryamyces hansenii, иммобилизованных в модифицированный ПВС с использованием различных синтетических сточных вод
Сy1 - то же, после инкубации, мг/дм3;- величина
разбавления.
2.7 Определение перманганатной
окисляемости
Определение перманганатной окисляемости проводили согласно ПНДФ [62]. Метод основан на окислении веществ, присутствующих в пробе воды, известным количеством перманганата калия в сернокислой среде при кипячении в течение 10 минут. Не вошедший в реакцию перманганат калия восстанавливают щавелевой кислотой. Избыток щавелевой кислоты оттитровывают раствором перманганата калия.
При определении перманганатной окисляемости после реакции должно оставаться не менее 40 % введенного перманганата калия, так как степень окисления зависит от его концентрации.
Для получения достоверных и сравнимых между
собой результатов необходимо строго придерживаться условий проведения анализа.
2.7.1 Подготовка дистиллированной воды
Перед использованием воду проверяют на отсутствие восстановителей. При холостом опыте расход раствора перманганата калия на титрование не должен превышать 0,5 см3, в противном случае следует провести процедуру очистки или использовать воду с меньшим содержанием органических соединений.
Для очистки от восстановителей к 1 дм3 дистиллированной воды добавляют 10 см3 серной кислоты (1:15) и небольшой избыток (до образования розового цвета) основного раствора перманганата калия, а затем перегоняют. Первую порцию дистиллята объемом 100 см3 отбрасывают. Перегнанную дистиллированную воду хранят в стеклянной бутыли со стеклянной пробкой.
Приготовление растворов вели согласно методике
прописанной в ПНДФ [62].
2.7.2 Выполнение измерений
В колбу помещают 100 см3 хорошо перемешанной пробы (при необходимости разбавленной дистиллированной водой до 100 см3), несколько капилляров или стеклянных шариков, приливают 5 см3 разбавленной серной кислоты (1:3) и 10 см3 раствора перманганата калия (0,01 моль/дм3 эквивалента). Смесь нагревают так, чтобы она закипела не позднее чем через 5 минут, и кипятят 10 ± 2 мин, закрыв маленькой конической воронкой для уменьшения испарения. Если в процессе кипячения содержимое колбы потеряет розовую окраску или побуреет, то определение надо повторить, разбавив исследуемую воду. К горячему раствору (80 - 90 °С) прибавляют 10 см3 раствора щавелевой кислоты (0,01 моль/дм3 эквивалента). Обесцвеченную горячую смесь титруют раствором перманганата калия (0,01 моль/дм3 эквивалента) до слабо-розового окрашивания. Если при титровании пробы расходуется перманганата калия более 60 % от добавленного количества, т.е. если при обратном титровании израсходовано более 7 см3 раствора титранта, то пробу разбавляют и повторяют определение.
Если при анализе предварительно разбавленной пробы на титрование расходуется менее 2 см3 раствора перманганата калия, то определение повторяют с менее разбавленной или неразбавленной пробой.
Холостое определение
Одновременно проводят холостой опыт со 100 см3
дистиллированной воды и обрабатывают ее так же, как анализируемую воду. Расход
раствора перманганата калия при холостом определении не должен превышать 0,5
см3. В противном случае проводят дополнительную очистку используемой
дистиллированной воды и посуды.
2.7.3 Обработка результатов эксперимента
Величину перманганатной окисляемости, выраженную
в мгО/дм3, рассчитывают по формуле:
![]()
где V1 - объем раствора перманганата калия (0,01 моль/дм3 эквивалента), израсходованного на титрование исследуемой пробы, см3;- объем раствора перманганата калия (0,01 моль/дм3 эквивалента), израсходованного на титрование холостой пробы, см3;- объем пробы, взятой для анализа (100), см3;- коэффициент разбавления пробы;
- эквивалент кислорода.
2.8 Результаты определения
перманганатной окисляемости и расчет величины разбавления
Для определения перманаганатной окисляемости проведено предварительное разбавление образцов браги. Образец №1 (до начала бражения) разбавлен в 500 раз, образец №2 (24 часа от начала брожения) - в 500 раз, образец №3 (48 часов от начала брожения) - в 500 раз, образец №4 (72 часа от начала брожения) разбавлен в 750 раз.
Расчет перманганатной окисляемости
![]() №1: 880 ± 90, мгО/дм3 (P = 0,95)
№1: 880 ± 90, мгО/дм3 (P = 0,95)
![]() №2:1500 ± 100, мгО/дм3 (P = 0,95)
№2:1500 ± 100, мгО/дм3 (P = 0,95)
![]() №3: 1600 ± 200, мгО/дм3 (P = 0,95)
№3: 1600 ± 200, мгО/дм3 (P = 0,95)
![]() №4: 480 ± 50, мгО/дм3 (P = 0,95)
№4: 480 ± 50, мгО/дм3 (P = 0,95)
Применяя то, что перманганатная окисляемость составляет 50% от ХПК, и остаточный кислород в кювете должен составлять 4-5 мг/л, то предварительное разбавление для определения БПК для образца №1 нужно провести в 200 раз. Образец №2 необходимо разбавить в 300 раз, образец №3 - в 350 раз, образец №4 нужно разбавить в 100 раз.
3. Обсуждение результатов
Анализ литературных данных показывает, что наиболее экспрессным методом определения БПК является метод на основе биосенсора. Для калибровки БПК-датчиков используют различные стандарты. В связи с этим, целью наших исследований был подбор оптимального стандарта для калибровки датчика БПК-биосенсора.
Для формирования рецепторного элемента сенсора использовали дрожжевой штамм Debaryamyces hansenii ВКМ Y-2482. Согласно литературным данным штамм обладает широкой субстратной специфичностью и способен окислять многие спирты, углеводы, аминокислоты и другие органические вещества [статьи про дрожжи]. Также штамм Debaryamyces hansenii устойчив к высоким концентрациям солей и к высокому осмотическому давлению. Данные особенности позволяют использовать данный штамм для анализа технологических сточных.
Формирование рецепторного элемента
проведено включением клеток микроорганизмов в гель модифицированного
поливинилового спирта (ПВС).
3.1 Определение характеристик макета
БПК-биосенсора на основе клеток Debaryamyces hansenii, иммобилизованных в
модифицированный ПВС на основе ГГС и ОЕСD
Операционная стабильность
Операционная стабильность является одной из важнейших характеристик биосенсора. Она показывает устойчивость ответа сенсора на одну и ту же концентрацию субстрата при проведении большого числа последовательных измерений и тесно связана с метрологической характеристикой сходимостью (повторяемостью).
Операционная стабильность сенсоров характеризуется относительным стандартным отклонением при многократном измерении стандартного образца и остаточной активностью (% от исходной) биосенсора после нескольких последовательных измерений в течение определенного периода времени.
Операционная стабильность на основе ГГС
Для определения операционной стабильности на основе ГГС было проведено 15 последовательных измерений ответа сенсора на 20 мкл 3 г/дм3 раствора глюкозо-глутаматной смеси (ГГС) (концентрация в кювете 19,9 мг/дм3). Смесь ГГС была выбрана, так как её применение как стандарта при анализе БПК определено в ПНДФ [61].
При введении субстрата в
измерительную ячейку микроорганизмы окисляют его. При этом возрастает
дыхательная активность клеток, и в приэлектродном пространстве снижается
концентрация кислорода, что регистрируется с помощью электрода Кларка (рис.13).
На монитор выводится графическое отображение изменения концентрации кислорода
от времени (рис. 14). По полученному отклику вычисляется ответ сенсора как
максимальная скорость изменения концентрации кислорода от времени (первая
производная).
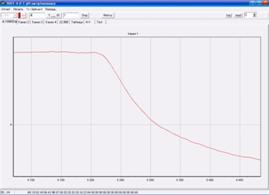
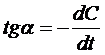
Рис. 14 - Ответ биосенсора на основе дрожжевого
штамма Debaryamyces hansenii, иммобилизованного в модифицированный ПВС на
добавление 35 мкл ГГС
Время между последовательными измерениями
составляло около 7 минут. Данные по операционной стабильности были получены на
четвертый день после иммобилизации. Результаты представлены на рисунке 15 и в
таблице 2
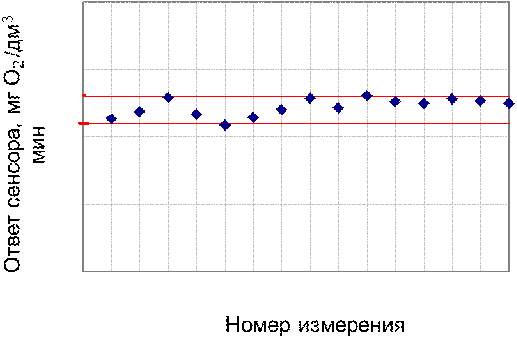
Рис. 15 - Операционная стабильность биосенсора
на основе иммобилизированных клеток Debaryamyces hansenii
Таблица 2 - Данные по операционной стабильности на основе ГГС
|
|
Стандартное отклонение S, мг/(дм3∙мин) |
Относительное стандартное отклонение Sr, % |
|
Обсчет в ручную |
6,611∙10-3 |
2,4 |
|
Обсчет в Excel |
6,611∙10-3 |
2,4 |
Операционная стабильность на основе OECD
Для определения операционной стабильности на
основе ГГС было проведено 15 последовательных измерений.
Таблица 3 - Данные по операционной стабильности на основе ОЕСD
|
|
Стандартное отклонение S, мг/(дм3∙мин) |
Относительное стандартное отклонение Sr, % |
|
Обсчет в ручную |
5,332∙10-3 |
2,7 |
|
Обсчет в Excel |
5,332∙10-3 |
2,7 |
Данные операционной стабильности представлены на
рис. 16
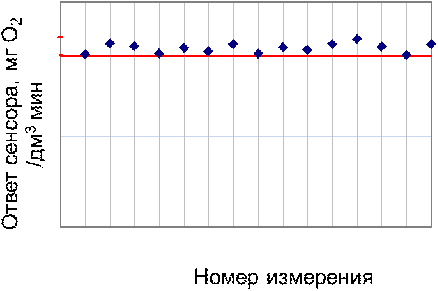
Рис. 16 - Операционная стабильность биосенсора
на основе иммобилизованных клеток Debaryamyces hansenii
Как видно из графиков ответы изучаемых биорецепторов оставались стабильными на протяжении всех 15 измерений. Стандартное отклонение, рассчитанное с помощью двух программ и вручную (приложение 1), составило 6,611∙10-3 мг/(дм3∙мин) на основе ГГС, относительное стандартное отклонение - 2,4%, среднее значение равняется 0,272 ±0,004 мг/(дм3∙мин). С использованием стандарта ОЕСD стандартное отклонение составило 5,332∙10-3 .относительное стандартное отклонение - 2,7%, среднее значение равняется 0,198 ±0,003 мг/(дм3∙мин).
Устойчивость ответа сенсора на одну и ту же концентрацию субстрата с использованием двух стандартов составляет менее 3% и различается незначительно.
Долговременная стабильность на основе ГГС
Долговременная стабильность является характеристикой самого рецепторного элемента. Она зависит от природы биомассы и от способа иммобилизации клеток. Долговременная стабильность характеризует устойчивость работы сенсора в течение длительного периода времени.
Долговременную стабильность определяли путём
ежедневного определения величины ответа сенсора на одну и ту же концентрацию
раствора глюкозо-глютаматной смеси (рис. 17). Между измерениями сенсор хранился
в буферном растворе при температуре 20 ºС.
За время стабильной работы рецепторного элемента принимали время, в течение
которого величина сигнала составляла не менее 30% от начальной. Для определения
долговременной стабильности микробных сенсоров использовали ГГC тех же
концентраций, что и для определения операционной стабильности. За 100%
принимается ответ биосенсора в первый день измерений.
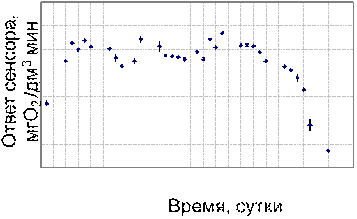
Рис. 17 - Долговременная стабильность биосенсора
на основе дрожжевого штамма Debaryamyces hansenii
В первый день после формирования рецепторного элемента дорожи D. hansenii иммобилизованные в модифицированный поливиниловый спирт имеют низкую активность. К четвертому дню активность возрастает (на %) что можно объяснить адаптацией микроорганизмов к изменившимся условиям внешней среды. К пятому дню дыхательная активность иммобилизованных дрожжей стабилизируется. Высокая активность клеток D. hansenii сохраняется до 36 дня посли формирования рецепторного элемента. К 43 дню активность дрожжей упала на 21 % от первоначальной, а к 46 дню снизилась до 75 %. Таким образом долговременная стабильность рецепторного элемента на основе дрожжей Debaryamyces hansenii иммобилизованных в модифицированный ПВС составила 43 дня.
Определение зависимости ответа биосенсора от концентрации
Для получения количественной информации о содержании анализируемых веществ в образце необходимо знать калибровочные характеристики биосенсора, то есть зависимость аналитического сигнала от концентрации в случае использования ГГС - стандарта, и зависимость аналитического сигнала от БПК в случае ОЕСD - стандарта. Поэтому градуировочная зависимость ответа сенсора от концентрации (БПК) определяемого вещества является важнейшей метрологической характеристикой.
Зависимость ответа сенсора от концентрации на основе ГГС
По полученным экспериментальным данным была
построена градуировочная зависимость отклика биосенсора от концентрации ГГС в
измерительной кювете.
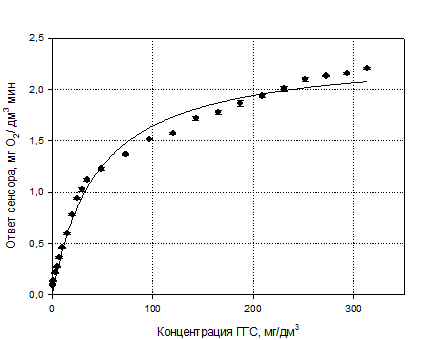
Рис. 18 - Зависимость ответа сенсора
от концентрации субстрата
Биорецепторы на основе целых клеток
микроорганизмов относятся к каталитическому типу, т.е. биологический ответ в
таких системах обеспечивается ферментативными реакциями микроорганизмов.
Поэтому зависимость, приведенная на рис. 18 хорошо описывается уравнением типа
Михаэлиса-Ментен:
![]() , где
, где
- максимальная скорость потребления кислорода иммобилизованными микроорганизмами, при которой все молекулы фермента участвуют в образовании фермент-субстратного комплекса. Достигается при [S]→∞; - скорость.
КM - эффективная константа Михаэлиса численно равна концентрации субстрата, при которой скорость ферментативной реакции достигает половины максимального значения (R=Rmax/2).
Была произведена аппроксимация
зависимости ответа сенсора от концентрации субстрата с помощью уравнения
Михаэлиса - Ментен. Параметры были рассчитаны с помощью программы Sigma Plot
(см. приложение 2). Параметры уравнения для биосенсоров на основе используемых
штаммов приведены в таблице 3.
Таблица 4 - Параметры уравнения Михаэлиса - Ментен зависимости ответа сенсора от концентрации ГГС
|
Эффективная константа Михаэлеса К´М,мг/дм3 |
Максимальная скорость потребления кислорода Rmax, мг/(мин∙дм3) |
Коэффициент смешанной корреляции R |
|
44±2 |
2,37±0,06 |
0,9936 |
Полученные зависимости величины ответа сенсора от концентрации субстрата имеют гиперболический вид.
Согласно уравнению Михаэлиса - Ментен концентрация
субстрата будет пропорциональна отклику биосенсора только при концентрациях,
гораздо меньших KM. Тогда уравнение приобретает следующий вид:
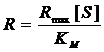
Для снижения ошибок анализа нередко ограничиваются использованием линейного участка градуировочной кривой.
Верхняя граница линейной зависимости была определена из уравнения Михаэлеса-Ментен. Численное значение верхней границы определяемых концентраций равно константе Михаэлеса, К´м. Итак, верхняя граница определяемых концентраций клеток Debaryamyces hansenii, иммобилизованных в модифицированный поливиниловый спирт, составляет 44±2 мг/дм3.
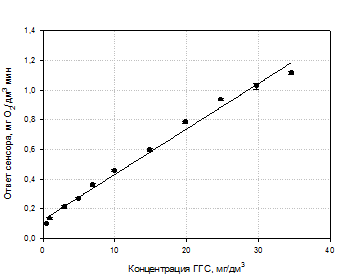
Далее были проведены дополнительные
опыты по определению зависимости ответа сенсора от концентрации субстрата на
линейном участке градуировочной прямой. По полученным данным построен график
зависимости ответа сенсора от концентрации ГГС. (рис. 19)