Материал: Определение характеристик макета БПК-биосенсора на основе дрожжей Debaryamyces hansenii, иммобилизованных в модифицированный ПВС с использованием различных синтетических сточных вод
В аэробных условиях круг усваиваемых субстратов шире: помимо углеводов в него входят также жиры, углеводороды, ароматические и одноуглеродные соединения, спирты, органические кислоты. Так ряд видов дрожжей рода Candida (Candida tropicalis, Candida intermedia, Candida lipolytica, Candida guilliermondii) отличается способностью к аэробному росту на длинноцепочечных жирных кислотах и алканах.
Если в анаэробных условиях лишь единичные виды дрожжей могут сбраживать пятиатомные сахара, то в присутствии кислорода пентозы (арабиноза, ксилоза и др.) и метилпентозы (рамноза) могут служить субстратами для очень многих дрожжей.
Довольно часто встречаются дрожжи, ассимилирующие крахмал. Более 20 видов дрожжей способны аэробно расти на метаноле в качестве единственного источника углерода и энергии. Наиболее активно ассимилируют метанол такие виды, как Pichia polymorpha, Pichia pastoris, Candida boidinii, Candida methylica.
Тем не менее, сложные соединения (лигнин,
целлюлоза) для большинства дрожжей (за исключением некоторых видов рода
Trichosporon, проявляющих целлюлолитическую активность) недоступны [15].
1.2.1 Общая характеристика рода Debaryomyces
Род Debaryomyces, назван по имени знаменитого ботаника А. де Бари.
Клетки рода Debaryomyces имеют чаще круглую реже
яйцевидную или овальную форму. Виды со сферическими клетками размножаются
вегетативно множественным почкованием. Вегетативное размножение происходит
истинным многосторонним почкованием. Мицелий обычно отсутствует, реже
образуется примитивный псевдомицелий.
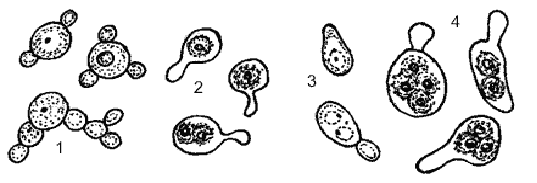
Рис. 3 - Различные типы организации у дрожжей
рода Debaryamyces: 1- почкующиеся клетки Debaryamyces hansenii; 2 - аски с
аскоспорами Debaryamyces hansenii; 3 - почкующиеся клетки Debaryamyces
vanrijiae; 4 - аски с аскоспорами Debaryamyces vanrijiae
Аски образуются в результате конъюгации между клеткой и ее почкой. Почка превращается в аск с 1-4 круглыми или слегка овальными аскоспорами с гладкой или бородавчатой поверхностью <#"876591.files/image004.jpg">
Рис. 4 - Схемы иммобилизации биоматериала на
преобразователе на примере ферментов: а - адсорбция; б - сшивка; в -
ковалентное связывание; г - сшивка и ковалентное связывание; д - включение
1.3.1 Химическая и физическая адсорбция
Одним из самых распространенных методов иммобилизации клеток является адсорбция, которая может быть физической или химической (хемосорбция). Адсорбцией пользуются, главным образом, на стадии исследований, когда достаточно слабого прикрепления биологического материала к преобразователю, а от сенсора не требуется длительной эксплуатации.
Ферменты адсорбируются на поверхности многих материалов. В числе таких материалов - алюминий, уголь, глина, целлюлоза, каолин, силикагелъ, стекло, коллаген и др. Для адсорбции не требуется ни дополнительных реагентов, ни отдельной стадии очистки. Метод практически не нарушает нативной конформации фермента или других белков. Однако белки располагаются неупорядоченно.
При физической адсорбции биоматериал удерживается Ван-дер-ваальсовыми силами, реже водородными и множественными солевыми связями и, в подходящих условиях, за счет образования комплексов с переносом электронов.
Химические методы иммобилизации клеток основаны
на образовании ковалентных связей между поверхностью клеток и материалом
носителя, то есть клетка химически пришивается к носителю. Это может
осуществляться как на поверхности соответствующего нерастворимого материала,
так и в объеме носителя (если при формировании матрицы в присутствии
иммобилизованных клеток происходят химические реакции присоединения,
затрагивающие функциональные группы биополимеров клеток).
1.3.2 Иммобилизация клеток путем включения в массу носителя (включение)
В методе включения биологический материал смешивают с раствором мономера, а затем к раствору добавляют инициатор полимеризации, в результате чего образуется гель, в который включен биоматериал. Полимерные гели предотвращают вымывание клеток микроорганизмов и обеспечивают доступ субстратов и кислорода.
Гель - система полимер-растворитель, пространственная сетка которой стабилизирована по всему своему объему устойчивыми во времени межмолекулярными связями. Различают гели 1-го и 2го рода. Пространственная сетка полимерных гелей 1-го рода образована ковалентными связями (химические сетки). Хорошо известными примерами таких материалов являются полиакриламидные гели, силикагель, гели типа сефадексов (поперечно-сшитые декстраны), полистирольные ионообменные смолы и др. В гелях 2-го рода пространственная сетка поддерживается за счет сил нековалентной природы (водородные связи, гидрофобные взаимодействия, зона образования кристаллитов; это - физические сетки). Примерами таких систем являются гели желатины, агара и агарозы, крахмала и др. Данным гелевым матрицам присуще обратимое плавление - застудневание при изменении температуры, поэтому их обычно называют термообратимыми. Существуют полимеры, растворы которых желируют при охлаждении (наиболее распространены), но есть высокомолекулярные соединения, растворы которых превращаются в гели при нагревании (например, водные растворы метилцеллюлозы) [8].
К недостаткам, связанных с использованием гелевых матриц относится: трудоемкость изготовления рецепторного элемента, необходимость специального подбора для каждого конкретного микроорганизма условий иммобилизации, снижение пластической прочности гелей после иммобилизации. Также через гели часто плохо диффундируют субстраты, что замедляет ферментативную реакцию. Кроме того, со временем фермент может вытекать из геля, что приводит к уменьшению биологической активности распознающего элемента.
Биорецепторные элементы на основе клеток, иммобилизованных в гелевых матрицах, как правило, характеризуются более низкими откликами по сравнению с элементами на основе адсорбированных клеток, причем для отдельных субстратов наблюдается резкое снижение откликов, то есть в зависимости от метода иммобилизации изменяется и субстратная специфичность клеток микроорганизмов. Это связано с тем, что при иммобилизации происходит полная или частичная блокировка активных центров ферментов, отвечающих за окисление этих субстратов. А так же затрудняется диффузия субстрата к клеткам.
Для иммобилизации биоматериала часто используется поливиниловый спирт. ПВС - доступный продукт многотоннажного синтеза, каждая его марка стандартизована, выбор этих марок достаточно широк. Известно так же что полимер-гелеобразователь поливиниловый спирт химически и микробиологически стабилен, нетоксичен и биосовместим [20], поэтому может быть эффективно использован в качестве матрицы для иммобилизации клеток микроорганизмов с целью увеличения пористости, долговременной и операционной стабильности биорецепторных элементов. [17]
В работе [21] описана модификация поливинилового
спирта (ПВС) N-Винилпирролидоном (ПВП). Предпополагаемый механизм сшивки
поливинилового спирта N-Винилпирролидоном с участием ионов Се+4 в качестве
инициатора, приводящего к появлению оксильных радикалов, приведен ниже:

Рис. 5 - Предполагаемый механизм
сшивки поливинилового спирта N-винилпирролидоном
Формирование рецепторного элемента может проведено путем включения клеток микроорганизмов в гель поливинилового спирта (ПВС), модифицированного N-винилпирролидоном (N-ВП), в силу того что N-поливинилпирролидон легко образует комплексы со многими соединениями (токсинами, лекарственными веществами, красителями), совмещается с различными веществами, лекарственными средствами, нетоксичен, является основой кровезаменителей. [22]
Схема включения клеток в гель на
основе поливинилового спирта, модифицированного N-Винилпирролидоном
представлена на (рис.6)
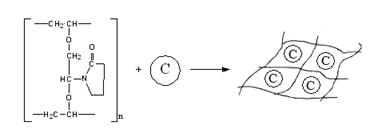
Рис. 6 - Включение клеток в гель на основе
поливинилового спирта, модифицированного N-Винилпирролидоном
1.4 Биохимическое потребление
кислорода
К основным показателям качества воды относят:
органолептические показатели: запах, вкус и привкус, мутность и прозрачность, пенистость;
- общие и суммарные показатели: температура, водородный показатель (рН), щелочность и кислотность, растворенный кислород (РК), биохимическое потребление кислорода (БПК), окисляемость, или химическое потребление кислорода (ХПК);
- минеральный состав: карбонаты, сульфаты, хлориды, сухой остаток, кальций, магний, общая жесткость, натрий, калий и т.д.;
- биогенные элементы: аммоний, нитраты, нитриты, фосфаты и общий фосфор;
- металлы: сумма тяжелых металлов, железо, алюминий;
- некоторые важнейшие показатели: фтор (фториды), хлор активный, нефтепродукты, поверхностно-активные вещества, фенолы.[23]
Биохимическое потребление кислорода (БПК) - один из часто используемых показателей загрязнения органическими веществами. Природными источниками органических веществ являются разрушающиеся останки организмов растительного и животного происхождения. Существуют также техногенные источники органических веществ: транспортные предприятия (нефтепродукты), целлюлозно-бумажные и лесоперерабатывающие комбинаты (лигнины), мясокомбинаты (белковые соединения), сельскохозяйственные и фекальные стоки и т.д.
В естественных условиях под действием
микроорганизмов происходит биохимическое окисление органических веществ:
окисляемое вещество - субстрат разлагается под действием растворенного в воде
кислорода, при этом выделяющаяся энергия расходуется на поддержание жизненных
процессов и роста клеточных веществ. Биохимическое потребление кислорода (БПК)
- это количество растворенного кислорода (мг), необходимое для окисления всех
биоразложимых органических отходов, находящихся в 1 дм3 воды. Если условно
принять суммарное соотношение жизненно необходимых элементов, входящих в состав
всех органических соединений, загрязняющих сточную воду, за соединение с
простейшей формулой CxHyOzN. Тогда расход кислорода при дыхании будет отвечать
следующей схеме [24]:
![]()
Коэффициенты перед кислородом означают:
х - на один атом углерода расходуется одна молекула кислорода;
у - на один атом водорода расходуется 1/4 молекулы кислорода.
Содержащийся в соединении кислород в величину БПК не входит, его вычитают, каждый атом составляет половину молекулы кислорода (z/2); азот восстанавливается до аммиака с затратой трех атомов водорода, что соответствует уменьшению количества кислорода еще на 3/4 молекулы.
При синтезе клеточных веществ
протекает примерно следующий процесс:
![]() , где
, где
C5H8O2N - среднее соотношение основных элементов в клеточном веществе бактерий.
Суммарное количество кислорода, израсходованного при этих процессах, и отвечает величине БПКполн.. В лабораторных условиях наряду с БПКполн. определяется БПК5 - биохимическая потребность в кислороде за 5 суток. Ориентировочно понимают, что БПК5 составляет около 70% БПКполн., но может составлять от 10 до 90% в зависимости от окисляющегося вещества.
Биохимическое окисление различных органических
веществ происходит с разной скоростью. Загрязнители различной природы могут
повышать (понижать) значение БПК. Динамика биохимического потребления кислорода
при окислении органических веществ в воде приведена на рис. 7.
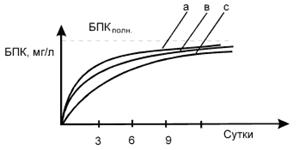
Рис. 7 - Динамика биохимического
потребления кислорода: а - легкоокисляющиеся вещества, в - нормально
окисляющиеся вещества, с - тяжело окисляющиеся вещества
К легкоокисляющимся («биологически мягким») веществам относятся глюкоза, мальтоза, формальдегид, низшие алифатические спирты, фенолы, фурфурол. Нормально окисляющиеся вещества - нафтолы, крезолы, резорцин, анионогенные ПАВ, сульфанол, пирокатехин и т.п. К тяжело окисляющимся («биологически жестким») веществам - неионогенные ПАВ, гидрохинон, тимол, сульфонол и т.п. [25]
Искажать характер потребления
кислорода может расходование кислорода на нитрификацию (рис.8)
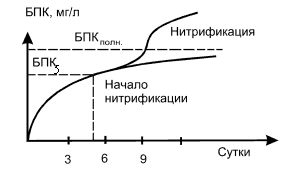
Рис. 8 - Изменение характера
потребления кислорода при нитрификации
Нитрификация протекает под
воздействием особых нитрифицирующих бактерий - Nitrozomonas, Nitrobacter и др.
Эти бактерии обеспечивают окисление азотсодержащих соединений, которые обычно
присутствуют в загрязненных природных и некоторых сточных водах, и тем самым
способствуют превращению азота сначала из аммонийной в нитритную, а затем и нитратную
формы. Соответствующие процессы описываются уравнениями:
2NH4+ + 3O2 = 2HNO2 + 2H2O + 2H+ + Q
2HNO2 + O2 = 2HNO3 + Q
где: Q - энергия, высвобождающаяся при реакциях.
Процесс нитрификации происходит и при инкубации пробы в кислородных склянках. Количество кислорода, пошедшее на нитрификацию, может в несколько раз превышать количество кислорода, требуемое для биохимического окисления органических углеродсодержащих соединений. Начало нитрификации фиксируется по минимуму на графике суточных приращений БПК за период инкубации. Нитрификация начинается приблизительно на 7-е сутки инкубации (см. рис. 10), поэтому при определении БПК за 10 и более суток необходимо вводить в пробу специальные вещества - ингибиторы, подавляющие жизнедеятельность нитрифицирующих бактерий, но не влияющие на обычную микрофлору (т.е. на бактерии - окислители органических соединений). В качестве ингибитора применяют тиомочевину (тиокарбамид), который вводят в пробу либо в разбавляющую воду в концентрации 0,5 мг/см3.[23]
Итак, полным биохимическим потреблением кислорода (БПКполн.) считается количество кислорода, требуемое для окисления органических примесей до начала процессов нитрификации.
В поверхностных водах величина БПК колеблется в пределах от 0,5 до 5,0 мг/дм3; она подвержена сезонным и суточным изменениям, которые, в основном, зависят от изменения температуры и от физиологической и биохимической активности микроорганизмов. Весьма значительны изменения БПК5 природных водоемов при загрязнении сточными водами.[26]
Норматив на БПКполн. не должен
превышать: для водоемов хозяйственно-питьевого водопользования - 3 мг/дм3, для
водоемов культурно-бытового водопользования - 6 мг/дм3. Соответственно можно
оценить предельно-допустимые значения БПК5 для тех же водоемов, равные примерно
2 мг/дм3 и 4 мгО2/дм3. В таблице 1 приведены значения БПК5 для водоемов разных
классов
Таблица 1 - Величины БПК5 в водоемах с различной степенью загрязненности
|
Степень загрязнения (классы водоемов) |
БПК5, мг/дм3 |
|
Очень чистые |
0,5-1,0 |
|
Чистые |
1,1-1,9 |
|
Умеренно загрязненные |
2,0-2,9 |
|
Загрязненные |
3,0-3,9 |
|
Грязные |
4,0-10,0 |
|
Очень грязные |
10,0 |
Определение БПК5 в поверхностных водах используется с целью оценки содержания биохомически окисляемых органических веществ, условий обитания гидробионтов и в качестве интегрального показателя загрязненности воды. Значение БПК говорит биологу о потенциальной возможности сточных вод истощать запасы кислорода в реке. Этот показатель - весьма важный индикатор загрязнения воды, так как недостаток кислорода приводит к гибели рыбы, а также порождает неприятный запах и развитие популяций нежелательных организмов, устойчивых к разного рода загрязнениям.