Материал: Определение характеристик макета БПК-биосенсора на основе дрожжей Debaryamyces hansenii, иммобилизованных в модифицированный ПВС с использованием различных синтетических сточных вод
Определение характеристик макета БПК-биосенсора на основе дрожжей Debaryamyces hansenii, иммобилизованных в модифицированный ПВС с использованием различных синтетических сточных вод
Введение
Последнее десятилетие отмечено интенсивным изучением аналитических возможностей и практическим применением биосенсорных систем. Экспресс-оценка степени загрязнения объектов окружающей среды органическими соединениями является необходимым компонентом экологического контроля. Учитывая постоянно растущий перечень веществ, поступающих как загрязнители в окружающую среду, эффективным инструментом анализа оказываются методы, основанные на интегральной оценке органических компонентов, а не только на определении содержания индивидуальных веществ. Потребности медицинской диагностики, различных областей биотехнологии, промышленности, экологических служб ставят перед аналитической химией комплекс задач, связанных с разработкой простых в применении, недорогих, высокочувствительных и специфичных
методов и приборов на их основе для обнаружения заданных веществ в образце.
Важной характеристикой степени загрязненности воды органическими веществами является индекс биохимического потребления кислорода (БПК). Стандартный метод определения БПК, регламентируемый в ПНДФ, основан на тестах, продолжительность которых составляет 5 или 20 суток. В силу значительной продолжительности процедуры метод не является адекватным, так как представляет результаты анализа со значительной задержкой. Вследствие этого возможно возникновение экологически опасных ситуаций.
Необходимо создание экспресс методов определения БПК. и реализация их требует разработки биоаналитический систем, основанных на применении низкоселективных биосенсоров.
Таким образом, создание универсального биосенсорного анализатора для определения БПК в современных условиях является важной задачей для биотехнологических производств.
Итак, целью данной курсовой работы является изучение характеристик кюветного БПК-биосенсора на основе дрожжевого штамма Debaryamyces hansenii с использованием двух стандартов: глюкозо-глутаматная смесь (ГГС) и ОЕСD-синтетические сточные воды.
При этом необходимо решить следующие задачи:
Во-первых, изучить метрологические (диапазон определяемых содержаний, правильность, воспроизводимость, повторяемость, чувствительность, предел обнаружения) и аналитические характеристики (длительность единичного анализа, время функционирования биосенсора без замены рецепторного элемента) кюветного БПК-биосенсора на основе дрожжевого штамма Debaryamyces hansenii с использованием двух стандартов: глюкозо-глутаматная смесь (ГГС) и ОЕСD-синтетические сточные воды.
Во-вторых, определить БПК реальных образцов стандартным методом разбавления.
В-третьих, применить БПК-биосенсор на основе дрожжевого штамма Debaryamyces hansenii для анализа образцов сточных води полупродуктов брожения, так же с использованием ГГС и ОЕСD.
1. Литературный обзор
.1 Общая характеристика микробных биосенсоров
.1.1 Современная концепция биосенсоров
Согласно определению Энтони Тернера биосенсор - это аналитическое устройство, содержащее биологический материал (ткани, клетки микроорганизмов, органеллы, клеточные рецепторы, ферменты, иммуноактивные компоненты, нуклеиновые кислоты и т.д.), находящийся в непосредственном контакте с физико-химическим преобразователем или преобразующей микросистемой, представленными оптическим, электрохимическим, термометрическим, пьезоэлектрическим или магнитометрическим устройствами. Как правило, преобразователь вырабатывает периодическое либо непрерывные аналоговые/цифровые сигналы, которые пропорциональны концентрации одиночного вещества или группы анализируемых соединений.[1]
Биосенсоры можно разделить на различные группы в соответствии с типом преобразователя (физический сенсор, регистрирующий изменение физико-химических свойств биоматериала, составляющего биорецептор) или биорецепторного элемента (основной анализирующий элемент сенсора, содержащий биологический материал (ферменты, клетки, срезы тканей, органеллы антитела/антигены, молекулы ДНК, РНК), реакция которого регистрируется преобразователем). По типу преобразователя биосенсоры можно разделить на следующие группы: электрохимические, оптические, пьезоэлектрические, термометрические. По типу биорецепторного элемента биосенсоры классифицируют на иммунохимические, ферментные, целоклеточные, рецепторные и ДНК-сенсоры.
Микробные сенсоры представляют собой иммобилизованные на преобразователях различных типов (оптических, электрохимических) клетками микроорганизмов, что позволяет достаточно простыми методами производить оценку концентрации многих органических соединений, осуществимую в ряде случаев лишь с помощью длительных химических процедур анализа. Наиболее часто используют преобразователи электрохимического типа [2]. Использование микроорганизмов в качестве основы биосенсоров является известным подходом. В ряде работ показано, что микробные биосенсоры могут быть эффективно использованы для анализа широкого спектра соединений при биотехнологических процессах и экологическом мониторинге. Важными моментами, указывающими на перспективность микробных биосенсоров, является многообразие ферментативного аппарата микробных клеток, что открывает возможность подбора микроорганизмов для анализа практически любого соединения, а также тот факт, что ферменты внутри клеток находятся в "эволюционно оптимизированных условиях" - это в ряде случаев приводит к высокой стабильности аналитических сигналов. Немаловажным с практической точки зрения фактором является более низкая стоимость микробных биосенсоров по сравнению с ферментными ввиду отсутствия необходимости очистки ферментов и использования кофакторов. Перечисленные факты обуславливают актуальность исследований, направленных на совершенствование и получение новых знаний в этой области. Принцип детекции, реализованный в биосенсорах, основан на том, что биоматериал (ферменты, клетки, антитела и др.), иммобилизованный на физическом датчике (преобразователе), при взаимодействии с определяемым соединением генерирует зависимый от его концентрации сигнал, который регистрируется преобразователем электрохимического, оптического или иного типа. Эти изменения могут непосредственно быть зарегистрированы электрохимическими датчиками, например, кислородным электродом или рН - метром.[3]
При использовании амперометрического
кислородного электрода измерение основано на регистрации тока, полученного при
восстановлении молекулярного кислорода. Сила тока пропорциональна концентрации
кислорода в исследуемом образце.
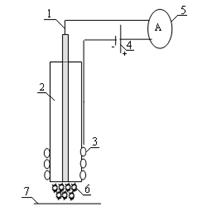
Рис. 1 - Схема кислородного электрода типа
Кларка с рецепторным элементом
Рассмотрим схему кислородного электрода типа Кларка с рецепторным элементом (рис.1). Электрод типа Кларка представлен измерительной парой - платиновым катодом и серебряным анодом.
. Платиновый электрод
. Стеклянный корпус
. Электрод сравнения (Ag/AgCl)
. Источник тока (U = -0,7 В)
. Амперметр
. Слой фермента или клеток
. Полупроницаемая мембрана
Потенциал поляризации - 0,7 В, приложенный к катоду относительно анода, восстанавливает на катоде кислород в соответствии с реакцией:
Катодная реакция: О2 + 2Н2О + 4ē → 4ОН¯
Анодная реакция: 4Ag + 4Cl¯ → 4AgCl + 4ē
Указанные химические реакции приводят к протеканию тока, который пропорционален парциальному давлению кислорода. Кислородный электрод поглощает кислород, который поступает к его поверхности из раствора
Помимо электродов типа Кларка существуют также безмембранные (открытые) кислородные электроды, но в сравнении с ними электрохимической ячейке электродов Кларка есть ряд преимуществ:
возможность измерения кислорода в газах и растворах
не приводят к взаимному загрязнению среды и электрода
сигнал в меньшей степени зависит от скорости потока
В связи с этим электроды типа Кларка получили
широкое распространение в настоящее время. К наиболее важным параметрам
электрода относиться толщина пленки электролита между мембраной и электродом -
она должна быть заключена в довольно узком интервале (рис.1) и в значительной
мере определяет нулевой ток и линейность измерений. Для каждого электрода можно
построить калибровочную зависимость, которые в большинстве случаев имеют
сигмоидальный или гипербоидальный вид, характерный для кинетики ферментативных
реакций. [4]
1.1.2 Биосенсоры на основе целых клеток.
Микроорганизмы - это живые датчики, которые меняют чувствительность при адаптации или сенсибилизации. Реакция таких датчиков зависит от взаимодействия целой группы факторов, отражая множество тонких и важных изменений в окружающей среде или среде организма.
В результате усвоения микроорганизмами органических веществ изменяется их дыхательная активность (процессы получения химической энергии за счет окисления органических веществ)
В начале 70-х годов XX в. исследователи показали, что не только ферменты, но также и целые клетки, в первую очередь микроорганизмы, могут успешно использоваться в биосенсорах. Первый микробный сенсор использован для определения этанола и представлен бактериями Acetobacter xylinum описан в работе [5].
С точки зрения функционирования клеточного биосенсора во многом аналогично функционированию ферментативного, вместе с тем применение целых клеток имеет некоторые преимущества в сравнении с использованием ферментов. Клетки - доступный биологический материал. Клетки микроорганизмов культивируются, легко воспроизводятся и поддерживаются в чистой культуре. В отличие от ферментов клетки не требуют дорогостоящих стадий очистки. Клетки сохраняют все наиболее важные структуры и проявляют большую стабильность. В некоторых случаях они обеспечивают жизнеспособность и активность ферментных систем в течение нескольких лет. Это позволяет проводить сложные последовательные реакции, осуществляя многостадийные процессы. Для многих типов клеток, особенно микробных, предложены эффективные методы генетических операций, что открывает возможность для работы с высокоэффективными каталитическими системами.
Другим важным преимуществом целых клеток является возможность использования их чувствительности к взаимодействию целой группы факторов, отражая множество тонких и важных изменений в окружающей среде или среде организма.
Таким образом, биосенсоры на основе целых клеток микроорганизмов могут быть использованы не только для определения содержания индивидуальных соединений в анализируемых объектах, но и для определения таких комплексных показателей загрязнения водных сред как биологическое потребление кислорода (БПК), цитотоксичность, мутагенность и т.д. Так, известно большое количество лабораторных моделей и несколько промышленно выпускаемых биосенсорных анализаторов БПК. В Германии, Бельгии, Японии и ряде других стран этот важный показатель качества воды определяют только экспресс-методом с использованием биосенсоров. Такие анализаторы позволяют производить определение БПК в среднем диапазоне 5-300 мг/л за время порядка нескольких минут. [6]
Несмотря на перечисленный положительные качества клеточных сенсоров, они имеют определенные недостатки:
клетки содержат множество ферментов, часть которых может взаимодействовать с соединениями, присутствующими в пробе и не относящимися к целевым. В этом случае возникает сигнал наличия целевого соединения и соответствующая ошибка анализа;
реакции протекают более медленно, так как субстраты должны проникнуть в клетку через мембрану, кроме того по такому же пути продукт должен выйти из клетки. Поэтому некоторые субстраты, в особенности макромолекулярные, не могут быть использованы для детекции клеточными биосенсорами;
различные метаболические пути утилизации субстрата в клетке могут быть источником побочных продуктов, регистрируемых преобразователем; это приводит к снижению селективности клеточного биосенсора;
- высокая приспособляемость и изменчивость микроорганизмов;
- проблема биологической устойчивости, связанная с необходимостью длительного хранения и поддержания жизнедеятельности микроорганизмов. [7]
Областями наиболее интенсивного применения микробных сенсоров являются ферментационный и экологический контроль. Например, Гильбо [8,9] приводит многочисленные примеры использования микроорганизмов для создания биосенсоров: Neigrospora europea - для определения аммиака, Trichosporon brassicae - для определения уксусной кислоты, Sarcina flava - для определения глутамина, Azotobacter vinelaudit - для определения нитратов и другие. Живые организмы (дрожжи, бактерии, клетки растений) используют в методах биоиндикации для выявления вредных веществ. По различию характеристик прироста в опыте и контроле определяют предельную концентрацию вещества, обнаруживаемую организмами. Для оценки токсичности в питательные среды с микроорганизмами вводят не только растворы исследуемых химических веществ, но и экстракты, извлекаемые с помощью растворителей из тканей, почв и т.п [6].
Спектр микроорганизмов, используемых в
биорецепторах, довольно широк, однако эффективное применение микробных клеток
возможно при наличие представлений об особенностях их физиологии, а также
информации о наборе ферментов, присущих выбранному штамму, так как
физиологические свойства микроорганизмов определяют чувствительность,
специфичность, стабильность биорецептора и другие параметры работы биосенсора.
1.2 Особенности биохимии дрожжевых
клеток
Дрожжи представляют собой одноклеточные
неподвижные организмы. Они могут быть различной формы: эллиптической, овальной,
шаровидной и палочковидной (рис 2). Длина клеток колеблется от 5 до 12 мкм,
ширина - от 3 до 8 мкм.
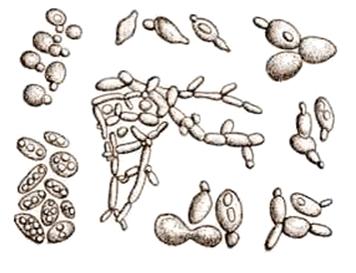
Рис. 2 - Различные формы дрожжей
Необходимую энергию для жизнедеятельности дрожжи получают в процессе дыхания. Существует два типа дыхания: аэробное, или настоящее дыхание, и анаэробное, или брожение. По соотношению процессов анаэробного и аэробного дыхания дрожжи можно разделить на несколько групп:[10]
) Дрожжи, существующие только за счет брожения, и не способные расти в аэробных условиях. Например, вид Arxiozyma telluris, обитающий в кишечном тракте грызунов.
) Активные бродильщики: интенсивно сбраживают различные субстраты, но в аэробных условиях переключаются на дыхательный обмен. Представители: Saccharomyces cerevisiae, Schizosaccharomyces pombe.
) Слабые бродильщики - в основном существуют за счет аэробного дыхания, но в анаэробных условиях могут бродить, однако значительно менее интенсивно, чем виды из предыдущей группы. Например, дрожжи из родов Pichia, Debaryomyces.
) Дрожжи, существующие только за счет дыхания, и не способные расти в анаэробных условиях. К этой группе относятся дрожжи из рода Lipomyces, Cryptococcus, Rhodotorula, Sporobolomyces.
Таким образом, дрожжи используют кислород для дыхания, однако при его отсутствии многие виды способны получать энергию за счёт брожения с выделением спиртов (спиртовое, молочнокислое, пропионовокислое, муравьинокислое, маслянокислое, уксусное брожение). В отличие от бактерий, среди дрожжей нет штаммов, гибнущих при наличии кислорода в среде. При пропускании воздуха через сбраживаемый субстрат дрожжи прекращают брожение и начинают дышать (поскольку этот процесс эффективнее, так как клетка лучше снабжается энергии, чем при брожении и молекула органического соединения расщепляется более глубоко), потребляя кислород и выделяя углекислый газ. Это ускоряет рост дрожжевых клеток (эффект Пастера). Однако даже при доступе кислорода в случае высокого содержания глюкозы в среде дрожжи начинают её сбраживать (эффект Кребтри) [11]. При брожении для получения энергии расходуется большое количество исходного материала, но зато при брожении создаются условия, в которых не могут развиваться другие микробы, конкурирующие с дрожжами, вызывающими брожение. Так, продукт спиртового брожения этанол оказывает губительное действие на многие бактерии и плесени.
Важно также отметить, что все бродящие дрожжи сбраживают глюкозу и фруктозу, поскольку именно с этих сахаров начинается гликолитическое расщепление. Кроме глюкозы и фруктозы могут сбраживаться другие соединения, такие как гексозы и построенные из них олигосахариды. Например, некоторые виды (Pichia stipitis, Pachysolen tannophilus, Phaffia rhodozyma) усваивают и пентозы, например, ксилозу.[12] Schwanniomyces occidentalis и Saccharomycopsis fibuliger способны сбраживать крахмал [13], Kluyveromyces fragilis - инулин (полифруктозан) [14]. Из моносахаридов наиболее часто сбраживается галактоза, из дисахаридов - сахароза, мальтоза, трегалоза. Значительно реже встречаются дрожжи, сбраживающие лактозу и мелибиозу.